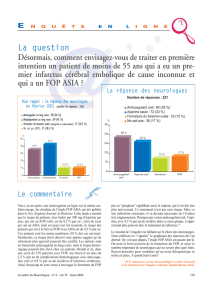
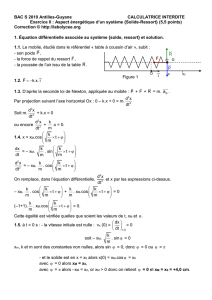
Diagnostic de perméabilité du Foramen Ovale (FO) en scanner

Diagnostic de perméabilité
du Foramen Ovale (FO)
en scanner multicoupe
cardiaque
Léonardo Botallo (1519-1588)
Explication anatomique et physiologique
du trou de Botal (Foramen Ovale) et du
canal artériel.
PA GANNE (1), S TISSIER(1), M. ANDRONACHE (2),
C BARBARY (1), A HUEBER (2), L MEYER-BISCH (1),
C DE CHILLOU (2), C CHABOT (3), D REGENT (1)
CHU Nancy - 2005 -
Département de radiologie (1)
Département de cardiologie (2)
Réanimation respiratoire (3)

Rappels d’embryologie
Rappels d’embryologie
Pendant la vie fœtale :
- Afflux veineux oxygéné dans l’oreillette droite
(AD) en provenance de la veine ombilicale, s’ajoutant au
flux en provenance de la VCI
- Poumons collabés : la circulation droite est un
territoire résistif à haute pression
- Création d’un shunt ADAG via le Foramen
Ovale (2)
Cloisonnement de l’oreillette primitive (4-6e semaine)
- Face septale de l’AG = septum primum, endocardique
- Face septale de l’AD = septum secundum, musculaire
Ces deux septa ont une croissance centripète, laissant un pertuis
central plutôt crânial à gauche (ostium primum) et plutôt caudal à droite
(ostium secundum).
Le foramen ovale (anciennement trou de Botal) correspond à la
persistance d’un canal entre ces deux septa (phénomène de valve à
trajet oblique
trajet oblique) (1).

Rappels d’embryologie
Rappels d’embryologie
A la naissance :
- La ventilation des poumons fait réduire significativement les
pressions des cavités cardiaques droites
- Parallèlement, la pression dans les cavités gauches augmente
Inversion du shunt
Inversion du shunt
Phénomène de clapet entre le septum primum et le
septum secundum
Fermeture spontanée du FO
Fermeture spontanée du FO
(chez environ 75 % des individus) (7)

Anatomie descriptive
Anatomie descriptive
- Situé au niveau de la fossette ovale,
portion la plus fine du septum inter-atrial
- Correspond au pertuis résiduel entre le
septum primum (épais, versant AG) et le
septum secundum (fin, versant AD) (2,3)
La valve de la VCI d’Eustachi oriente le
flux veineux ascendant vers le FO,
pouvant le maintenir ouvert et perméable
Foramen ovale perméable = défect septal atrial

Épidémiologie
Épidémiologie
•Foramen ovale perméable (FOP) est le
shunt cardiaque le plus fréquent.
•Prévalence : 17 à 30 % des individus (1)
•
•Plus fréquent à l’âge jeune
Plus fréquent à l’âge jeune : jusqu’à
34% chez les moins de 30 ans (séries
autopsiques) (3).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%