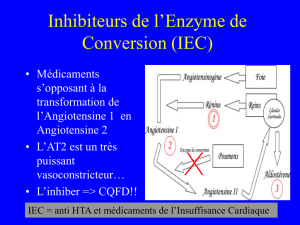
Vial_Med_Risque - Les Jeudis de l`Europe

Médicaments et
personnes âgées
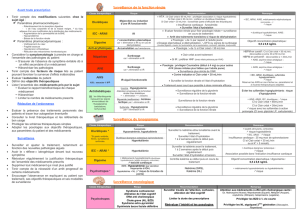
Principales classes
médicamenteuses à risque

Médicaments à risque
(Afssaps, juin 2005)
Cardiotropes et médicaments de la coagulation
AVK et héparines
Diurétiques
IEC, sartans, béta-bloquants, calcium-bloquants, nitrés
Digitaliques et antiarythmiques
Psychotropes
Antidépresseurs, thymorégulateurs
Anxiolytiques et hypnotiques, neuroleptiques
AINS
Antidiabétiques
Antibiotiques
Statines
Médicaments de la démence

Antivitamines K
1% de la population traitée
Forte liaison aux protéines plasmatiques
Effet prolongé après l’arrêt du traitement
Médicament Demi-vie Durée d’action
Demi-vie courte Sintrom 8-9 h 2-4 j
Demi-vie
longue
Préviscan
Coumadine
30 h
35-45 h
3-4 j
4-5 j

Incidence des
hémorragies sous AVK
Hémorragies majeures
• 1,2 à 5,6 pour 100 Patient/Année
•1000 patients /an Midi-Pyrénées
Hémorragies fatales
• 0,24 à 0,8 pour 100 Patient/Année
•200 patients / an Midi-Pyrénées
Accidents hémorragiques en 1998
• 17000 hospitalisations
• 13 % des hospitalisations pour iatrogènie
• 800 hémorragies cérébrales : 8 % dues aux AVK

Facteurs de risque
d’hémorragie sous AVK
Durée et intensité du traitement
• INR > 4,5: risque x 6
• Un point d’INR: risque x 2
• Instabilité de l’INR (préférer les AVK à ½ vie longue)
Autres facteurs de risque
• Age > 75 (x 2,5)
• Trois premiers mois de traitement
• Comorbidité: HTA, IC sévère, IH, IRC, AVC, cancer
• Hypoalbuminémie
• ATCD de saignements digestifs
• Maladies intercurrentes infectieuses
• Associations médicamenteuses / Alimentation
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
1
/
67
100%