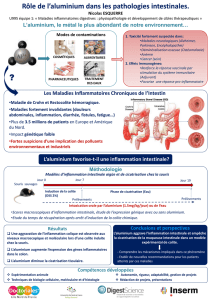
FACTEURS ENVIRONNEMENTAUX AU COURS DES MICI

Cours05
1
Auteur : Pierre DESREUMAUX
La réponse inflammatoire muqueuse au cours des MICI
Introduction
La maladie de Crohn (MC) et la rectocolite hémorragique (RCH) sont des maladies inflammatoires
chroniques de l’intestin (MICI), évoluant par poussées entrecoupées de périodes de rémission. Cette
évolution particulière est à l’origine de lésions d'âge différent que l'on peut distinguer
macroscopiquement et histologiquement en lésions aiguës et chroniques.
L’origine des MICI est encore inconnue et la susceptibilité génétique ne suffit pas à expliquer leur
développement. L’hétérogénéité spatiale et temporelle des MICI, l’étude des jumeaux homozygotes et
des populations migrantes plaident en faveur de facteurs environnementaux. Le tabagisme et
l’appendicectomie sont à ce jour les deux seuls facteurs environnementaux clairement impliqués dans
le développement et l’évolution des MICI. La consommation active de tabac a des effets opposés au
cours des MICI : elle protège contre la RCH et améliore son évolution mais favorise le développement
de la MC et l’aggrave. De nombreux facteurs environnementaux ont été impliqués dans la
physiopathologie des MICI tels que l’allaitement maternel, certains aliments, les contraceptifs oraux, les
vaccinations, le stress et certains microorganismes. Ces facteurs en cours d’investigation restent
discutés. Les modifications de notre mode de vie depuis quarante ans pourraient participer à
l’augmentation de la fréquence des MICI : l’hygiène, la modification de l’alimentation et la pollution
industrielle sont trois changements majeurs qui pourraient directement ou par la modification de la flore
intestinale participer à l’apparition des MICI.
Les avancées récentes dans la physiopathologie des MICI ont permis de mettre en évidence le rôle
important de la flore intestinale, l’implication de microorganismes spécifiques et une perturbation des
interactions hôte/bactéries. Les MICI sont caractérisées par une dysrégulation de la réponse
immunitaire muqueuse, dirigée contre des éléments de la flore intestinale, survenant chez des patients
génétiquement déterminés. L’activation de cette réponse immunitaire se traduit par la mise en jeu d’une
cascade de mécanismes.
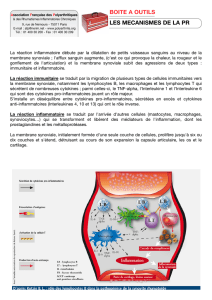
Le premier est la stimulation anormale des cellules résidentes dans la muqueuse intestinale, à
l’origine de l’activation de voies de transduction (voies de NFκB et des kinases de stress). Cette
activation permettra la production de médiateurs inflammatoires (cytokines et chimiokines) qui

Cours05
2
Auteur : Pierre DESREUMAUX
seront également impliqués dans le recrutement de nouvelles cellules inflammatoires sanguines dans la
paroi intestinale via la surexpression de molécules d’adhésion (Figure 1). Ces deux premiers
mécanismes vont aboutir à la formation, dans la paroi intestinale, d’un infiltrat de cellules pro-
inflammatoire activées. Un dernier mécanisme pathologique, caractérisé par une inhibition des
mécanismes de mort naturelle des cellules (apoptose), entraînera une augmentation de la survie de
ces cellules pro-inflammatoires dans la muqueuse intestinale et donc la chronicité de l’inflammation.
Cette activation anormale du système immunitaire intestinal est associée à une rupture de la
tolérance vis-à-vis de sa propre flore intestinale faisant intervenir une augmentation de la perméabilité
de la barrière intestinale, des anomalies fonctionnelles des cellules épithéliales/cellules de Paneth, et
des anomalies de lymphocytes T particuliers appelés lymphocytes T régulateurs.
Activation des voies de transduction
Les deux principales voies de transduction du signal impliquées dans les phénomènes
inflammatoires sont les voies de NFκB/IκB et des kinases de stress ou protéines kinases activées par
des mitogènes (MAPK)(Figure 2). L’hétérodimère NFκB/IκB est présent dans le cytoplasme de toutes
nos cellules. Après activation de la cellule, une cascade de phosphorylation entraîne une dégradation
de la protéine inhibitrice IκB permettant la translocation de NFκB du cytoplasme vers le noyau de la
cellule. Lors de sa translocation nucléaire, NF-κB se fixe sur l’ADN est induit l’expression de nombreux
gènes impliqués dans la production de cytokines inflammatoires, de facteurs de croissance, de
chimiokines, de molécules d’adhésion, d’enzymes … (1). Classiquement, ce facteur est considéré
comme un élément clef dans l’initiation d’une réaction inflammatoire systémique mais pourrait avoir
également un rôle protecteur en fonction des stades évolutifs de la maladie (2).
La voie des MAPK est constituée d’une cinquantaine de facteurs de transcription cytoplasmiques
organisés en 3 modules : les MAP kinases kinases kinases (MAPKKK), les MAP kinases kinases
(MAPKK) et les MAP kinases (MAPK). L’activation de ces 3 modules par des facteurs de stress sera
essentiellement à l’origine de 3 facteurs (p35, JUNK et ERK) qui vont pouvoir passer dans le noyau de
la cellule et activer des gènes impliqués dans la réaction inflammatoire (Figure 2).
Dans les MICI, plusieurs travaux ont mis en évidence une augmentation dans la muqueuse
intestinale de l’activation des voies de NFκB/IκB et des MAPK. Le rôle pathologique de cette activation

Cours05
3
Auteur : Pierre DESREUMAUX
locale a surtout été apprécié dans les modèles de colite expérimentale où des inhibiteurs de la voie de
NFκB (oligonucléotide antisens codant pour la p65 de NFκB ou inhibiteur enzymatique (OXIS)) ou des
MAPK (anti p38) ont été utilisés avec succès pour le traitement de ces animaux. Plusieurs essais
thérapeutiques ont été réalisés chez des patients atteints de MC ou de RCH. Les résultats actuels pour
cette classe de médicaments sont très décevants avec notamment, pour le seul essai de phase III
réalisé, une absence d’efficacité d’un inhbiteur de MAPK (BIRB 796) chez les patients atteints de MC
active (3). Cette absence d’efficacité peut s’expliquer par la dualité fonctionnelle de l’activation de la
voie NF-κB par les cellules épithéliales intestinales, capable d’induire une inflammation systémique
mais également de protéger localement l’intestin de phénomènes apoptotiques provoqués par des
facteurs physiques, chimiques ou infectieux (Figure 3)(2). Ces résultats sont importants à considérer
pour le développement d’inhibiteur de NF-κB capable en théorie de diminuer l’inflammation systémique
mais inversement de l’augmenter localement.
Production de cytokines et de chimiokines
Classification des cytokines et chimiokines
Les cytokines sont des protéines solubles de faible poids moléculaire impliquées dans la
communication entre les cellules. Elles peuvent être synthétisées par plusieurs types cellulaires. Elles
sont produites localement en faible quantité et ont une demi-vie courte, ce qui rend difficile leur
détection et explique l’intérêt des techniques d’identification par amplification génique (PCR). Les
cytokines sont exprimées à l’état physiologique dans la muqueuse intestinale et des techniques
quantitatives d’analyse sont nécessaires pour leur attribuer un éventuel rôle physiopathologique. Depuis
la mise en évidence de la première cytokine en 1957, plusieurs classifications basées sur la structure et
les principales fonctions de ces médiateurs ont été proposées. Malgré l’existence de nombreuses
boucles de régulation et l’étonnant pléiotropisme fonctionnel des cytokines, 3 grands groupes ont été
caractérisés : les cytokines inflammatoires/anti-inflammatoires, les cytokines immunorégulatrices et les
chimiokines (Figure 4). La balance entre les cytokines inflammatoires (IL-1, IL-6, IL-8, TNFα) et anti-
inflammatoires (antagoniste du récepteur de l’IL-1 (IL-1RA), IL-10, TGFβ) gère localement l’intensité et
la durée de la réaction inflammatoire. Elle peut-être également à l’origine d'effets systémiques tels que
la diminution de la synthèse de l'albumine et l'augmentation de la synthèse de protéines inflammatoires.
Les cytokines immunorégulatrices interviennent dans i) la susceptibilité/résistance aux agents

Cours05
4
Auteur : Pierre DESREUMAUX
infectieux, ii) les mécanismes allergiques et iii) la régulation des cytokines inflammatoires. Elles sont
classées en 2 types appelés chez l’homme type 1 ou type 2 par analogie avec la classification proposée
par Mossman et collaborateurs chez la souris pour les clones lymphocytaires T CD4+ (profils Th1 et
Th2)(Figure 4). Les cytokines immunorégulatrices de type 1 sont représentées par l’IL-2 et l’IFNγ. Elles
sont impliquées dans l'activation du système immunitaire cellulaire et la résistance aux infections
bactériennes, les réactions d'hypersensibilité retardée et la synthèse d'IgG2a. Les cytokines de type 2
(IL-4, IL-5 et IL-13) interviennent préférentiellement dans la synthèse d’IgE, l'activation et le recrutement
des éosinophiles, la résistance aux infections parasitaires, les mécanismes allergiques et la
susceptibilité aux infections bactériennes.
Récemment, une nouvelle famille de lymphocytes T exprimant le récepteur nucléaire RORγ appelée
Th17 (4), induits par l’IL-6-TGFβ, stabilisés par l’IL-23, et caractérisés par leur capacité à produire de
l’IL-6 et IL-17 a été mise en évidence au sein du système immunitaire muqueux intestinal (Figure 5).
Ces lymphocytes Th17 et cette production d’IL-23 jouent un rôle important dans l’immunité muqueuse
spécifique et innée, la défense contre les pathogènes extracellulaires et les infections fungiques,
l’initiation de mécanismes inflammatoires chroniques intestinaux (4), dépendants ou non de la présence
de lymphocytes T ou B (Figure 5).
Les chimiokines définissent un sous groupe d’une cinquantaine de médiateurs caractérisés par leurs
propriétés chimioattractantes (5). En fonction de leur structure, on distingue essentiellement 2 sous-
familles : les CXC chimiokines représentées notamment par l’IL-8, GROα, β, γ impliquées dans le
recrutement et l’activation des polynucléaires neutrophiles et les CC chimiokines dont MCP-4 et 5,
RANTES et l’éotaxine impliquées avec l’IL-5 dans l’activation et le recrutement des éosinophiles dans
les tissus.
Les cytokines agissent sur les cellules cibles en se fixant sur des récepteurs spécifiques qui vont
activer une cascade d’événements intracellulaires et notamment les voies de NFκB/IκB et des MAPK. Il
y aura donc des boucles autocrines et/ou paracrines entre ces signaux de transduction et la production
de cytokines inflammatoires dont les éléments régulateurs restent actuellement mal connus. La
découverte de ces signaux intracellulaires a permis de mieux comprendre les mécanismes d’action des
cytokines et de développer des molécules capables de bloquer à leur base la transcription de gènes
induite par plusieurs cytokines (Figure 2).

Cours05
5
Auteur : Pierre DESREUMAUX
Cytokines et modèles animaux de colite
Trois groupes d’une cinquantaine modèles animaux développant des colites inflammatoires ont
été décrits (Tableau 1)(6). Le premier groupe est représenté par les modèles de colite spontanée
survenant chez des animaux manipulés génétiquement. Ces animaux peuvent être invalidés pour un
gène (animaux knockout), ou exprimer anormalement un gène (animaux transgéniques ou transfert de
gène dans un tissu). Les deux autres groupes développent des colites induites soit par le transfert de
cellules activées (transfert de lymphocytes T chez la souris immunodéficiente SCID), soit par des
agents chimiques (indomethacine, acide trinitrobenzène sulfonique (TNBS), sulfate de dextran sodique
(DSS), acide acétique), soit par des produits bactériens (peptidoglycane-polysaccharide (PGPS)). La
majorité des lésions chroniques dans ces modèles animaux est située dans le côlon (Figure 6).
Les lésions intestinales dans tous ces modèles sont associées à une augmentation de la
synthèse des cytokines inflammatoires. Si l’on considère les cytokines immunorégulatrices, les lésions
de colite chronique sont associées à une augmentation de la synthèse de cytokines de type 1 (IL-2 ou
IFNγ)(7). Ainsi, l’IFNγ joue un rôle important dans l’induction et la chronicité des lésions dans les
modèles de souris invalidées pour le gène codant pour l’IL-10 ou pour la protéine inhibitrice de
transduction Gαi2 ainsi que lors du transfert de cellules T activées (CD45RBhigh) chez la souris SCID
(Figure 7). Plus récemment, il a été également montré que les lymphocytes Th17 via l’IL-23 ont une
plus grande capacité d’induction d’une colite que les lymphocytes Th1 dans le modèle de transfert chez
des souris SCID. Plusieurs travaux ont mis en évidence l’importance des cytokines de type 2 dans
l’induction des lésions coliques (Figure 8). Dans les modèles de colite spontanée (souris invalidée pour
la chaîne α du récepteur T) ou induite par des agents chimiques (TNBS), les profils de cytokines
évoluent en fonction de l’ancienneté des lésions intestinales: les lésions aiguës sont associées à une
augmentation de la synthèse d’IL-4 et à la production locale d’IgE, l’évolution des lésions vers la
chronicité est précédée par une modification des profils de cytokines immunorégulatrices d’un type 2
vers un type 1. Enfin, des lésions inflammatoires iléales et coliques mimant des MICI ont été décrites
chez les souris transgéniques pour l’IL-5 et l’IL-4, deux cytokines de type 2.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%