Chimio-embolisation hépatique pour le traitement des CHC par voie

Chimio-embolisation hépatique pour le traitement des
CHC par voie radiale : fin de la voie fémorale ?
C.PROUST, AF MANICHON, A RODE, JC JOUVET, JF BERGEROT, LOIC BOUSSEL- LYON -
France.

PLAN
INTRODUCTION
TECHNIQUE DE LA VOIE RADIALE
MATERIEL ET METHODE
OBJECTIFS DE L’ETUDE
POSITIONNEMENT DE L’ETUDE
CONCLUSIONS
DISCUSSION
LIMITES
RESULTATS
BIOBLIOGRAPHIE

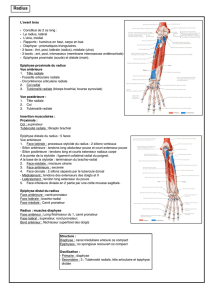
Introduction
① La voie radiale est en constante augmentation depuis de nombreuses années en raison des
modifications des pratiques en cardiologie pour la réalisation des coronarographies. Cependant, malgré
cette croissance constante, elle ne représente encore que 10 % des procédures (coronarographies) dans
le monde.
②L’utilisation de la voie radiale est largement absente des communautés de radiologie interventionnelle et
chirurgie vasculaire.
③L’artère brachiale (humérale) continue d’être l’artère du membre supérieure la plus utilisée pour les
procédures de radiologie interventionnelle non coronarienne.
④Les raisons de cette sous utilisation de cette voie d’abord sont le plus souvent un manque de formation,
une inadéquation de longueur de cathéter ou un manque de forme appropriée des matériaux utilisés.
⑤Il y a plusieurs avantages évident de la voie radiale à la voie fémorale. L’artère radiale est plus
superficielle que la fémorale et il n’y a pas les structures environnantes qui sont vulnérables aux
blessures. L’artère est facilement compressible et les patients préfèrent souvent cette voie d’abord.
⑥La chimio-embolisation hépatique pour le traitement des CHC est une procédure courante en radiologie
interventionnelle. Il s’agit de l’un des gestes les plus réalisés en dehors des drainages.
⑦La population traitée présente le plus souvent des troubles de la crase du fait de l’atteinte hépatique ce
qui accroit le risque de complications vasculaires de la voie d’abord. Ce sont tous ces facteurs qui nous
ont inciter à tester la voie radiale.

Technique voie radiale
Matériel en plus à prévoir pour une voie radiale :
Une aguille hypodermique orange de 25 G pour anesthésie locale.
Une ampoule d’héparine pour injecter IVD une fois le désilet posé 50 UI/kg avec max de 5000 unités.
Une cupule avec une ampoule de Risordan © (ampoule de 10 ml : 10 mg/10 ml).
Un guide Terumo © standard 0.035 mm de 180 cm et non 150 cm.
Un guide Medtronic © 0.035 mm de 175 cm.
Un désilet spécial voie radial (coronarographie) court 5F avec aiguille poncteur jupe.
Une Sonde vertébrale 4F de 125 cm Merit Medical ©.
Un bracelet compressif spécial voie radial Terumo © de 18 ml.
Prévoir si besoin à portée de main :
Une sonde JR4 5F de 125 cm (sonde de coronarographie = coronaire droite diagnostique).
Un microcathéter Merit Medical ©.de 150 cm + micro guide Terumo © de 0,018 mm de 183 cm.
Sonde vertébrale 4F 125 cm
Guide Medtronic

Désilet voie radiale 5F
Bracelet compressif voie radiale
Micro cathéter de 150 cm
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
1
/
23
100%