Cours distribué - WORD v2012-2013 partie chimie

Classes de 5
e
Lycée Aline Mayrisch
Nom :______________________________
C H I M I E / P H Y S I Q U
E
Physique
Classes
de 5e
Chimie

C-2
Chapitre 1 – Changements d’état – Matière, corps purs et mélanges
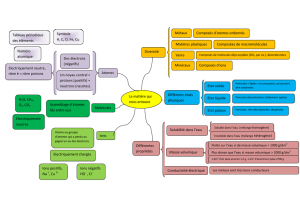
1.1. La matière
En chimie, le mot « corps » désigne le matériau dont est
constitué un objet.
Ex. de corps chimiques : ______________________________________.
Chaque corps a une masse et occupe un volume.
1.2. Les corps purs
Un corps pur est un corps qui n’est constitué que d’un seul
type de substance. Il possède des propriétés
caractéristiques, bien définies et invariables.
Ex. de corps purs : _______________________________________.
1.3. Les états de la matière
La matière peut se présenter sous trois états différents :
solide, liquide ou gazeux.
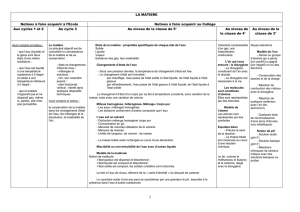
1.4. Propriétés des états
Complète chacune des cases ci-dessous à l’aide des mots « fixe »
(si la grandeur examinée ne peut pas être changée)
,
ou « variable »
(si la grandeur examinée peut être changée)
.
Solide Liquide Gaz
Forme
Volume
1.5. Changements d’état
Dans quels états l’eau se trouve-t-elle dans le paysage ci-dessous ?

C-3
a. Influence de la température :
Activité : Complète le texte suivant :
On sait que,
- si la glace est chauffée, elle _______________.
- si l’eau est chauffée fortement, elle _______________.
(petite aide : http://leconjugueur.lefigaro.fr/conjugaison/verbe/bouillir.html)
Par ailleurs,
- si la vapeur d’eau est refroidie, elle _______________.
- si l’eau est refroidie, elle _______________.
Expérience : Du diiode est chauffé dans une flamme. Refroidissons-le ensuite.
Observations : ___________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
On appelle
• sublimation le passage direct de l’état solide à l’état gazeux,
• resublimation le passage direct de l’état gazeux à l’état solide
b. Influence de la pression :
Observation : Les bonbonnes « Campinggaz » contiennent un liquide. Mais en ouvrant le robinet, un gaz
s’échappe.
Expérience : Un ballon rempli d’eau est mis sous vide à l’aide d’une pompe à vide.
Observation : L’eau ______________________ à température ambiante.
Conclusion. : Les états de la matière sont également influencés par _____________________________.

C-4
Activité : compléter le diagramme des états d’agrégation :
Remarques : On distingue entre
- Evaporation qui désigne le passage lent de l’état liquide à l’état gazeux et qui se fait à toute t°
- Ebullition qui désigne le passage rapide de l’état liquide à l’état gazeux et qui se fait à une t°
constante qu’on appelle température d’ébullition .
Exercice C1 : * Complète le texte suivant !
Lors d’une augmentation de la __________________________, la plupart des corps solides passent à l’état
_________________ : ce changement d’état s’appelle __________________________. Certains corps
solides passent directement à l’état _______________________ dans ces conditions : ce changement d’état
s’appelle ___________________________.
Lors d’une _______________________________ de la pression, un corps à l’état _____________________
devient en général d’abord _________________________ (ce changement d’état s’appelle condensation), et
puis _____________________ (ce changement d’état s’appelle __________________________).

C-5
1.6. Le modèle corpusculaire
La matière est formée de particules fondamentales de très petite taille (10
-8
m), représentées par des boules.
Caractéristiques de l’état solide
______________________________________________________________
______________________________________________________________
______________________________________________________________
Concl. :
forme et volume déterminés
durs
Fusion
Les particules sont soumises à une agitation thermique de plus en plus
forte, ce qui fait que le réseau est détruit.
Caractéristiques de l’état liquide
________________________________________________________
________________________________________________________
________________________________________________________
________________________________________________________
Concl : forme variable, mais volume déterminé
Ebullition
L’agitation thermique est devenue assez grande pour que les particules
puissent quitter le liquide.
Caractéristiques de l’état gazeux
________________________________________________________
________________________________________________________
________________________________________________________
________________________________________________________
Concl :
Masse volumique faible
Les gaz peuvent être comprimés
Exercice C2 : *
Schématise les situations suivantes à l’aide du modèle corpusculaire !
a. Le sel est un solide.
b. Des glaçons fondent.
c. Du dioxyde de carbone solide sublime.
d. Dans l’atmosphère, la vapeur d’eau condense en gouttelettes d’eau.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
1
/
65
100%