DOC

1
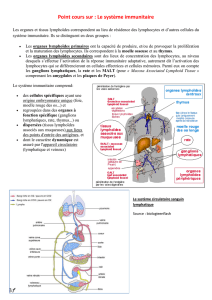
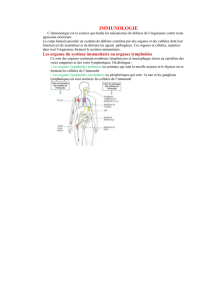
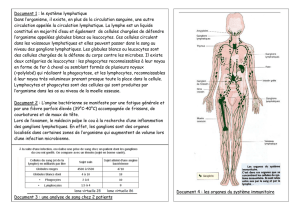
TISSU ET ORGANES LYMPHOIDES
Le tissu lymphoïde est réparti de manière diffuse dans l’organisme ou alors constitue des organes anatomiquement définis. Il
assure la production, la différenciation et l’évolution des cellules lymphoïdes. Le tissu et les organes lymphoïdes jouent un
rôle primordial dans le déroulement des réactions immunitaires spécifiques.
Le tissu lymphoïde comprend :
La moelle osseuse hématopoïétique : lieu de production des cellules lymphoïdes (cellules souches) et chez les Mammifères,
lieu de différenciation des lymphocytes B.
Les organes lymphoïdes primaires (centraux) :
Le thymus : lieu de différenciation des lymphocytes T (thymodépendants) chez les Mammifères et les Oiseaux. La bourse de
Fabricius : lieu de différenciation des lymphocytes B (burso-dépendants) chez les Oiseaux. Annexée au cloaque chez les
Oiseaux et dont il ne semble pas y avoir d’équivalent chez les Mammifères. Les organes lymphoïdes primaires sont très
développés à la naissance puis involuent plus ou moins entièrement dans la première partie de l’existence. Ils sont
responsables de la maturation fonctionnelle des lymphocytes en cellules immunocompétentes.
Les organes et tissus lymphoïdes secondaires (périphériques) :
- les nœuds lymphatiques, situés sur la circulation lymphatique
- la rate, située sur la circulation sanguine
- les ganglions hémolymphatiques, connus chez le Rat
- les organes ou tissu lymphoïde associés aux muqueuses :
* digestives (G.A.L.T. pour Gut Associated Lymphoid Tissue) : tissu lymphoïde associé à l’intestin :
- les tonsilles (amygdales)
- le tissu lymphoïde diffus de la muqueuse gastrique et intestinale
- les plaques de Peyer (intestin grêle)
* respiratoires (B.A.L.T. pour Bronchus Associated Lymphoid Tissue) : tissu lymphoïde situé à la périphérie des voies
respiratoires extra et intra-pulmonaires
Ce sont des organes et tissus peu présents à la naissance mais qui se développent sous l’effet des stimulations antigéniques
successives auxquelles est soumis l’individu. Ils persistent durant toute la vie mais subissent une régression chez les sujets
âgés.
Ils représentent les lieux de localisation principale des lymphocytes B et T ; lieux de leur transformation et du développement
des réactions immunitaires spécifiques.

2
DIFFERENCIATION ET CARACTERISTIQUES PHYSIOLOGIQUES DES CELLULES
LYMPHOÏDES CHEZ LES MAMMIFERES
In « Veterinary Immunology, I.R.Tizard, 6th edition, 2000 »

3
LES ORGANES LYMPHOÏDES PRIMAIRES
Les organes lymphoïdes primaires ou centraux sont des organes de structure lympho-épithéliale. Ils associent un
réticulum de cellules épithéliales (d’origine endodermique) à des cellules libres (lymphocytes et macrophages).
Très développés à la naissance, leur régression est précoce au cours de la vie. Ils permettent la maturation
fonctionnelle et l’acquisition de l’immunocompétence des lymphocytes issus de la moelle osseuse. Ils comprennent :
- le thymus, responsable de la production des lymphocytes T chez les Mammifères et les Oiseaux.
- la bourse de Fabricius, responsable chez les Oiseaux de la production des lymphocytes B et que nous
n’envisagerons pas ici. Chez les Mammifères qui ne possèdent pas de bourse de Fabricius, les lymphocytes B
mûrissent directement dans la moelle osseuse hématopoïétique (et au moins dans certaines espèces comme les
Ovins, dans les Plaques de Peyer intestinales).
LE THYMUS
Organe lymphoïde de structure lymphoépithéliale situé presque en totalité dans le médiastin antérieur chez
les Mammifères. Il se différencie très précocement chez l’embryon et est très développé à la naissance et chez le
jeune. Il régresse à la puberté et ne persiste chez l’adulte que sous la forme de vestiges atrophiés, dispersés dans le
tissu conjonctivo-adipeux médiastinal.
Le thymus est le siège de la multiplication et de la maturation des lymphocytes T ou lymphocytes thymodépendants
qui seront responsables de l’immunité à médiation cellulaire.
I. DEVELOPPEMENT EMBRYOLOGIQUE
Le mode de développement du thymus permet de comprendre la nature lymphoépithéliale du parenchyme
thymique.
Organogenèse
Le thymus est issu d’une ébauche provenant des 3e et 4e poches endodermiques pharyngiennes, c’est-à-dire de
structures épithéliales. Ces poches forment de part et d’autre deux ébauches thymiques symétriques. Un
épaississement antérieur s’individualise pour constituer les ébauches des glandes parathyroïdes postérieures. La
poche constituant l’ébauche thymique se referme et isole cette ébauche de l’épithélium endodermique. Le canal
thymique central s’obstrue progressivement en même temps que des cloisons conjonctives se développent dans les
ébauches pour constituer les lobules thymiques.
Les ébauches parathyroïdiennes et thymiques se séparent et migrent vers leur localisation définitive :
- les ébauches parathyroïdiennes postérieures rejoignent la partie postérieure des glandes thyroïdes.
- les ébauches thymiques migrent en direction du médiastin antérieur et se rejoignent.
Après la naissance, le thymus est entièrement situé dans le médiastin antérieur.

4
Histogenèse
L’ébauche thymique est initialement une structure purement épithéliale qui s’enfonce dans le mésenchyme.
L’ébauche se divise progressivement en lobules séparés par des cloisons d’origine mésenchymateuse. Cette
lobulation s’accompagne de la prolifération du tissu épithélial et de la pénétration des vaisseaux sanguins. La
vascularisation des lobules est rapidement suivie d’une diapédèse de lymphocytes circulants qui colonisent le
parenchyme du lobule et s’y multiplient.
Les lymphocytes qui colonisent le thymus sont des lymphocytes non immunocompétents, produits par les tissus
hématopoïétiques. Il s’agit de cellules pré-T, déjà engagées dans la lignée cellulaire responsable de l’immunité à
médiation cellulaire.
La colonisation spécifique du thymus par des cellules pré-T dépendrait de la présence de récepteurs particuliers sur
les cellules endothéliales des capillaires et des veinules post-capillaires thymiques.

5
Les cellules pré-T se localisent en périphérie des lobules où elles se transforment en cellules d’aspect immature, les
thymoblastes, qui se multiplient rapidement, donnant naissance à de très nombreux lymphocytes T ou thymocytes.
Ceux-ci gagnent progressivement la région centrale du lobule, où ils sont moins nombreux ; il se constitue ainsi dans
chaque lobule une corticale et une médullaire. Les thymocytes mûrs quittent le thymus par diapédèse et rejoignent
la circulation sanguine au niveau des veinules post-capillaires.
II. HISTOLOGIE TOPOGRAPHIQUE
Le thymus est constitué de deux ébauches qui s’accolent, fusionnent partiellement et se divisent en lobules : c’est
donc un organe bilobé et lobulé.
II.1.Charpente conjonctive et lobules thymiques
Le thymus est limité par une fine capsule conjonctive d’où émanent des cloisons conjonctives principales qui
divisent l’organe en lobules. Certains lobules, incomplètement séparés, apparaissent partiellement fusionnés. De
courtes cloisons secondaires se forment à la périphérie des lobules.
Au faible grossissement, chaque lobule est constitué d’une corticale périphérique très dense et basophile, d’une
médullaire moins dense, plus éosinophile. Dans la médullaire apparaissent de petites formations sphériques
éosinophiles : les corpuscules thymiques (anciennement corpuscules de Hassal).
II.2.Vascularisation et innervation
Des artères provenant des cloisons pénètrent dans les lobules et se ramifient en artérioles qui cheminent à la
jonction cortico-médullaire. Elles donnent naissance à un réseau de capillaires qui sont drainés par des veinules
post-capillaires, surtout nombreuses à la jonction cortico-médullaire, puis par des veines qui rejoignent les cloisons
conjonctives.
Le parenchyme thymique est dépourvu de veines lymphatiques. On observe quelques fentes lymphatiques dans les
cloisons drainées vers les nœuds lymphatiques régionaux. Il n’y a pas de vaisseaux lymphatiques afférents au
thymus.
Un réseau de fibres nerveuses provenant du nerf vague et du système sympathique accompagne les vaisseaux
sanguins et joue un rôle essentiellement vasomoteur.
Le thymus est donc un organe lymphoïde lobulé. Chaque lobule est constitué d’une corticale et d’une
médullaire ; il ne présente pas de follicules comparables à ceux des organes lymphoïdes secondaires, ni de
vaisseaux lymphatiques afférents.
III. STRUCTURE HISTOLOGIQUE
Le cortex et la médullaire thymiques sont principalement composés d’un réticulum épithélial et de thymocytes.
Les cellules réticulaires épithéliales (le caractère épithélial de ces cellules est à souligner car normalement les
cellules réticulaires sont d’origine mésenchymateuse) sont unies les unes aux autres par les extrémités de leurs
prolongements cytoplasmiques. Elles dessinent de larges mailles et forment un revêtement continu tout le long des
cloisons conjonctives, en s’appuyant sur une lame basale. Elles ont un cytoplasme éosinophile moyennement
abondant, un noyau ovoïde clair et nucléolé et de longs prolongements cytoplasmiques non visibles en microscopie
photonique.
Elles sont plus nombreuses dans la médullaire où elles constituent un réseau à mailles plus étroites que dans la
corticale (laissant une place plus faible aux cellules lymphoïdes). Dans la médullaire, elles se regroupent en
formations concentriques évoquant des bulbes d’oignons, les corpuscules thymiques ou corpuscules de Hassall.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%