7 – Chimie douce

1
7 – Chimie douce
Polymérisation inorganique, Synthèse d’oxydes

2
7 – Chimie Douce
Polymérisation inorganique, Synthèse d’oxydes
I.Réactions de combustion
1. Chimie des feux d’artifice
2.1. Oxydo-réduction
2.2. Incandescence (corps noir)
2.3. Emission de flamme (luminescence atomique)
2. Chimie de la propulsion
3. Synthèse d’oxydes par combustion
II. Chimie douce
1. Chimie modificative
1.1. Solides de basse dimensionnalité
1.2. Applications de la chimie d’intercalation
2. Chimie Sol-Gel
2.1. Matériaux bio-inspirés
2.2. Polymérisation inorganique
2.2.1. Dissolution d’un sel dans l’eau
2.2.2. Modèle des charges partielles
2.2.3. Diagramme Charge-pH
2.2.4. Condensation en solution aqueuse
2.2.5. Condensation en milieu non aqueux

3
La chimie du solide est une chimie des hautes températures (≥1500ºC)
Oxydes
Verres, Céramiques, Monocristaux
Semi-conducteurs
Ex : MgO + Al2O3→MgAl2O4
Plusieurs jours à 1500ºC
Silicium : réduction de SiO2dans un
four à arc, purification, tirage d’un
lingot
Réactions lentes aux interfaces
entre solides

4
!Transformation à basse température d’un matériau
classique pour en modifier les propriétés physiques
"Greffage
"Echange ionique
"Intercalation
!Procédé Sol-Gel : Polymérisation inorganique à partir de
précurseurs moléculaires liquides
Le gel obtenu se densifie à basse température,
permettant l’élaboration de verres ou de céramiques
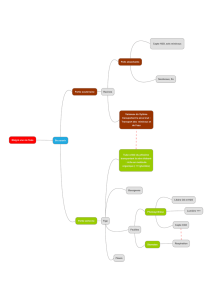
Alternatives :
I. Réactions de combustion
Synthèse d’oxydes
II. Chimie douce

5
Le triangle du feu :
Toute combustion a besoin d’énergie pour atteindre son point d'ignition
I. Réactions de combustion
Energie
Combustible Comburant
C, fuel
S
métaux
C, fuel
S
métaux
O
2
Chlorates
Nitrates
O
2
Chlorates
Nitrates
Chaleur
Etincelle
Frottement
Chaleur
Etincelle
Frottement
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
1
/
61
100%