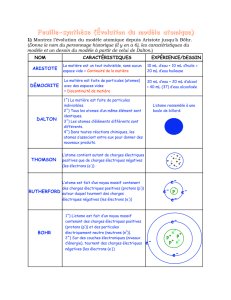
Des modèles successifs de l`atome

Des modèles successifs de l’atome
Les philosophes de la Grèce antique comme Leucippe et Démocrite (460-370 av JC) furent les
premiers à supposer l’existence de particules invisibles et indivisibles, les atomes (‘atome’ vient du
grec ‘atomos’ qui signifie « qu’on ne peut diviser »). Cette idée ne reposait pas sur des faits
expérimentaux ni sur des observations , mais sur une intuition.
Aristote (384-322 av JC) affirme que la matière est constituée de 4 éléments : le feu, la terre, l’air et
l’eau ; l’idée de l’atome est abandonnée . Les idées d’Aristote seront employées pendant plus de 20
siècles… avant que l’on s’aperçoive qu’elles étaient fausses !
Lorsqu’en 1803 le chimiste britannique John Dalton (1766-1844) étudia les réactions chimiques, il
fonda sa théorie sur l’existence de petites particules sphériques et insécables, les atomes . C’est le père
incontesté de la théorie atomique.
Il mit en évidence qu’au cours d’une réaction chimique, les atomes se combinent pour former de
nouveaux composés. Chaque type d’atome, représenté par un symbole (C pour le carbone, H pour
l’hydrogène, O pour l’oxygène ..), a des propriétés particulières et peut se combiner avec des atomes
différents.
Reconsidérant les travaux de Dalton, le chimiste italien Amadéo Avogadro (1776-1856) établit, en
1811, la distinction entre atome et molécule : une molécule est constituée d’un ou plusieurs atomes.
Ce ne fut qu’à la fin du XIXe siècle que la notion d’atome indivisible fut mise en doute.
En 1833, l’anglais Faraday (1791-1867) explique la conduction dans les électrolytes par la notion
d’ions.
En 1869, le savant russe Mendeleïev (1834-1907), étudiant les propriétés chimiques communes de
certains types d’atomes, fut le premier à proposer une classification.
En 1881, le physicien anglais Joseph Thomson (1856-1940) démontra que ces petits grains de
matière que existaient lors des expériences dur les décharges électriques dans les gaz étaient identiques
quel que soit le corps étudié. Son compatriote Stoney baptisa ces particules électrons en 1891.
La découverte de l’existence des électrons conduisit Thomson à proposer un nouveau modèle de
l’atome : les électrons, chargés négativement, et des particules plus massives, de charge positive, se
trouvent confinés dans une sphère de rayon égal à 10-10m.
En 1911, Ernest Rutherford (1871-1937), voulant étudier la disposition spatiale à l’intérieur de
l’atome, fit une découverte capitale ; En bombardant une mince feuille d d’or avec des particules
neutres, il observa que la plupart des particules traversaient la feuille sans être déviées, alors que
certaines étaient cependant détournées.
Une théorie révolutionnaire apparut alors : l’atome est constitué principalement de vide. Il est formé
d’un noyau massif, chargé positivement, autour duquel gravitent les électrons. De nombreuses
recherches affinèrent par la suite ce modèle.
La structure du nuage électronique fut étudiée en physique quantique. En, 1913, une disposition en
« couches » fut proposée par le physicien Danois Niels Bohr (1885-1962).
Actuellement, on admet qu’il est impossible d ‘associer à l’électron une trajectoire bien définie. Tout
ce que l’on peut dire, c’est que la probabilité de trouver un électron en un point déterminé de l’espace
est plus ou moins grande.
En 1924 la mécanique ondulatoire développée par De Broglie ‘(1892-1987) permet de calculer la
probabilité de présence des électrons autour du noyau. On parle de cortège électronique. Ce modèle est
appelé l’atome probabiliste.
1
/
1
100%