chapitre 15 : additions nucleophiles

!"#$%&'()*+),)-..%&%/01)02345/$"%4(1) ) ) ) 6!78)
)
*)
!9-68:;<)*+),)-==8:8>?7)?@!A<>698A<7)
)
=>!@B<?:)*),)6;<7<?:-:8>?)=<7)>;C-?>B-C?<78<?7)B8D:<7)
)
E/'F24()G505'#4(),))
)
-211%)#$$(451)H)'5#3&%I1).()C'%G0#'.)J)3#').53/2K('&1)$#')L%3&/')C'%G0#'.M)$'%N)?/O(4)*P*Q)$/2')
H) $/2') 4#) .53/2K('&() .2) '5#3&%I) 5$/0RF() .() C'%G0#'.M) 3() S2%) #) $('F%1) '53(FF(0&) .() I#%'()
#O/0.#FF(0&)$'/G'(11(')4#)3"%F%()/'G#0%S2()JT)
A(1)/'G#0/F#G051%(01)I/0&)$#'&%().()4#)I#F%44().(1)/'G#0/F5,%S2(1)UF/45324(1)$/115.#0&)20()
4%#%1/0)!VB5WT))
>O&(0&%/0),)
A(1)/'G#0/F#G051%(01)F%N&(1)1/0&)/O&(021)(0)I#%1#0&)'5#G%')20).5'%K5)"#4/G505);D)12')4()F#G051%2F)F5,%S2()BGU1W)
.#01)20)1/4K#0&)#$$'/$'%5)U20)5&"('/NR.();V>V;XW)(&).(1)3/0.%&%/01)$#'&%324%Y'(1)UK/%'):6WT)
<S2#&%/0)O%4#0),))
)
Insertion)du)magnésium)d’autant)plus)facile)que)la)liaison)C-X)est)polarisable.)
)
?/F(034#&2'(),)H)"#4/G502'().X#4ZR4F#G051%2F)J)
)
!9[BG8),)8/.2'().()F5&"R4F#G051%2F)))))6"BG\'),))
)
),)!"4/'2'().()$'/$VQVR4F#G051%2F)))<&BG\'),))
)
=>!@B<?:)Q),)<A<!:;>?<C-:8L8:<)=<)]@<A]@<7)<A<B<?:7)
)
=>!@B<?:)[),)8?:<;<:)=<7)>;C-?>B<:-AA8]@<7)<?)7^?:9<7<),)!;<-:8>?)=<)A8-87>?)!V!)
)
R X
Dérivé halogéné
R Mg X
Organomagnésien mixte
+Mg(s)
Magnésium
solide
Etheroxyde
"mixte" car de part et d'autre du Mg : R et X
MgCl
<45F(0&)U_W
)
9)
)
)
)
)
)
)
)
9()
A%)U`MPaW)
\()
)
\)
!
)UQMbW)
?)
>)
E
)UcM`W)
?()
?#)
BG
)U*M[W)
)
-4)
7%)
6)
7)
!4)
U[MQW)
-')
d)
!#)
)
C#)
C()
-1)
7()
\'
)U[M`W)
d')
;O)
7')
)
80)
70)
7O)
:()
8
)UQMeW)
D()
R Mg X
Alkyle
Magnésium
Halogène :
Cl, Br, I

!"#$%&'()*+),)-..%&%/01)02345/$"%4(1) ) ) ) 6!78)
)
Q)
=>!@B<?:)c),)<!9<AA<)=<)6d-),)6>78:8>?)=<7)>;C-?>B-C?<78<?7)
)
)
=>!@B<?:)+),)7^?:9<7<)=X>;C-?>B-C?<78<?7)-!<:^A<?8]@<7)
A#) 1R0&"Y1() 212(44() .(1) /'G#0/F#G051%(01) 0() F#'3"() $#1) #K(3) 4(1)
"#4/G50/#43R0()U)f)4%#%1/0)&'%$4()!!)$2%1)20)#&/F().X"#4/GY0(W)T)84)(1&)3($(0.#0&)
$/11%O4() .X2&%4%1(') 4(1) $'/$'%5&51) O#1%S2(1) .(1) /'G#0/F#G051%(01) #I%0) .()
1R0&"5&%1(').(1)/'G#0/F#G051%(01)#35&R450%S2(1),))
)
)
) ) )))))))#43R0()K'#%))))))))))))))))))))))))))))) ) ))
)
)
)
AX5&"#0()I/'F5)(1&)20)G#g)S2%)1X53"#$$().()4#)1/42&%/0M)(&)4X/'G#0/F#G051%(0)#35&R450%S2()#%01%)$'5$#'5)$(2&)#4/'1)h&'().%'(3&(F(0&)
2&%4%15)(0)1R0&"Y1(T))
)
=>!@B<?:)b),)6>@;]@>8)E-8;<)AX9^=;>A^7<)<?)B8A8<@)-!8=<)i))
-)4X%112().()4X-?M)/0)/O&%(0&)20)#43//4#&(M)O#1()I/'&().#01)4X(#2),)4X(#2)(1&)20)#3%.()12II%1#FF(0&)I/'&)
$/2')/O&(0%')4X#43//4)3/''(1$/0.#0&T)
-4/'1)
$/2'S2/%)1()$4#3(')(0)F%4%(2)#3%.()
$/2')4X"R.'/4R1()U$#')(N(F$4()(0)2&%4%1#0&)20()1/42&%/0).()
?9c
jM) !4VU#SWW)i) <0) F%4%(2) O#1%S2() /2) 0(2&'(M) BGU>9WQU1W) $'53%$%&(M) 3() S2%) 3/F$4%S2() 4(1) $"#1(1)
24&5'%(2'(1).()&'#%&(F(0&).2)O'2&)'5#3&%/00(4)$/2')/O&(0%')4()$'/.2%&)à)/0)1()$4#3()(0)F%4%(2)#3%.()
$/2')5K%&(')4#)$'53%$%&#&%/0)UK/%')3"T*b),)6'53%$%&#&%/0WT)
)
)
)
)
)
Uj)BGDjW)
Amine)
Alcool)
Eau)
Acide)carboxylique)
pKA
RO-ROH
HO-H2O
Alcoolate
18
14
Alcyne)terminal)
Uj)BGDjW)
dk)f))

!"#$%&'()*+),)-..%&%/01)02345/$"%4(1) ) ) ) 6!78)
)
[)
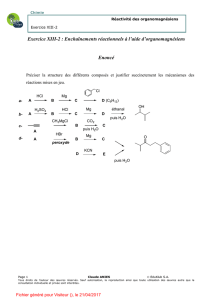
=>!@B<?:)e),)6>@;)-AA<;)6A@7)A>8?),)7:<;<>7<A<!:8L8:<)=<)AX-?)=X@?)>;C-?>B-C?<78<?)7@;)@?)!-;\>?^A<T)
AX#..%&%/0).X20)/'G#0/F#G051%(0)12')20).5'%K5)3#'O/0R45M).()G5/F5&'%()4/3#4(F(0&)$4#0(M)(1&)0/0)1&5'5/154(3&%K()
1%)4(1).(2N)I#3(1)
.2)3#'O/0R4()1/0&)5S2%K#4(0&(1
T))
Exemple):))
)
B#%1) 1%) 4(1) .(2N) I#3(1) 0() 1/0&) $421) 5S2%K#4(0&(1M) 3X(1&) l) .%'() 1%) 4X20() (1&) $421) (03/FO'5() S2() 4X#2&'(M) /0) /O1('K('#) 20()
1&5'5/154(3&%K%&5).()4X#..%&%/0T)AX#&&#S2().()4X/'G#0/F#G051%(0) 1() I('#)$'5I5'(0&%(44(F(0&)12')4#)I#3()4#)F/%01) (03/FO'5()$/2')
4%F%&(')4#)GY0()1&5'%S2(T)!X(1&)4()3#1)$#')(N(F$4()1%)20).(1)#&/F(1).()3#'O/0()(0)α)(1&)#1RF5&'%S2()U3I)(N(F$4()G#23"()3%V.(11/21WM)
/2)O%(0)1%)4()G'/2$()3#'O/0R4()(1&)%03421).#01)20)3R34()./0&)4(1).(2N)I#3(1)1/0&).%II5'(FF(0&)(03/FO'5(1)U3I)(N(F$4().'/%&(WT)
)
)
)
=>!@B<?:)a),)!-;\>CA-!<)
)
)
=>!@B<?:)P),)\8A-?)=<7);<-!:8>?7)-)6-;:8;)=X9-A>C<?>-A!-?<7);D)<:)=X>;C-?>B-C?<78<?7)B8D:<7);BCD)
)
)
)
) )
tBu
O
H
CH3
Ph 1) CH3MgBr, Et2O
2) H2O, H+tBu
H
CH3
Ph
H3COH
tBu
H
CH3
Ph
CH3
HO
Majoritaire
O
Camphre
1) CH3MgBr, Et2O
2) H2O, H+
OH
OH +
Majoritaire
base
forte
alcène
SN
β-E2 SN
halogénoalcane
organomagnésien
mixte ROH
R' R''
1) , Et2O
2) H2O, H+
1) CO2(s), Et2O
2) H2O, H+
ROH
O
alcool
primaire,
secondaire
ou tertiaire
acide
carboxylique
AN2
R' R''
O
aldéhyde ou cétone

!"#$%&'()*+),)-..%&%/01)02345/$"%4(1) ) ) ) 6!78)
)
c)
=>!@B<?:)*`),);<:;>7^?:9<7<)
E#%'() 4#) H)'5&'/1R0&"Y1()J) .X20() F/45324() <) 3/01%1&() l) %F#G%0(') l) $#'&%') .() S2(44(1) F/45324(1) $421) 1%F$4(1) /0) $(2&) /O&(0%') 4#)
F/45324()<T))
>0)53'%&)20)13"5F#).()'5&'/1R0&"Y1()l)4X#%.().()
I4Y3"(1)'5&'/1R0&"5&%S2(1
)U⇒)M)'($'51(0�&)4X%0K('1().()I4Y3"(1).()'5#3&%/0).()
1R0&"Y1(T)!()1RFO/4()1()4%&)H)(1&)/O&(02)l)$#'&%').()JT)
)
-$$4%3#&%/0)
,)6'/$/1(')20()1R0&"Y1().2)O2�VQV/4)l)$#'&%').()'5#3&%I1)0()$/115.#0&)S2()Q)#&/F(1).()3#'O/0()#2)F#N%F2FT)
)
)
)
)
)
)
)
)
)
)
84)(N%1&()1/2K(0&)$421%(2'1)K/%(1).()1R0&"Y1(1)$/2')20()F/45324()./005(T)<0)$'#&%S2(M)/0)3"/%1%'#)3(44()S2%)$/11Y.()4()
F(%44(2')'(0.(F(0&M)/2)4#)$421)#%15()l)F(&&'()(0)m2K'(T)
Exemple)1):))
)
Exemple)2):))
)
)
A B C D E
Synthèse de la
molécule-cible E :
E D C B A
Rétrosynthèse de E :
BG!4)
1
/
4
100%