Transport O2 et CO2 : Cours sur le transport des gaz sanguins

Typeurs : Mickael Aubignat, Justine Giunta / Correctrice : Léa Spagnol
Transport O2 et CO2
« Comment les gaz sont transportés entre les alvéoles et les tissus »
I. Transport de l'O2 dans le sang.
- L'oxygène est transportée:
o dans le plasma: sous forme dissoute
o dans les hématies: sous forme dissoute et essentiellement lié à l'Hb
I.1. Oxygène dissous.
- Dépend de la Loi de henry : Cx = α x Px
- Le contenu de gaz dissous Cx dans un liquide est déterminé par :
o la pression partielle de gaz : Px
o son coefficient de solubilité : alpha, qui dépend du gaz, du solvant et de la T (si T ↑ α ↓). Il est
exprimé en ml de gaz/ 100 ml sg / mmHg
- Dans le sang artériel : PaO2 = 100 mmHg = 13,3 kPa (pour passer des Kpa au mmHg on multiplie par
7.5)
- Le contenu en O2 dissous : Co2 = 0,3 ml d'O2 / 100 ml de sang artériel
- Si débit cardiaque = 5 L/min, apport de 15 ml d'O2 par minute c'est très peu par rapport aux besoins
(qui sont de 250 ml/min) donc c'est insuffisant pour oxygéner les tissus correctement, il faut un autre
moyen de transport : l'Hb des GR!
I.2. Oxygène combinée à l'Hb.
- RAPPEL : L'Hb est une protéine présente exclusivement dans les hématies et se lie de façon réversible
à l'O2
o Taux normaux : 13 à 17 g/dl chez l'homme ; 12 à 16 chez la femme.
o 4 chaines polypeptidiques (a1, a2, b1 et b2) = globine
o 4 groupements hèmes :
chaque gpt comporte un atome de Fe
chaque Fe peut se lier de façon réversible à une mol d'O2
o Différentes Hb normales :
adulte de type A (HbA1)
Hb fœtale : HbF remplacée au cour de la première année de vie par l'HbA
o Hb anormales :
mutation dans des chaînes polypeptidiques
ex : HBS → la drépanocytose
affinité diminuer pour l'O2
faiblement soluble et précipite à l'intérieur du GR.
oxydation du Fe 2+ (ferreux) en Fe 3+ (ferrique) : méthémoglobine (brune)
combinaison avec un gaz toxique : le CO
affinité 240 fois plus forte que O2
HbCO : carboxyhémoglobine (rouge vif)
<1% chez le non fumeur et 5 à 8% chez le fumeur
- Propriétés allostérique de l'Hb :
o la désoxyHb a une affinité faible pour l'O2
o la fixation d'une première molécule d'O2 change la configuration de la molécule d'Hb et facilite
la fixation de la seconde molécule
Typeurs : Mickael Aubignat, Justine Giunta / Correctrice : Léa Spagnol
o donc l'affinité de l'Hb pour l'O2 varie selon le degrés de saturation de la molécule
o De ce fait la relation entre la saturation de l'Hb et la PO2 n'est pas une relation linéaire (car
allostérie)
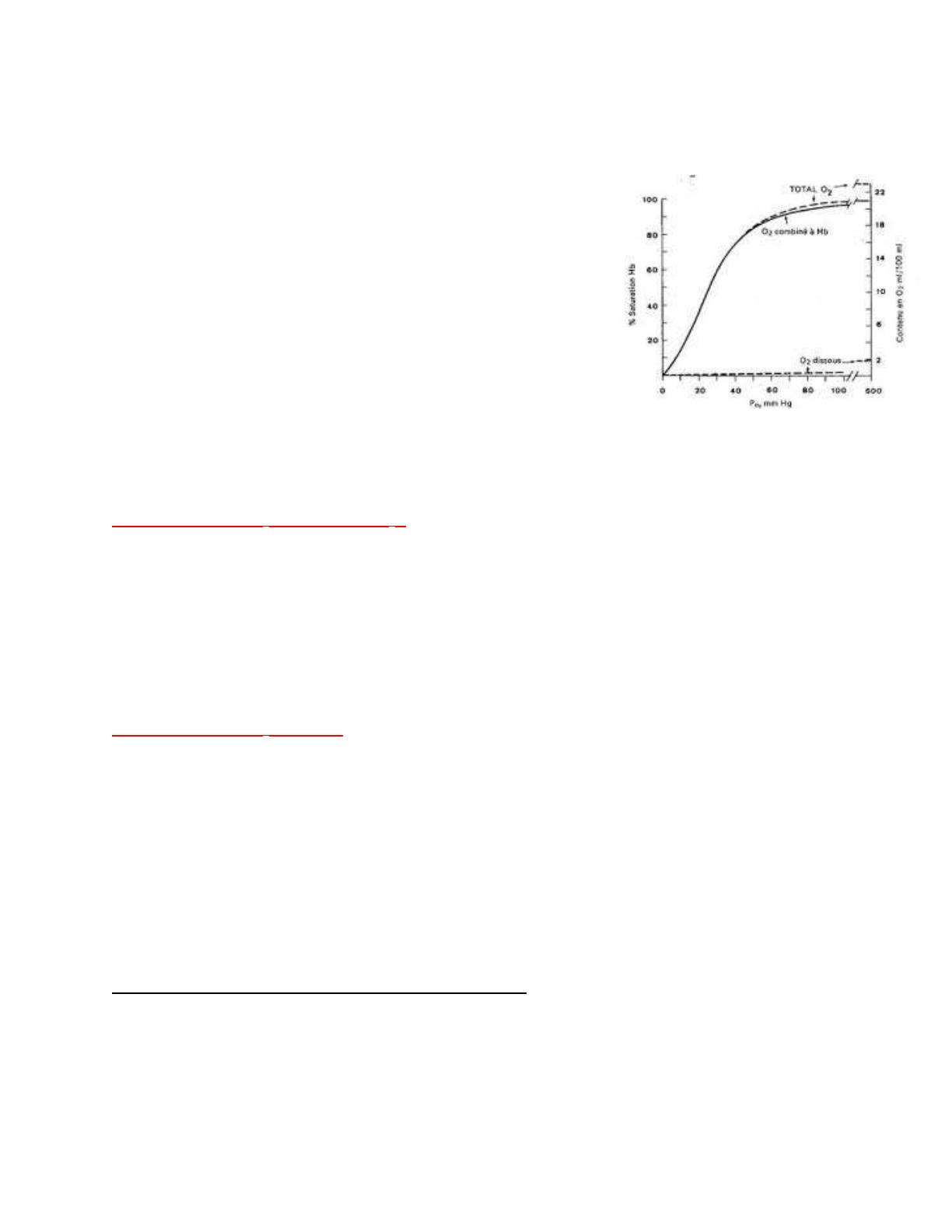
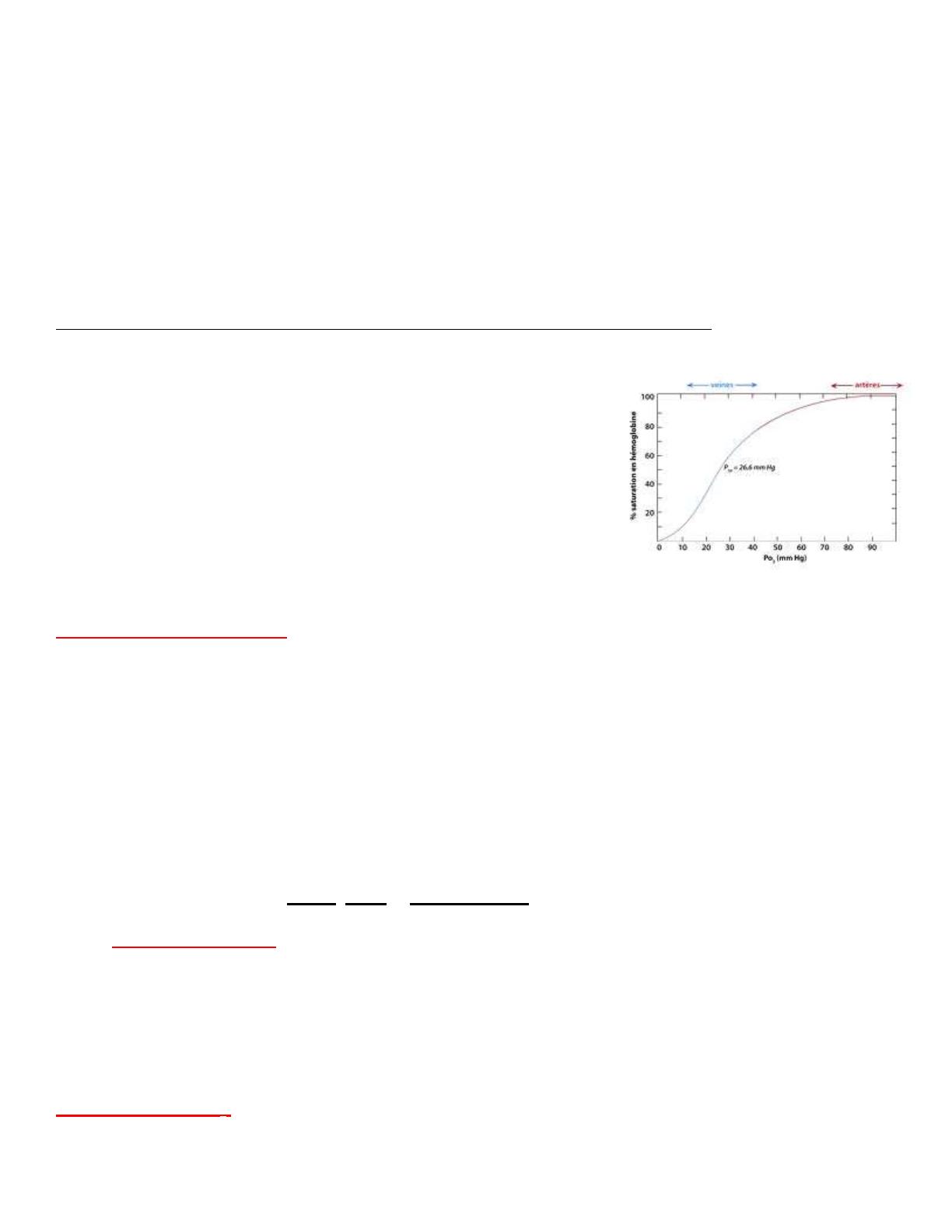
Courbe de dissociation de l'oxyhémoglobine :
- Contenu du sang en O2 = [O2 dissous + O2 combiné à l'Hb]
o Le contenu en O2 dissous (0,003 x PO2) est très faible
par rapport au contenu lié à l'Hb.
o Le contenu augmente rapidement jusqu'à une PO2 de
50 mmHg au delà la courbe devient beaucoup plus
plane.
- La capacité de transport en O2 :
o 1g d'Hb fixe au max 1,39 ml d'O2 = pouvoir
oxyphorique
o Pour une [Hb] de 15g/dl: 15 x 1,39 = 20,8 ml d'O2/ 100
ml
o La quantité max d'O2 pouvant se lier à l'Hb = la capacité
en O2
- La capacité effective en O2 = 1,39 x ([Hb] totale – [Hb] non fonctionnelle), en pratique = 1.34 x
[Hb]totale.
o Hb non fonctionnelle est la quantité en méthémoglobine ou carboxy (HbCO).
- La saturation en O2 de l'Hb est SO2 :
o SO2 = (contenu en O2 combiné à l'Hb) / (capacité totale en O2) (en %)
o Analogie avec 1 train : - la capacité en O2 = capacité de transport = nb de siège
- le contenue en O2 combiné avec Hb = nb de siège occupé
o Au fur et à mesure qu'on augmente la PO2, la SO2 augmente (cf schéma au dessus)
o SO2 fonctionnelle : SO2 / [100 - % Hb non fonctionnelle]
- contenu en O2 = (1,39 x [Hb] x SO2) + 0,003 x PO2
= lié à l'Hb = dissous
- La saturation en O2 de l'Hb :
o Dans le sang artérielle la pression partielle de l'O2 est de 100 mmHg, taux de saturation de
98%, ici la courbe de dissociation est plane (sang qui quitte les poumons).
o Dans le sang veineux la PaO2 est de 80mmHg avec un taux de saturation de 75%, la courbe est
plus raide (sang quittant les tissus).
o Quand la saturation change, sa couleur change, le sang artériel est rouge et le sang veineux est
plutôt bleu (noir). Cela explique la cyanose (coloration violacé des téguments : peau, muqueuses
…), elle est influencée par le taux d'Hb :
anémie : pâleur (baisse du CO2)
polyglobulie (Hb élevée) : cyanose (augmentation du CO2)
o Mesure de la saturation par spectrométrie : spectre dans les longueurs d'onde absorbé par oxyHb
et déoxyHb (plus foncée).
- Relation entre PO2, SO2 et le contenu en O2 (Co2) :
o le contenu en O2 dépend de [Hb] et de la PO2
o /!\ la saturation ne dépend pas de [Hb], ne dépend que de la PO2.
Anémie : Taux Hb ↓ et poumon normal, la concentration en O2 est ↓ mais la saturation est normale en
revanche le contenu en O2 est ↓. (on réduit le nb de wagon mais tjs 98% des passagers)
Polygobulie : Taux d'Hb ↑, la saturation est normale mais le contenu en O2 est ↑.
L'hypoxie stimule la sécrétion d'EPO en altitude donc on fabrique plus d'Hb, c'est pourquoi les entraînement de
sportif se font en altitude, le contenu en O2 sera élevé pour le même taux de saturation en O2.
Typeurs : Mickael Aubignat, Justine Giunta / Correctrice : Léa Spagnol
o Pour saturer l'Hb à 100% il faut ↑ la ventilation alvéolaire ou ↑ la fraction inspirée d'O2, mais
le taux de saturation dépend de la PO2 : à une PO2 de 100 (à l'équilibre), 98% de l'Hb sera
saturée quelque soit la quantité totale d'Hb.
o Une fois la saturation à 100%, pour avoir une PO2 dans le sang plus élevé, on doit augmenter la
fraction inspirer → O2 dissous augmente.
o Avec la même concentration fractionnaire de O2 (FI02 = 21%), on peut augmenter la pression
barométrique et cela augmente la pression partielle)
PO2 > 100 mmHg, l'↑ de PO2 n'affecte plus la SO2, toute l'Hb est saturée.
60 > PO2 > 100 mmHg, une ↓ de PO2, ↓ peu la quantité d'O2 transportée.
PO2 < 60 mmHg, une ↓ de PO2, ↓ beaucoup la quantité d'O2 transportée.
La forme sigmoïde de la courbe de dissociation de l'Hb a des avantages physiologiques :
- Si la PO2 ambiante ↑ et par conséquent la PO2 du sang artériel ↓
de 20 mmHg, la SO2 ne ↓ que très peu.
o Ceci traduit une plus grande affinité de l'Hb pour
l'O2, pour des valeurs de PO2 correspondant au sang
artériel.
- Pour des valeurs de PO2 correspondant au sang veineux → de
faibles baisses de PO2 entraînent de forte chute de SO2.
o Ceci traduit une baisse de l'affinité de l'Hb pour l'O2
pour des valeurs de PO2 correspondant au sang
veineux. => favorise la libération de l'O2 dans les
tissus
L'affinité de l'Hb pour l'O2 :
- P50 = PO2 nécessaire pour saturer l'Hb à 50% (normalement = à 27 mmHg), elle reflète l'affinité
globale pour l'O2.
- Une ↓ de l'affinité de l'Hb pour l'O2 :
o ↑ de la P50
acidose (augmentation de [H+]) effet Bohr : ex augmentation CO2 dans les tissus ou
accumulation d'autres types d'acide comme l'acide lactique pendant un effort.
↑ de CO2
↑ de la T°
o déplacement de la courbe de dissociation vers la droite
o ↑ du 2,3 DPG (produit par la glycolyse anaérobie dans les hématies) qui ↑ en hypoxie chronique
et ↑ si acidose mais ↓ dans les poches de sang conservées pour la transfusion.
- Le muscle à l'effort est chaud, acide et hypercapnique, ces conditions favorisent la libération d'O2 par
l'Hb car sont affinité diminue.
- Intoxication au CO : intoxication irréversible, on ↓ la capacité de l'Hb car l'O2 ne peut plus se
fixer, ainsi :
o la capacité en O2 ↓
o ↓ du contenu en O2 dans le sang artériel (CaO2)
o déplace la courbe de la dissociation vers la gauche: ↑ de l'affinité de l'Hb pour O2 et donc ↓ de la
libération d'O2 tissulaire, cela favorise l'hypoxie.
II. Transport du CO2.
- Le CO2 est transporté sous trois forme dans le sang :

Typeurs : Mickael Aubignat, Justine Giunta / Correctrice : Léa Spagnol
o CO2 dissous (5%)
o à l'état de bicarbonates (essentiellement à 90%)
o sous forme de composés carbaminés (5%)
- Le CO2 dissous est à la fois dans le plasma et le GR, il obéit à la loi de Henry mais le CO2 est 20 fois
plus soluble que l'O2 : rôle significatif dans le transport
- 10 % du dégagé au niveau pulmonaire est transportée sous forme dissoute et 60% sous forme de
bicarbonates et 30% en cabaminés.
II.1. CO2 à l'état bicarbonates.
- Il se combine avec l'H2O et forme l'acide
carbonique (H2CO3): réaction lente dans le
plasma mais rapide dans les GR grâce à
l'ahnydrase carbonique.
- Le bicarbonate (HCO3-) produit par la
dissociation de l'acide carbonique diffuse en
dehors du GR.
- l'H+ est retenu par la membrane des GR
- Pour maintenir la neutralité électrique de
Gibbs-Donnan, l'HCO3- est échangé contre
un Cl- → ce phénomène est appelé « effet
hamburger » ou déplacement des chlorures.
- Une partie de l'H+ libéré se lie à l'Hb, cette réaction a lieu car l'Hb réduite a une plus grande affinité
pour l'H+ (moins acide, accepte plus facilement un proton). La liaison de l'H+ à l'Hb diminue son
affinité pour l'O2 = effet bohr.
II.2. CO2 sous forme de composés carbaminés.
- Formés par la combinaison du CO2 avec les groupes amines terminaux des protéines dans le plasma
ou GR.
- Réaction rapide ne nécessitant pas d'enzyme.
- La protéine la plus abondante est la globine de l'Hb → carbaminohémoglobine
- l'Hb réduite fixe plus de CO2 sous forme carbamino que l'HbO2
- signification : la libération d'O2 par l'Hb dans les tissus facilite la captation de CO2 (= la capacité de
carbamination de l'Hb ↑ quand elle n'est plus lié à l'O2)
II.3. Relation entre le contenu en CO2 et la PCO2 : « courbe de dissociation du CO2 »
- La SaO2 modifie la courbe de dissociation du CO2 :
o sang artériel: ↑ de SaO2 → le sang peut capter moins de CO2
o sang veineux: ↓ de la SaO2 → à PCO2 égale, le sang peut capter plus de CO2
- La courbe de dissociation du CO2 dépend de la SaO2, c'est l'effet Haldane (=la désoxygénation du sang
↑sa capacité à transporter du CO2)
- Signification :
o dans les tissus: la désaturation de l'Hb favorise la captation du CO2
o dans le poumon: la fixation de l'O2 par l'Hb favorise le larguage du CO2
- Mécanisme :
o la liaison de l'H+ à l'Hb réduite (tissus ++ ) dans les GR facilite la captation du CO2 sous forme
de HCO3-
o l'Hb réduite (tissus) fixe plus de CO2 sous forme de carbamino-Hb que l'HbO2
Typeurs : Mickael Aubignat, Justine Giunta / Correctrice : Léa Spagnol
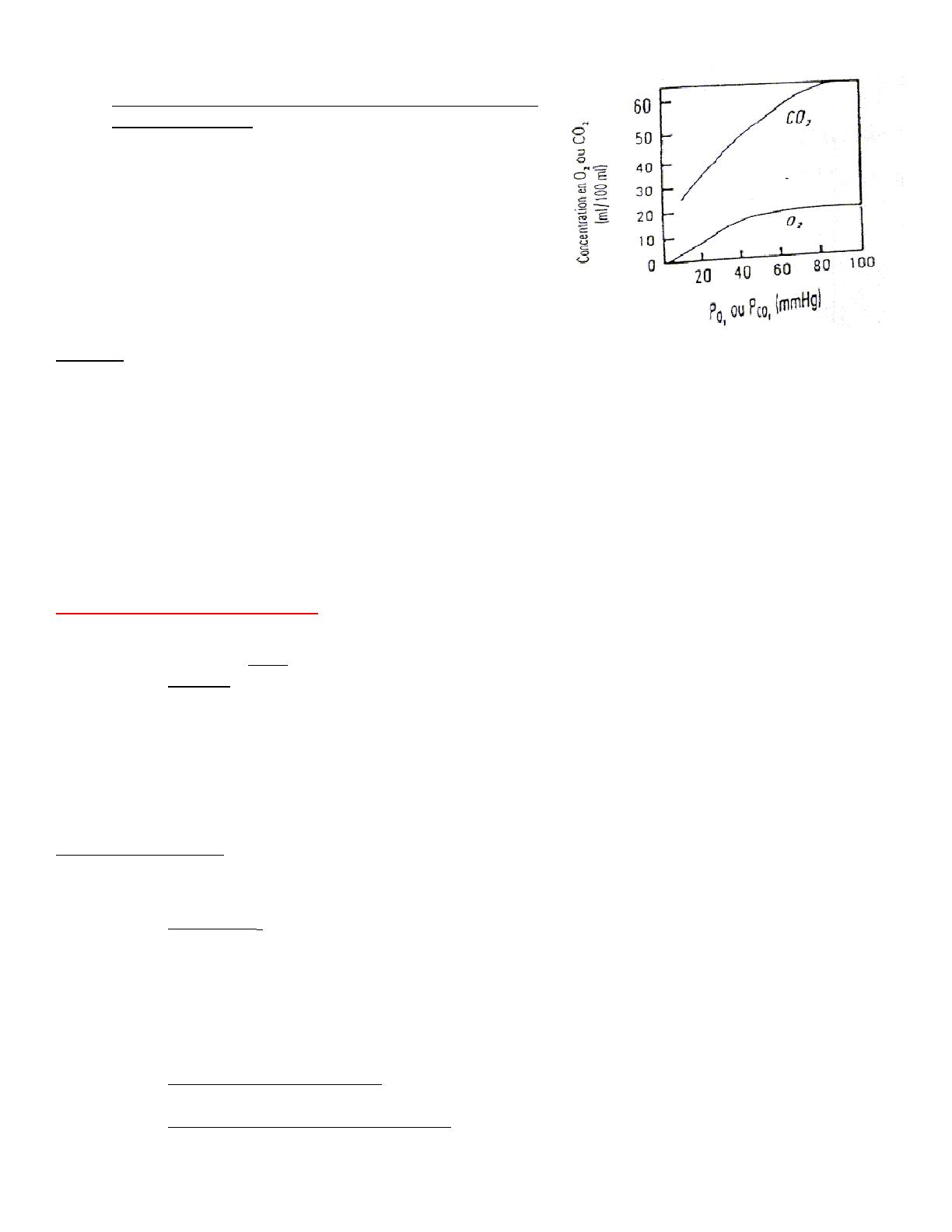
- Courbe de dissociation du CO2 est beaucoup plus pentue
que celle de L'O2 :
o contenu veineux en CO2 : 53 ml/100ml pour une
PCO2 de 45
o contenu artériel en CO2 : 48ml/100ml pour une
PCO2 de 40
o La forme pentue de la courbe permet de capter
(tissus) ou libérer (poumon) le CO2 pour une
variation de PCO2 relativement faible (5
mmHg).
RAPPEL : Relation entre transport de CO2 et équilibre acido-basique :
La réaction entre le CO2 et l'eau produit le système tampon le plus important de l'organisme : bicarbonates /
acide carbonique.
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3-
- les systèmes tampons résistent aux variations de pH des liquides organiques :
o en libérant des ions H+ (agissant comme des acides) quand augmentation du pH.
o en fixant les ions H+ (agissent comme des bases) quand baisse du pH
- La ventilation alvéolaire agit sur la PCO2 qui agit à son tour sur [H+]
o hyperventilation → augmentation de l'élimination de CO2 → alcalose respiratoire
o hypoventilation → baisse de l'élimination de CO2 → acidose respiratoire
III. Échanges gazeux sang-tissus.
- L'O2 et le CO2 sont échangés entre le sang capillaire et les tissus par simple diffusion.
o muscle au repos : distance de diffusion de 50 µm
o exercice : VD artérielle donc ↓ de la distance
o l'O2 qui sort du capillaire est consommé par le tissu → ↓ de PO2
o Dans les fibres musculaires la myoglobine agit comme une réservoir d'O2 et facilite sa diffusion
du capillaire vers la cellule
- La PO2 tissulaire est déterminée à tout moment par l'équilibre entre l'apport capillaire et
l'utilisation tissulaire.
A connaître par cœur :
- Hypoxie tissulaire = apport inadéquat d'O2 aux tissus
o Apport en O2 = Q x CaO2
o ↓ de la CaO2 (contenu artériel en O2)
si ↓ de la PaO2 car pathologie pulmonaire = hypoxie hypoxémique
hypoventilation alvéolaire
inadéquation V/Q (ex : shunt)
↓ de la capacité de transport de l'O2 :
anémie
intoxication via CO
o ↓ du débit sanguin tissulaire (baisse de Q) si choc hémodynamique, la perfusion diminue
(ichémie)
o ↓ de la capacité du tissu à utiliser l'O2 = hypoxie hystotoxique dans l'intoxication par le
cyanure (bloque le cytochrome oxydase)
1
/
5
100%