question d`actualité

8
La spectroscopie par résonance
magnétique nucléaire (RMN)
est une méthode non invasive
permettant d’étudier la nature
biochimique des tissus. Elle com-
plète l’imagerie anatomique,
morphologique, par une « image-
rie du métabolisme cellulaire».
Grâce aux récents développe-
ments des aimants, des antennes
et surtout des logiciels de post-
traitement, elle s’intègre de façon
plus large aux explorations stan-
dardisées de la prostate sur les
imageurs IRM actuels. L’apport
réel de la spectroscopie dans la
détection des cancers de la prosta-
te infra-cliniques reste toutefois à
démontrer pour une utilisation en
pratique courante.
L’imagerie par résonance magné-
tique découle des pro p r i é t é s
magnétiques de la matière. Les
noyaux hydrogènes situés dans un
champ magnétique intense et sou-
mis à une onde de radiofréquence
précise subissent un phénomène
de résonance puis de relaxation à
l’origine du signal RMN.
Pour une série d’impulsions de
radiofréquence choisie (séquence
d’imagerie) les temps de relaxa-
tion T1, T2 (retour à une phase
d’équilibre des protons hydrogè-
nes) varient en fonction de la
nature des tissus. Ces variations
déterminent le contraste des ima-
ges (pondération T1 ou T2). Le
signal IRM dépend donc des
temps de relaxation.
La spectroscopie RMN est une
analyse détaillée des fréquences
de résonance (et non des temps de
relaxation) d’atomes de même
n a t u re dans un enviro n n e m e n t
chimique diff é rent. Dans des
conditions de très bonne homogé-
néité, la fréquence de résonance
pour un atome d’hydrogène dans
d i ff é rents composés chimiques
est déplacée selon le groupement
chimique dans lequel cet atome
est engagé. Par exemple, les
protons hydrogènes liés aux lacta-
tes ont une fréquence de résonan-
ce différente de celle des protons
hydrogènes liés aux lipides ou à
la choline). Ce déplacement chi-
mique permettant d’étudier l’en-
v i ronnement électronique d’un
atome est à l’origine de la spec-
troscopie RMN.
Les travaux de COSTELLO (1) ont
largement développé les mécanis-
mes de production du citrate pro-
statique à partir de modèles ani-
maux et d’extraits ex vivo de pro-
state. Cette glande produit, sécrè-
te et stocke des sécrétions riches
en citrate dont la concentration
est variable en fonction de ses
zones anatomiques. Des taux éle-
vés sont observés dans la zone
périphérique et des taux plus fai-
bles dans les zones transitionnelle
et centrale ainsi que dans les
zones peu glandulaires antérieu-
res et urétrales.
A la diff é rence des citrates, le
spectre de la choline n’est pas spé-
cifique d’un seul composé (phos-
phocholine, glycéro p h o s p h o c h o-
line, éthanolamine…) ce qui
explique l’importance de la choli-
ne dans les spectres des tissus
péri-urétraux car le liquide sémi-
nal est riche en glycérophopho-
choline (Figure 1).
III. LE MÉT
ABOLISME
PROST
A
TIQUE
II. RAPPEL DES ASPECTS
TECHNIQUES
: LE SIGNAL
RMN - LE SIGNAL
SPECTROSCOPIQUE
I. INTRODUCTION
N°2 Septembre 2003
Spectr
oscopie-IRM de la Pr
ostate
Richard Aziza, -
Radiologie Institut
Claudius Regaud.
QUESTION
D’ACTUALITÉ
Michel Soulié
Urologue CHU de Rangueil,
Toulouse

9
Un cancer se développant dans la
zone périphérique engendre une
augmentation du taux de choline
dans la zone périphérique norma-
le et une diminution du taux des
citrates car existent une diminu-
tion des sécrétions prostatiques,
une augmentation de l’oxydation
des citrates et une diminution des
canaux glandulaires contenant le
citrate.
La technique RMN actuelle offre
par codage 3D la possibilité de
localiser les spectres du citrate et
de la choline de toutes les régions
p rostatiques anormales, de les
corréler à une image haute résolu-
tion, de repérer l’extension spatia-
le du métabolite anormal et de
couvrir l’ensemble de la glande
prostatique. Les variations de ces
métabolites sont au mieux préci-
sées par un rapport choline +
créatine rapporté au lactate (déri-
vé des citrates). Ainsi dans les
zones tumorales, le rapport choli-
ne + créatine / lactate est aug-
menté. Des acquisitions m u l t i
voxel sont aujourd’hui disponibles
avec des temps d’examen raison-
nables de 20 à 30 minutes. Un exa-
men complet intégrant l’imagerie
anatomique et l’étude spectrosco-
pique avec l’antenne endorectale
ne dépasse pas une heure.
L’imagerie IRM « classique » en
pondération T2 représente les
zones pathologiques de la prosta-
te périphérique par des signaux
de faible intensité (hyposignal)
qui contrastent avec le signal
élevé des zones saines (hypersi-
gnal). Cependant toutes les
lésions de bas signal ne sont pas
toujours de nature maligne. La
détection des métabolites cellulai-
res dans ces zones suspectes chez
un patient porteur d’un cancer
prostatique améliore la spécificité
de l’examen (Figure 2).
Yu (2), Scheidler (3), Kurhanewicz
(4) ont décrit les premières appli-
cations cliniques puis l’améliora-
tion de la détection d’une exten-
sion extracapsulaire par l’utilisa-
tion conjointe de l’imagerie habi-
tuelle et de la spectroscopie 3D
proton. Kaji (5) a montré que la
spectroscopie associée à l’image-
rie augmente de manière très
significative la possibilité de
détecter les zones tumorales au
V
. APPLICA
TIONS CLINIQUES
IV
. V
ARIA
TION DU MÉT
ABO
-
LISME LIÉE AU CANCER
N°2 Septembre 2003
Question
D’ACTUALITÉ Spectr
oscopie-IRM de la Pr
ostate
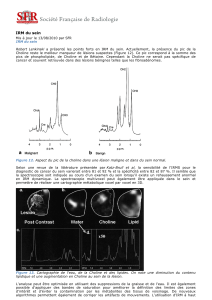
Figure 1 : cartographie des métabolites dans la zone centrale et périphérique de la prostate.

10
sein des foyers hémorragiques
après biopsies par rapport à la
seule utilisation de l’imagerie
classique. Le repérage de foyers
tumoraux est, de ce fait, forte-
ment utile dans le cas d’une
deuxième série de biopsies si la
première série n’est pas contribu-
tive (Figures 3 et 4).
Les traitements hormonaux et la
radiothérapie, au même titre que
des lésions de prostatites, des
dépôts de corps amylacés et des
hématomes post-biopsies, eff a-
cent le signal intense de la zone
périphérique et masquent les
zones tumorales. Evaluer l’effet
thérapeutique sur une plage
tumorale ou prouver une récidive
locale (en dehors de nouvelles
biopsies) est peu concevable par
l’imagerie spin écho habituelle.
La spectroscopie IRM offre l’a-
vantage de s’affranchir de ces
limites. Mueller-Lisse(6) a ainsi
montré que la spectroscopie 3D
RMN, combinée à l’imagerie
IRM, 4 mois après un traitement
hormonal avait la même capacité
et la même précision de localisa-
tion des zones tumorales que
pour un groupe témoin non traité
par hormonothérapie.
Coakley (7) a intégré la spectros-
copie RMN à l’imagerie IRM pour
étudier le volume tumoral. Il
d é m o n t re que la technique est
réalisable pour des volumes de
0,5 cm3mais qu’au-dessous de ce
seuil les variabilités de mesure
limitent l’estimation quantitative
du volume tumoral surtout pour
les petites tumeurs.
Ces quelques exemples montrent
les nouvelles possibilités de l’IRM
p rostatique avec spectro s c o p i e .
Cependant cette technique d’exa-
men n’est pas encore suffisam-
ment diffusée. Elle demande une
grande rigueur dans sa phase de
mise en place et une bonne
connaissance de cette nouvelle
sémiologie radiologique pour
l’interprétation des résultats.
N°2 Septembre 2003
Question
D’ACTUALITÉ Spectr
oscopie-IRM de la Pr
ostate
Figure 2 : identification des métabolites
dans une zone tumorale de bas signal à
droite (pic de citrate abaissé) et dans une
zone saine à gauche (pic de citrate élevé).
Figure 3 :A. la lésion de bas signal dans la zone périphérique
droite témoigne d’un cancer car le pic du citrate est effondré et
celui de la choline augmenté. B. ici la lésion de bas signal n’est
pas tumorale mais est liée à une séquelle de biopsie, le pic du
citrate est supérieur à celui de la choline.

11
1. Costello LC., Littleton GK,
Franklin RB : regulation of citrate-
related metabolism in normal and
neoplatic prostate. In Sharma RK,
CrissWE (eds):endocrine contro l
in neoplasia. New york, raven
press 1978, p 303.
2. Yu KK.et coll .: prostate cancer :
prediction of extracapsular exten-
sion with endorectal Mr imaging
and three-dimensional proton Mr
spectroscopic imaging. Radiology
1999; 213:481-488.
3. Scheidler J et coll.: prostate can-
cer :localisation with three-dimen-
sional proton Mr spectro s c o p i c
imaging, clinicopathologic study.
Radiology 1999; 231:473-480.
4. Kurhanewicz J et coll.: thre e -
dimensional H-1 MR spectrosco-
pic imaging of the in situ human
prostate with high ( 0.24-0.7 cm3)
spatial resolution. Radiology
1996; 198:795-805.
5. Kaji et coll. :localizing prostate can-
cer in the presence of postbiopsy
changes on Mr Images : role of
p roton MR spectroscopic imaging.
Radiology 1998; 206:785-790.
6. Mueller-Lisse U et coll. : localized
prostate cancer : effect of hormone
deprivation therapy measured by
using combined three-dimensio-
nal 1H MR spectroscopy and MR
imaging: clinicopathologic case-
controlled study. Radiology 2001;
221: 380-390.
7. Coakley FV et coll.: prostate can-
cer tumor volume: measurement
with endorectal MR and MR spec-
t roscopic imaging. Radiology
2002; 223: 91-7
RÉFÉRENCES
N°2 Septembre 2003
Question
D’ACTUALITÉ Spectr
oscopie-IRM de la Pr
ostate
Figure 4 : représentation colorimétrique des métabolites à partir des spectres du citrate et de la choline de la tumeur
prostatique dans la zone périphérique gauche.
*images provenant d’une plaquette d’information technique de Ge Medical Systems.
1
/
4
100%