Lettre d`intention Syndrome de Lynch et instabilité des

Lettre d’intention Syndrome de Lynch et instabilité des microsatellites
Titre
« Criblage moléculaire du syndrome de Lynch et instabilité des microsatellites »
Acronyme
DEFMMR
Première soumission de ce projet de recueil de données ?
OUI
Nom et prénom de l’investigateur-coordinateur
Dr Chrystelle COLAS – Pitié Salpêtrière
Dr Marie-Pierre BUISINE - Lille
Financement(s) antérieur(s) dans le cadre des appels à projet de la DGOS
NON
Sociétés savantes coordinatrices
GFCO (E Rouleau) - GGC (MP Buisine) – SFP (JY Scoazec)
Médecin, Chirurgien-Dentiste / Biologiste / Infirmière / autres Paramédicaux
Anatomopathologiste, Biologiste /Techniciens et ingénieurs en biologie moléculaire
Etablissement-coordonateur responsable du budget pour le Ministère de la santé
Domaine de Recherche
Oncologie – cancer du côlon, cancer de l’endomètre et cancer associé au spectre du
Syndrome de Lynch.
Nom du méthodologiste (+ tel + email) à déterminer
Nom de l’économiste de la santé (si nécessaire) (+ tel + email) à détermine
Structure responsable de la gestion de projet à déterminer
Structure responsable de l’assurance qualité à déterminer
Structure responsable de la gestion de données et des statistiques à déterminer
Nombre prévisionnel de centres d’inclusion (NC)
28 plateformes financées par l’INCa
16 laboratoires impliqués dans la génétique constitutionnelle du syndrome de Lynch
Co-investigateurs (1 à N)
Nom
Etablissement
Ville Pays Hôpital E-mail Tel
Spécialité}]
Domaine d’expertise
Dr Chrystelle Colas
Pitié Salpêtrière
<chrystelle.colas@psl.aphp.fr>
Syndrome de Lynch
Dr Marie-Pierre Buisine
Lille
<marie-pierre.buisine@chru-
lille.fr>
Syndrome de Lynch
Pr Olivier Schischmanoff
Hôpital Avicenne, BOBIGNY
74, rue Marcel Cachin
93017 BOBIGNY
Screening Syndrome de
Lynch et

Utilisation thérapeutique
des MSI
Dr Etienne Rouleau
CLCC – Paris
Utilisation thérapeutique
des MSI
Pr Antoinette Lemoine
Paul Brousse – Paris
Syndrome de Lynch
Pr Hagay Sobol
CLCC Marseille
Syndrome de Lynch
PROJET DE RECHERCHE
Rationnel (contexte et hypothèses)
Le syndrome de Lynch est associé principalement à une augmentation du risque de
cancers colorectaux et de cancer de l’endomètre. Il s’agit d’une prédisposition génétique à
transmission autosomique dominante liée à une altération génétique constitutionnelle d’un
gène MMR de réparation des mésappariements de l’ADN :des gènes MLH1, MSH2, MSH6 et
PMS2, ceci est à l’origine d’un risque accru de cancer colorectal, avec un risque cumulé de
30-48 % avant l’âge de 70 ans, mais aussi de cancer gynécologique, avec un risque cumulé
de 33% pour l’endomètre et de 9% pour l’ovaire (Bonadona et al, JAMA 2011;305:2304-10).
Le risque concerne aussi d’autres organes, avec une fréquence moindre (spectre du syndrome
de Lynch).
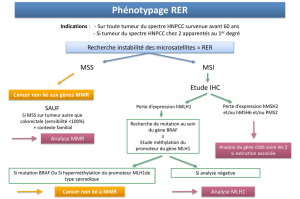
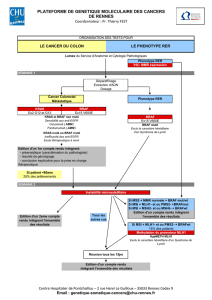
Les tumeurs développées dans le cadre du syndrome de Lynch présentent une
déficience du système MMR révélée par l’association d’une instabilité microsatellitaire (MSI
pour MicroSatellite Instability) et d’une perte d’expression d’une ou deux protéines MMR. La
recherche de cette déficience permet donc d’identifier des patients susceptibles d’être porteurs
d’une altération constitutionnelle d’un gène MMR et devant de ce fait être orientés vers une
consultation d’oncogénétique.
La défaillance du système MMR se traduit en effet par une perte d’expression d’une ou
deux protéines MMR et par une augmentation/accumulation des erreurs de réplication
particulièrement sur les séquences répétées de type microsatellites (séquences d’ADN mono,
di ou tri-nucléotidiques répétées en tandem au sein du génome).
La défaillance du système MMR peut aussi concerner des tumeurs sporadiques.
Cette défaillance est alors majoritairement liée à une répression épigénétique de l’expression
du gène MLH1 par hyperméthylation de son promoteur. En complément des tests
somatiques recherchant une déficience du système MMR, il est donc nécessaire dans
certains cas (tumeurs présentant une perte de la protéine MLH1) de mettre en œuvre une
recherche de méthylation du promoteur du gène MLH1 et de la recherche de mutation du
gène BRAF (uniquement cancer colorectal) avant de préconiser l’orientation vers une
consultation d’oncogénétique. L’application du gène BRAF n’est pas valable dans les autres
cancers du spectre (Estomac / Domingo et al., 2004).
- Côlon / MLH1 : Bettstetter M, Dechant S, Ruemmele P, Grabowski M, Keller G, Holinski-Feder E,
Hartmann A, Hofstaedter F, Dietmaier W. Distinction of hereditary nonpolyposis colorectal cancer and
sporadic microsatellite-unstable colorectal cancer through quantification of MLH1 methylation by real-time
PCR. Clin Cancer Res. 2007
- Endomètre / MLH1 Goodfellow PJ, Billingsley CC, Lankes HA, Ali S, Cohn DE, Broaddus RJ, Ramirez N,
Pritchard CC, Hampel H, Chassen AS, Simmons LV, Schmidt AP, Gao F, Brinton LA, Backes F, Landrum
LM, Geller MA, DiSilvestro PA, Pearl ML, Lele SB, Powell MA, Zaino RJ, Mutch D. Combined Microsatellite
Instability, MLH1 Methylation Analysis, and Immunohistochemistry for Lynch Syndrome Screening in
Endometrial Cancers From GOG210: An NRG Oncology and Gynecologic Oncology Group Study. J Clin
Oncol. 2015 Dec 20;33(36):4301-8.
- Endomètre / MLH1 Garg K, Soslow RA. Lynch syndrome (hereditary non-polyposis colorectal cancer) and
endometrial carcinoma. J Clin Pathol. 2009 Aug;62(8):679-84.

- Goodfellow et al, 2009 ; Hampel et al. 2006
- Côlon / BRAF Wang L, Cunningham JM, Winters JL, Guenther JC, French AJ, Boardman LA, Burgart LJ,
McDonnell SK, Schaid DJ, Thibodeau SN. BRAF mutations in colon cancer are not likely attributable to
defective DNA mismatch repair. Cancer Res. 2003 Sep 1;63(17):5209-12.
Enfin, il existe des applications thérapeutiques pour l’utilisation du phénotype de
défaillance du système MMR par le test MSI. L’instabilité des microsatellites peut être utilisée
dans les cas de cancer colorectal de stade 2 afin d’orienter la décision d’une chimiothérapie
adjuvante. En effet, une chimiothérapie adjuvante n’est à l’heure actuelle pas recommandée
chez les patients avec tumeurs de stade 2 MSI (Thésaurus National de Cancérologie
Digestive, 20/07/2011).
- MSI/5-FU Sargent, D. J. et al. Defective mismatch repair as a predictive marker for lack of efficacy of
fluorouracil-based adjuvant therapy in colon cancer. J. Clin. Oncol. 28, 3219–3226 (2010).
- MSI/Immunothérapie Le, D. T. et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N. Engl.
J. Med. 372, 2509–2520 (2015).
La recherche d’instabilité microsatellitaire en complément de l’IHC des protéines MMR,
la méthylation du gène MLH1 et la mutation BRAF sont utilisées depuis des années dans
l’orientation des patients dans le contexte de suspicion de syndrome de Lynch. Il est donc
demandé une validation par l’HAS de leur utilité clinique. Par contre, le criblage de population
pour identifier des familles avec une prédisposition génétique reste en cours d’évaluation.
Parallèlement, l’utilisation thérapeutique des microsatellites est pratiquement validée
pour les tumeurs de stade 2 dans le cancer colorectal et doit encore être validée pour
l’immunothérapie. L’arrivée de l’immunothérapie semble indiquer une utilisation/utilité
probable de ce marqueur pour identifier les tumeurs hypermutées, les plus susceptibles de
répondre au traitement (Le at al, NEJM 2015).
Originalité et Caractère Innovant
Les actes associés au criblage somatique du syndrome de Lynch doivent être évalué
par l’HAS car ils sont matures.
L’utilisation des microsatellites dans le cadre thérapeutique peut encore faire l’objet
d’un recueil de données, mais devrait sous moins de 3 ans passer à l’HAS.
Objet de la Recherche
Marqueurs concernés
Liste RIHN
N500
Instabilité microsatellitaire
N533
Méthylation MLH1
Liste complémentaire
N501
Recherche de la mutation BRAF V600 par technique moléculaire

Mots Clés [5]
Instabilité des microsatellites, syndrome de Lynch, prédisposition au cancer, épigénétique
Objectif Principal
Les données sur le criblage du syndrome de Lynch sont déjà bien documentées.
A déterminer – évaluation principalement à réaliser avec l’utilisation théranostique.
Objectifs Secondaires A déterminer
Critère d'évaluation principal (en lien avec l’objectif principal A déterminer
Critères d'évaluation secondaires (en lien avec les objectifs secondaires) A déterminer
Population d’étude
Il y a deux sources de recrutement : patients ayant eu une consultation d’oncogénétique,
patients ayant un cancer du spectre à un jeune âge (criblage de population). Pour ces
derniers cas, l’INCa a préconisé un criblage des patients de moins de 60 ans.
Plan expérimental A déterminer
Si Analyse Médico-économique A déterminer
Si groupe comparateur A déterminer
Durée de la participation de chaque patient A déterminer
Durée prévisionnelle de Recrutement (DUR) A déterminer
Nombre de patients / observations prévu(e)s à recruter (NP) A déterminer
Nombre de patients / observations à recruter / mois / centre ((NP/DUR)/NC) A
déterminer Nombre attendu de patients éligibles dans les centres A déterminer
Participation d’un réseau de recherche A déterminer
Participation de partenaires industriels A déterminer
Autres éléments garantissant la faisabilité du projet
Il s’agit d’étude déjà en place dans les laboratoires des plateformes de génétique somatique
des tumeurs.
Bénéfices attendus pour le patient et/ou pour la santé publique
Les actes décrits dans cette lettre d’intention sont réalisés en routine dans les laboratoires.
MOTS CLES
Domaine du coordinateur : généticien clinique et généticien moléculaire spécialisé dans le
cancer colorectal
Domaine du rapporteur suggéré : génétique somatique des tumeurs solides
COMMENTAIRES DES EXPERTS [citer] ET REPONSES CORRESPONDANTES
1
[max 320 mots]
1
Item à compléter si le projet a déjà été soumis à un appel à projets de la DGOS.
1
/
4
100%