2015-exos03-analyse spectrale2 - leprof

1
Exercice 1 : Etude de spectres
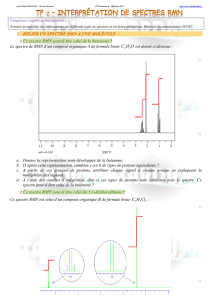
1- Le spectre de RMN d’une espèce de formule brute C3H6O2 est donné
document 1. Cette espèce peut-elle être l’acide propanoïque ?
2- Le spectre de RMN d’une espèce de formule brute C2H6O est donné document 2.
Identifier cette espèce.
(la question posée ainsi est hors programme élève)
3- Le spectre de RMN d’une espèce de formule brute C2H4Cl2 est donné document 3. Identifier cette espèce.
Document 1 : Document 2 : Document 3 :
Exercice 2 : Identifier des groupes caractéristiques à l’aide de spectres IR et RMN (4 points)
La bande due à la liaison C=O (1650 – 1 800 cm–1) est l’une des plus caractéristiques de l’infrarouge. Très
intense du fait de la forte polarité de cette liaison, elle est vite reconnue. La présence de cette bande n’est qu’un
indice sur la structure de la molécule. C’est l’examen des autres bandes associées à la fonction qui permet
l’identification du composé.
1- À quoi est due la polarité de la liaison C=O?
2- On va étudier les spectres infrarouges de quatre composés : le butanal, la butanone, l’acide butanoïque et le
butanoate de méthyle.
2.1- Donner la formule semi-développée de ces quatre composés en nommant le groupe fonctionnel
correspondant.
2.2- À partir des spectres fournis en annexe et des tables, relier chaque type de liaison à son nombre d’onde.
2.3- L’indication « cette bande est une des plus caractéristiques de l’infrarouge (1650 – 1800 cm–1) » est-elle
confirmée ici ?
2.4- Comment distinguer un aldéhyde d’une cétone à partir du seul spectre infrarouge ?
2.5- Qu’est-ce qui permet d’identifier la présence d’un acide carboxylique ? Justifier.
3- Composé inconnu
3.1- On donne ci-dessous le spectre infrarouge d’un composé inconnu. Que pouvez-vous déduire de ce spectre ?
Peut-on déterminer exactement la fonction du composé ?
3.2- À partir d’une analyse complémentaire, on détermine la formule brute du composé inconnu C4H8O2. Cette
formule est-elle compatible avec l’analyse précédente ?
3.3- Donner alors les formules semi-développées envisageables des isomères de formule C4H8O2.
3.4- Le spectre RMN de ce composé montre trois signaux sur le spectre, quel composé pouvez-vous éliminer ?
3.5- Avec les valeurs des déplacements chimiques données en annexe, interpréter le spectre RMN suivant et
identifier le composé inconnu. Le nommer.

2
Annexes : Spectres IR
Déplacements chimiques
Exercice 3 : étude d’un anti-inflammatoire
Description de l’ibuprofène
La molécule d’ibuprofène possède deux stéréoisomères, notés R et S, représentés ci-dessous :
Molécule R
Molécule S
1- Quel est le nom du groupe caractéristique oxygéné que comporte l’ibuprofène ? Quelle est la fonction
chimique correspondante ?
2- Quel qualificatif utilise-t-on pour désigner l’atome de carbone noté 2 sur les représentations ci-dessus ?
3- Les molécules R et S sont-elles identiques, énantiomères ou diastéréoisomères ? Justifier.
Proton
δ
Proton
δ
CH3–C
0,9 ppm
C–CH2–C
1,3 ppm
CH3–CO–O–R
2,0 ppm
C–CH2–CO–O–R
2,2 ppm
CH3 –O–CO–R
3,7 ppm
C–CH2–O–CO
4,1 ppm
CH3–
–CH2–

3
Document 2 : Bandes d’absorption IR de quelques types de
Document 1 : Spectre infrarouge de l’ibuprofène liaisons chimiques
Document 3 : Spectre RMN de l’ibuprofène
L’aire du doublet (a) est environ six fois supérieure à celle du singulet (g), c’est-à-dire que le saut de la courbe
d’intégration est six fois plus grand pour (a) que pour (g).
Document 4 : Déplacements chimiques en ppm (partie par million)
4-. Diverses techniques d’analyse ont permis de connaître la structure de la molécule d’ibuprofène. Les
spectroscopies IR (infrarouge) et de RMN (résonance magnétique nucléaire) en sont deux exemples.
4.1- Donner l’origine des bandes d’absorption 1 et 2 du spectre infrarouge IR (document 1) en exploitant les
données du document 2.
4.2- Représenter l’ibuprofène en formule semi-développée et entourer le ou les atomes d’hydrogène associés au
signal (g) du spectre RMN. Justifier votre réponse à l’aide du document 4.
4.3- Toujours sur la formule semi-développée de l’ibuprofène dessinée en 1.4.b, entourer la ou les atomes
d’hydrogène associés au signal (a) du spectre RMN. Justifier votre réponse.
4.4- signal (a) est un doublet. Justifier cette multiplicité.

4
Exercice 4 : Suivi d'une réaction de déshydratation (4 points)
La réaction en milieu acide de déshydratation du 2-méthylbutan-2-ol en 2-méthylbut-2-ène (Fig. 1) est étudiée.
Pour s'assurer que la réaction s'est bien déroulée, on effectue un spectre RMN du réactif de départ (Fig. 2) et du
produit de réaction (Fig. 3). Le signal intégral nous permet de connaître le nombre de protons associés à chacun
des signaux RMN (ce nombre est indiqué ici directement sur les spectres).
Réaction étudiée.
Spectre RMN du 2-méthylbutan-2-ol. Spectre RMN du 2-méthylbut-2-ène.
1- Étude du spectre du 2-méthylbutan-2-ol
1.1- Repérer les groupes de protons équivalents du 2-méthylbutan-2-ol et montrer que leur nombre et le nombre
de signaux observés sur le spectre sont cohérents.
1.2- Attribuer chaque signal du spectre à l'un des quatre groupes de protons équivalents du
2-méthylbutan-2-ol.
1.3- Quel est le déplacement chimique du proton de la fonction alcool ?
1.4- Proposer une interprétation de la multiplicité des trois signaux à 0,90 ;1,25 et 1,45 ppm.
2- Étude du spectre du 2-méthylbut-2-ène
2.1- Quel est le déplacement chimique du proton entouré sur la molécule ci-contre ?
2.2- À quel groupe de protons est associé le signal à 2,05 ppm ?
2.3- Est-il possible d'attribuer précisément les deux singulets à 1,80 et 1,70 ppm ?
3- Étude d'un mélange
La réaction est arrêtée au bout de 3 minutes. Le spectre RMN du mélange est réalisé. Parmi les différents
signaux, on observe un triplet à 0,90 ppm et un singulet à 1,70 ppm. Le signal intégral est deux fois plus grand
pour le triplet que pour le singulet.
3.1- L'alcool a-t-il été totalement convertit en alcène?
3.2- Le mélange contient-il plus d'alcool ou d'alcène ?
Exercice 5 : Réaction de Cannizzaro
La réaction de Cannizzaro produit deux espèces organiques que l'on peut séparer. L'objectif de cet
exercice est de montrer comment les spectroscopies IR et de RMN permettent d'identifier chacun des
produits obtenus.
1- Illustration de la réaction sur le benzaldéhyde
Le benzaldéhyde, dont la formule topologique est donnée ci-dessus, est un liquide incolore à odeur d'amande
amère utilisé pour parfumer le kirsch ou encore le sirop d'orgeat. La réaction du benzaldéhyde avec une solution
d'hydroxyde de sodium conduit, après chauffage puis retour à un milieu acide, à deux produits organiques:
Al, de formule brute C7H8O, et A2, de formule brute C7H6O2.
Cette réaction est appelée réaction de Cannizzaro. Lors de cette réaction, le cycle à six atomes de carbone du
benzaldéhyde n'est pas modifié.

5
Document 1 : Spectre IR en phase condensée du produit A1 Document 2 : Spectre de RMN du produit A1
Document 3 : Spectre IR en phase condensée du produit A2 Document 4 : Spectre de RMN du produit A2
1.1- Quel(s) spectre(s) est-il judicieux d'analyser pour identifier la nature du (des) groupe(s) caractéristique(s)
présent(s) dans chaque produit?
1.2- Quel groupe caractéristique est vraisemblablement présent dans le produit A1 ? Justifier.
1.3- En déduire une formule topologique pour A1.
1.4- En utilisant une démarche analogue, proposer une formule topologique pour la molécule A2.
1.5- Analyser les spectres de RMN du proton des molécules A1 et A2 et vérifier qu'ils sont cohérents avec les
formules topologiques proposées.
Aide. Le plus souvent, un atome d'hydrogène porté par un atome d'oxygène n'est pas considéré comme voisin
d'autres atomes d'hydrogène.
1.6- Proposer une équation pour la réaction de Cannizzaro subie par le benzaldéhyde. On pourra s'aider des
formules brutes des réactifs et produits.
2- La réaction de Cannizzaro subie par le glyoxal (ou éthanedial) conduit à un unique produit B, de formule
brute C2H4O3.
Pourquoi la réaction de Cannizzaro conduit-elle dans ce cas à une unique espèce chimique? Proposer une
formule semi-développée pour cette espèce.
Exercice 6 : Départager des isomères par spectroscopie
L'objectif de cet exercice est de montrer que les spectroscopies IR et de RMN peuvent permettre d'identifier
deux isomères.
Un chimiste dispose de deux molécules isomères A et B de formule brute C3H6O. Il sait que chaque formule
topologique représentée ci-dessous correspond à l'un de ces isomères.
1- Vérifier que ces deux molécules sont bien isomères.
2- Laquelle est le propanal ?
3- Combien le propanal contient-il de groupes de protons équivalents?
Doc 1 : Spectre de
RMN de la molécule A
Doc 2 : Spectre de
RMN de la molécule B
Doc 3 : Spectre IR de
l'un des deux isomères
 6
6
1
/
6
100%