1- Appareil cardiovasculaire

1- Appareil cardiovasculaire - Physiologie
18 janvier 2012
1
Typeur : Camille.C , Raoul.R Examinateur : Eya.J
L’activité électrique du cœur
L’activité électrique du cœur est générée par un ensemble de cellules excitables qui crée un potentiel
d’action en réponse à un stimulus externe.
Certaines de ces cellules ont une activité « pacemaker » (isolée) c'est-à-dire automatique qui peuvent
être à la base du rythme cardiaque. Cependant il faut aussi que les cellules cardiaques soient
adaptables et donc qu’elles reçoivent des afférences, des informations du système.
Les cellules cardiaques sont organisées en réseaux, connectées les unes aux autres. Ces réseaux
ajoutés aux cellules pacemaker sont à l’origine du rythme cardiaque automatique mais qui a la
propriété de pouvoir s’adapter. L’activité électrique est donc adaptable.
L’ensemble produit le rythme cardiaque automatique.
L’activité électrique de cet ensemble de réseaux électrique cardiaque peut être enregistrée à distance
par des électrodes placée sur la peau, c’est l’électrocardiogramme.
L’activité électrique cardiaque est très semblable d’un individu à l’autre, on peut donc définir des
normes et un électrocardiogramme normal.
L’analyse de l’électrocardiogramme permet de diagnostiquer certaines pathologies cardiaques
associées à des désordres des propriétés électriques du réseau cardiaque.
Il est aussi possible de suivre l’évolution de certaines pathologies et d’évaluer l’efficacité
thérapeutique.
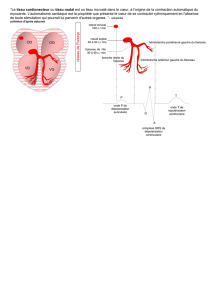
I. Rappel anatomique
On a un cœur droit et un cœur gauche, une grande circulation avec l’aorte et une petite avec l’artère
pulmonaire. Le sang oxygéné est expulsé du ventricule gauche vers l’oreillette gauche vers l’aorte, il
nourrit les tissus puis revient au cœur par les veines cave inf et sup à l’oreillette droite, puis passe
dans le ventricule droit, il est pauvre en Oxygène, il expulsé vers les artères pulmonaires pour
l’oxygéner dans les poumons, et revient par les veines pulmonaires dans le ventricule gauche.
Pour ce contracter le cœur à besoin d’une pompe composée de muscle strié composé de cellules
myocardiques avec une réponse à la mise en jeu des cellules nodales, cellules pilotes de cet
automatisme.

2
II. Tissus nodal
Dans le tissu nodal, on trouve les cellules automatiques.
Il y a différents amas de cellule qui ne constituent en fait qu’un seul et grand réseau : le tissu nodal.
a) Disposition
Le nœud sinusal (Nœud de Keith et Flack) au niveau de l’oreillette droite sera suivi en dessous par
le nœud auriculo-ventriculaire (Nœud d’Ashoff Tawara) situé entre l’oreillette droite et le
ventricule droit puis vient le faisceau de Hiss avec une branche droite et une branche gauche. Il va
ensuite se ramifié en réseau de fibres de Purkinje et innerver le muscle strié cardiaque c'est-à-dire le
tissu myocardique.
Le tissu nodal permet l’élaboration de l’influx nerveux et de sa propagation vers les tissus
myocardique à l’origine du rythme cardiaque.
Le tissu myocardique est un tissu musculaire strié à l’origine de la contraction.
b) ECG
L’ECG est un complexe d’ondes :
- L’onde P correspond à la dépolarisation auriculaire
- Le complexe QRS correspond à la dépolarisation ventriculaire
- L’onde T correspond à la repolarisation ventriculaire
**S’il y a un bloc de conduction entre oreillette et ventricule, il allonge le délai entre l’onde P et
QRS.
** Si il a des troubles de la dépolarisation ventriculaire, c’est le syndrome du QT long, augmentation
du délai entre l’onde Q et T.
La forme des ondes va également avoir une indication pathologique ou non.
c) Propagation
L’influx nait au niveau du nœud sinusal et provoque la contraction du myocarde auriculaire. Il se
propage au nœud auriculo-ventriculaire avec une latence de 0,15sec.
Il se propage au tronc du faisceau de Hiss puis dans ses branches au niveau des cellules du
myocarde ventriculaire par le réseau de Purkinje et créé une contraction.
Le myocarde auriculaire est séparé du myocarde ventriculaire par un anneau fibreux permettant
d’isoler ces deux myocardes électriquement (séparation des contractions).
Les délais sont liés aux vitesses de conductions élevées de 4m/sec et au délai de 0,15sec entre nœud
sinusal et nœud auriculo-ventriculaire.

3
C’est un système stable chez les individus normaux mais on peut avoir des ralentissements (bloc).
L’organisation des tissus est différentes entre les cellules myocardiques et les cellules nodales (non
contractiles).
Les cellules myocardiques sont liées de manières électriques par des Gap-jonctions.
III. L’activité électrique des cellules myocardique
Ce sont des éléments excitables :
- Potentiel de repos de -90mV
- Potentiel d’action avec 5 phases en plateau
Elles sont liées entre elles par des gap-jonctions.
Les 5 phases du potentiel d’action sont :
- 0 : ouverture des canaux Na rapide dépolarisation rapide
- 1 : fermeture des canaux Na rapide repolarisation rapide et partielle
- 2 : entrée de Ca et de Na par des canaux lents dépolarisation en plateau
- 3 : sortie de K+ repolarisation tardive et lente
- 4 : pompe NA/K retour au potentiel de repos, équilibre ionique.
Comparaison entre le Potentiel d’Action d’une fibre myocardique et le potentiel d’action d’un
neurone : Il y a une importante différence de temps : ici on aura un temps de potentiel d’action des
cellules myocardique de 400ms contre 4ms pour un neurone. Le potentiel d’action d’une cellule
myocardique est très lent.
Phase 0
C’est une dépolarisation rapide (1ms) de grande amplitude (110-120mV) aboutissant à une
inversion de potentiel de membrane.
On a une ouverture de canal sodium (canal rapide, 1 à 2ms) permettant un flux entrant de Na
voltage dépendant (seuil). La dépolarisation de la cellule va donc entrainer une augmentation de la
probabilité d’ouverture des canaux Na ce qui explique la rapidité d’ouverture.
L’ouverture des canaux Na entraine un déplacement du potentiel de membrane vers le potentiel
d’équilibre du sodium ENa (+58mV).
Mais progressivement, l’inactivation des canaux Na évolue vers la mise en place de la phase de
repolarisation rapide.

4
Phase 1
C’est la phase de repolarisation initiale rapide (quelques ms) partielle vers un potentiel de
membrane en plateau à 0mV.
Elle s’explique par une fermeture des canaux sodium rapide et donc un arrêt du flux de Na entrant.
Parallèlement on a une ouverture transitoire des canaux potassiques voltage dépendant (canaux
rapides) ce qui donne un flux sortant de Potassium avec 2types de canaux :
- Canaux It01 bloqué par la 4-aminopyridine et indépendant du Ca intracellulaire
- Canaux It02 bloqué par TEA et dépendant du Ca intracellulaire
Si le Ca intracellulaire augmente, It02 augmente et entraine un raccourcissement du PA et une
diminution du Ca intracellulaire (régulation).
Phase 2
C’est la phase de repolarisation lente (200-300ms) avec un maintien d’un potentiel de membrane en
plateau à 0mV.
On a une balance entre le courant entrant positif (dépolarisant) et le courant positif sortant
(repolarisant).
Le courant entrant positif correspond à l’ouverture des canaux calcium lents voltage-dépendant L
(ventriculaire lent) ou T (atrial, nodal, Purkinje transitoire).
Le flux entrant de Ca est un déclencheur de la contraction par libération du calcium du réticulum
sarcoplasmique.
Le courant sortant positif est le courant potassique retardé voltage dépendant.
Phase 3
C’est la phase de repolarisation rapide. C’est une repolarisation membranaire vers EK
(-90mV).
On a une inactivation des courants calciques et une augmentation des courants potassiques
(Ik jusque -5àmV puis Ik0).
Phase 4
C’est la phase de repolarisation terminale rapide.
Les canaux K1 sont ouvert avec le potentiel de repos qui correspond à EK (-90mV)
C’est une phase stable puisque la somme des courants positifs sortant et négatifs entrant est égale à
0.
Il y a une restauration par la pompe Na/K (ATP dépendante)

5
IV. Autorythmicité
C’est le potentiel d’action des cellules nodales.
On aura 2 types de cellules nodales selon la vitesse de dépolarisation.
Les fibres à réponse lentes permettent la genèse de l’excitation cardiaque (nœuds sinusal et
auriculo-ventriculaire).
Les fibres à réponse rapide permettent la conduction de l’excitation (faisceau de Hiss et Purkinje).
La vitesse de dépolarisation (potentiel de repos vers potentiel seuil) est modifié par :
- L’acétylcholine qui diminue la vitesse de dépolarisation en diminuant la fréquence des PA et
donc la fréquence cardiaque.
- Les catécholamines qui augmentent la vitesse de dépolarisation en augmentant la fréquence
des PA et donc la fréquence cardiaque.
Fibres à réponse lente
Permettent la genèse de l’excitation cardiaque : Nœud sinusal et Nœud Auriculo-Ventriculaire. Le
potentiel de membrane est instable avec une dépolarisation lente pendant la diastole qui est
l’origine de l’automatisme cardiaque (diminution progressive de la perméabilité au K+ et donc de la
sortie de K+ et adaptation du potentiel de membrane).
Différences avec les cellules myocardiques :
- Potentiel diastolique plus faibles (-80mV)
- Vitesse de dépolarisation plus lente (100ms)
- Amplitude de PA plus faible
- Sommet arrondi, pas de plateau
- Phase 0 : canaux Ca au lieu de Na
- Instabilité du potentiel de repos (à l’origine de l’automatisme cardiaque et différence
principale +++)
Fibres à réponse rapide
Permettent la conduction de l’excitation : faisceau de Hiss et fibres de Purkinje
Ce sont les même que les cellules myocardiques mais on aura une instabilité du potentiel de repos
pendant la diastole avec une dépolarisation diastolique lente (phase 4).
Vitesse de dépolarisation
La vitesse de dépolarisation varie en fonction de la structure considérée.
Au niveau du nœud sinusal, elle est de 75cycle/min.
C’est la zone pacemaker avec une dépolarisation rapide. On parle de rythme normal ou rythme
sinusal.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%