Cours 2 : Suivi d`une réaction chimique I – Transformation chimique

COURS 2 : SUIVI D’UNE REACTION CHIMIQUE
I – TRANSFORMATION CHIMIQUE
1 – Système chimique
Un système chimique : ……………………………………………………………………………………………………………
…………………………………………..
Exemple : (TP volume molaire)
L’état du système est décrit par :
-
-
-
Exemple : (TP volume molaire)
Etat initial : ………………………………………………………………………………………………………….
Etat final : ………………………………………………………………………………………………………….
2 – Transformation chimique
C’est le passage du système de l’état initial à l’état final.
Cl-(aq) n’a pas été affecté par la transformation chimique c’est ………………………………………………...
Au cours de la transformation :
- certaines espèces chimiques disparaissent au moins partiellement : ce sont ………………………………..
Exemples :
- de nouvelles espèces chimiques sont formées : ce sont …………………………………….
Exemples :
3 – Réaction chimique
Une réaction chimique est le modèle d’une transformation chimique. On la symbolise par une équation chimique :
………………………………. ………………………………………….
Exemple :
Cette équation est équilibrée par des coefficients stoechiométriques pour permettre de respecter la conservation des éléments et
des charges lors de la transformation chimique.
Il ne peuvent être placé que devant les réactifs ou les produits pas à « l’intérieur ».( 2 CO mais pas C2O)
Equilibrer les équation suivantes :
Cu2+ + HO- Cu(OH)2 N2 + H2 NH3 Fe2O3 + H2 Fe + H2O
C + O2 CO SO2 + O2 SO3 CuO + C CO2 + Cu
Etat initial
Etat final
Transformation
chimique

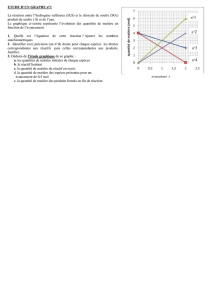
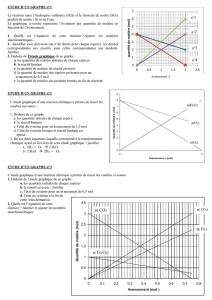
II - ETUDE DE L’EVOLUTION DU SYSTEME
1 – Notion d’avancement
L’avancement d’une réaction chimique est une valeur, notée …………., qui permet de déterminer les quantités de matière des
réactifs et des produits tout au long de la transformation. (à l’état initial, au cours de la transformation, à l’état final).
Exemple 1 : Mg + 2 H+ Mg2+ + H2
Quand ………………….. de magnésium réagissent, …………………… d’ions hydrogène réagissent, ………… d’ions
magnésium et …………………………… de dihydrogène apparaissent.
2 – Réactif limitant
L’état final est atteint quand l’avancement est ……………………………. et lorsque l’un ,au moins, des deux réactifs a
………………………………. : ce réactif est alors ……………………………………………………...
3- Tableau d’avancement
Exemple 1 :
Equation de la réaction : Mg + H+ Mg2+ + H2
Etat du système
avancement
nMg (en mol)
nacide(en mol)
nMg2+(en mol)
nH2 (en mol)
Etat initial
0
0,10
0,45
0
0
Etat intermédiaire
X
Etat final
Xmax =
Quel est le réactif limitant ?
Exemple 2 :
Equation de la réaction : O2 + H2 H2O
Etat du système
avancement
nO2
nH2
nH2O
Etat initial
0
3
1
0
Etat intermédiaire
x
Etat final
xmax =
Quel est le réactif limitant ?
III – ETUDE DE CAS PARTICULIERS
1- Mélange stoechiométrique
On introduit 810 mg d’aluminium dans un flacon contenant 540 mL de dioxygène, il se forme de l’alumine Al2O3.
Données : M(Al) = 27,0 g.mol-1 ; M(O) = 16,0 g.mol-1 ;Vm = 24,0 L.mol-1
1) Ecrire l’équation bilan de la réaction.
2) Calculer les quantités de matière des réactifs mis en jeu.
nAl =
nO2 =

3) Dresser la tableau d’avancement. Y a t’il un réactif limitant ?
Equation de la réaction :
Etat du système
avancement
Etat initial
0
Etat intermédiaire
X
Etat final
Réactif limitant :
4) Quelle sera la masse d’alumine formé ?
m(Al2O3) =
2- Réaction réalisée à V ou P constants.
Le sodium métallique Na réagit violemment avec l’eau : la réaction produit du dihydrogène, des ions Na+ et des ions HO-. On
mesure V = 50,0mL d’eau et m = 0,23g de sodium métallique.
Données :
eau = 1,00 g.cm-3 ; M(Na) = 23,0 g.mol-1 ; M(H) = 1,0 g.mol-1 ; M(O) = 16,0 g.mol-1
1) Calculer les quantités de matière initiales des réactifs.
2) Ecrire l’équation chimique de la réaction.
3) Dresser le tableau d’avancement de la réaction et déterminer le réactif limitant.
Equation de la réaction :
Etat du système
avancement
Etat initial
Etat intermédiaire
Etat final
Quel est le réactif limitant ?
4. Quelle sera la quantité de matière de dihydrogène produite par la réaction ?
1
/
3
100%