Mai 2005 - De la mère au nourrisson

Pathophysiologie
Cycle menstruel
Nous décrivons ici les principales caractéristiques du cycle
menstruel afin de faciliter la compréhension des traite-
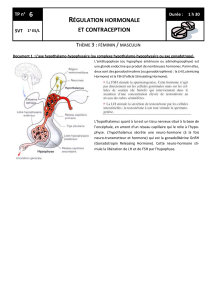
ments utilisés lors d’infertilité3,4. Le cycle est illustré à la
figure 1. Le jour 1 correspond à la première journée de la
menstruation (flot sanguin soutenu).
L’hypothalamus libère de façon pulsatile la
gonadolibérine (GnRH ou gonadotropin releasing hor-
mone). Sa libération est stimulée par l’adrénaline ou la
noradrénaline, et est inhibée par la dopamine ou la séro-
tonine.
Au niveau de l’hypophyse antérieure, la GnRH
stimule la libération des gonadotrophines, soit l’hormone
folliculo-stimulante (FSH) et l’hormone lutéinisante
(LH). La FSH stimule le recrutement (3eau 7ejours) et
la maturation (7eau 14ejours) de quelques follicules
ovariens. En général, un seul devient le follicule domi-
nant et libère de l’œstradiol, dont la quantité augmente
au fur et à mesure de sa maturation. L’œstradiol exerce
une rétroaction négative sur la libération de GnRH et de
FSH, amenant la dégénérescence des autres follicules
recrutés. L’œstradiol prépare aussi l’implantation de l’em-
bryon et favorise la production d’un mucus de bonne
qualité pour la motilité des spermatozoïdes.
Lorsque les concentrations sériques d’œstradiol
atteignent un certain seuil de façon soutenue, il y a une
libération rapide de LH au niveau de l’hypophyse, per-
mettant la maturation finale du follicule et l’ovulation,
soit la libération de l’ovule par le follicule dominant.
L’ovule se rendra par la suite dans la trompe de Fallope,
où a lieu la fécondation. Le reste du follicule dominant
devient alors le corps jaune ou corpus luteum. Le pic de
LH stimule le corps jaune à sécréter de la progestérone,
qui agit au niveau de l’endomètre pour permettre l’im-
plantation de l’embryon et le maintien de la grossesse. La
progestérone inhibe aussi la libération de GnRH, de
FSH et de LH, afin de prévenir le développement
d’autres follicules.
S’il y a grossesse, l’hormone chorionique humaine
(hCG) produite par les trophoblastes de l’embryon (pla-
centa) empêchera la dégénérescence du corps jaune afin
qu’il maintienne sa production de progestérone et
d’œstradiol jusqu’à ce que la stéroïdogenèse du placenta
soit bien établie, soit jusqu’à la 9eou la 10esemaine de
grossesse. S’il n’y a pas de fécondation, il y aura
dégénérescence du corps jaune et, par conséquent,
diminution de la production de progestérone et d’œstra-
diol, amenant la menstruation, l’arrêt de l’inhibition de la
FSH et le début d’un nouveau cycle.
Québec Pharmacie vol. 52, no5, mai 2005 307
Texte rédigé par
Jihad Kahwati,
B. Pharm., M. Sc.,
Pharmacie François
J. Coutu, et
Caroline Morin,
B. Pharm., M. Sc.,
CHU Sainte-Justine.
Texte original soumis
le 18 janvier 2005.
Texte final remis
le 21 février 2005.
Révision :
Louis Granger, MD,
FRCSC,
CHU Sainte-Justine,
Hôpital Maisonneuve-
Rosemont, départe-
ment d’obstétrique-
gynécologie de
l’Université de
Montréal,
PROCREA Cliniques.
de la MÈRE au NOURRISSON
Pour y voir plus clair dans le traitement
de l’infertilité
L’infertilité se définit par une absence de conception après un an de relations sexuelles
régulières sans utilisation de méthode contraceptive1. Au Canada, un couple sur huit connaît
des problèmes d’infertilité2. Étant donné que le nombre de consultations pour ce problème
est en augmentation et que les traitements évoluent, le pharmacien est de plus en plus
appelé à intervenir auprès de ces couples. Dans cet article, nous présenterons les principales
modalités de traitement utilisées dans le traitement de l’infertilité féminine. Nous ne dis-
cuterons pas de l’infertilité liée au partenaire masculin.
Cas clinique
Sophie, 34 ans, vient vous voir à la pharmacie avec l’ordonnance suivante :
• Éthinylœstradiol 30 mcg + désogestrel 150 mcg (MarvelonMD) 1 comprimé per os die pour 21 jours
• Leuprolide (LupronMD) 5 mg/mL : 0,1 mL S.C. die, à diminuer à 0,05 mL S.C. die lors de l’ajout de RepronexMD
• Ménotrophines (RepronexMD) 2 ampoules S.C. die pour 10 jours
• hCG 10 000 UI S.C. pour une injection
• Progestérone (PrometriumMD) 200 mg par voie intravaginale TID pour 15 jours, à poursuivre
si grossesse
Elle vous demande de lui expliquer les étapes de cette ordonnance et le rôle de chaque médicament. Elle prend
déjà une multivitamine prénatale contenant 1 mg d’acide folique une fois par jour. Elle ne prend aucun autre
médicament et ne présente pas de problème de santé particulier.
Chaire pharmaceutique
Famille Louis Boivin
Médicaments, grossesse et allaitement
Université de Montréal
Faculté de pharmacie HÔPITAL
SAINTE-JUSTINE
Pour l’amour des enfants

Étiologie de l’infertilité
L’infertilité chez la femme est
responsable de 30 % à
50 % des cas de couples infer-
tiles5. Les raisons principales
sont liées à des anomalies aux
niveaux ovarien, tubaire,
utérin ou cervical5. Dans
10 % à 20 % des cas, l’étiolo-
gie demeure inconnue5.
Les anomalies ovariennes
représentent de 30 % à
40 % des causes d’infertilité
chez la femme5,6. Tout élé-
ment influant sur l’axe hypo-
thalamo-hypophyso-ovarien
pourra affecter la sécrétion de
GnRH, de LH et de FSH.
Une hyperprolactinémie, un
changement de poids majeur,
l’exercice physique intense,
une hypothyroïdie et certains
médicaments peuvent af-
fecter l’axe4,5.
De plus en plus de
femmes décident de reporter
la grossesse à un âge plus
avancé, ce qui entraîne une
augmentation de la préva-
lence des couples infertiles. Six pour cent des femmes de
20 à 24 ans sont incapables de concevoir, alors que ce pro-
blème atteint 30 % des femmes âgées de 35 à 39 ans7. Cette
augmentation de l’infertilité avec l’âge serait liée à des
anomalies au niveau des ovules, mais surtout à une diminu-
tion de la réserve ovarienne8.
Le syndrome des ovaires polykystiques se caractérise par
des cycles anovulatoires, une oligoménorrhée depuis la
ménarche en excluant les années d’utilisation de contracep-
tifs oraux (de 50 % à 90 % des cas), une obésité (de 40 %
à 60 % des cas), un hyperandrogénisme clinique (hir-
sutisme, acné ou alopécie frontale) et/ou biochimique, et
une hyperinsulinémie compensatoire à une résistance
périphérique à l’insuline (jusqu’à 80 % des cas)4,9. Cet excès
d’insuline augmente la sécrétion d’androgènes, influe sur
l’axe hypothalamo-hypophysaire et affecte l’ovulation9. De
55 % à 75 % de ces femmes ont des problèmes d’infertilité9.
Toute anomalie au niveau des trompes de Fallope peut
aussi entraîner des difficultés de conception4,5. Les infections
pelviennes inflammatoires représentent la cause la plus
fréquente d’anomalie tubaire. L’endométriose, des facteurs
péritonéaux tels des adhérences, une cervicite chronique ou
des changements, quoique rares, dans la qualité du mucus
cervical peuvent aussi affecter la fécondité.
Le traitement
On doit suggérer certaines mesures non pharmacologiques
lorsqu’elles sont indiquées4,5. La perte de poids en cas
d’obésité, la diminution du stress et le report de régimes
amaigrissants sévères sont des exemples. L’hypothyroïdie,
ou tout autre état contribuant à l’infertilité, doit être cor-
rigée. Les patientes présentant un problème d’infertilité
devraient, si possible, s’abstenir de prendre des anti-inflam-
matoires non stéroïdiens autour de la période de l’ovulation
puisque les prostaglandines sont nécessaires à la libération
de l’ovule par le follicule dominant et à l’implantation de
l’embryon au niveau de l’endomètre4,10. Par mesure de pru-
dence, on doit éviter les médicaments pouvant amener une
hyperprolactinémie, telles le métoclopramide, la dompéri-
done et les phénothiazines4. Enfin, certains lubrifiants
vaginaux peuvent affecter la motilité des spermatozoïdes5.
Nous verrons, dans un premier temps, les médicaments
utilisés pour induire ou stimuler l’ovulation et, dans un
deuxième temps, les différents médicaments utilisés lors des
techniques de reproduction assistée, dont les étapes sont
présentées au tableau I. On propose les techniques de
reproduction assistée au couple lors d’infertilité liée à des
problèmes au niveau des trompes de Fallope, d’infertilité
masculine grave, d’infertilité inexpliquée ou d’échec aux
autres méthodes. L’insémination artificielle est une autre
technique qui consiste à déposer du sperme lavé (où seule-
ment les spermatozoïdes de bonne qualité sont conservés)
à l’intérieur de la cavité utérine à l’aide d’un petit cathéter.
On l’utilise lors d’infertilité masculine ou d’infertilité inex-
pliquée. Elle peut aussi être associée à des médicaments qui
induisent ou stimulent l’ovulation. Au tableau II figurent
les principaux médicaments utilisés dans le traitement de
l’infertilité.
Les médicaments qui induisent ou stimulent
l’ovulation
On parle d’induction de l’ovulation quand une patiente
n’ovule pas régulièrement et de stimulation de l’ovulation
quand la patiente ovule régulièrement et ne tombe pas
enceinte (infertilité inexpliquée). Ces médicaments sont
généralement utilisés seuls, mais on peut parfois les associer
à l’hCG ou aux gonadotrophines.
Le clomiphène
Le clomiphène est le médicament de premier recours pour
induire ou stimuler l’ovulation. En se liant aux récepteurs
œstrogéniques au niveau de l’hypothalamus et de l’hy-
pophyse, il bloque la rétroaction négative de l’œstrogène
endogène, ce qui amène une augmentation compensatoire
de la sécrétion des gonadotrophines endogènes (FSH, LH),
favorisant ainsi le recrutement et la croissance folliculaires11.
Pour qu’il soit efficace, il faut absolument que l’axe hypo-
thalamo-hypophyso-ovarien soit fonctionnel. Le taux
d’ovulation est d’environ 80 %11. L’effet antiœstrogénique
au niveau de la muqueuse du col utérin et de l’endomètre
et sa demi-vie de cinq jours pourraient nuire à l’implanta-
tion de l’embryon. Ce mécanisme est controversé dans la
documentation médicale, mais il pourrait expliquer que
seulement 70 % à 75 % des femmes ayant une ovulation
sous clomiphène ont une grossesse11,12.
308 Québec Pharmacie vol. 52, no5, mai 2005
de la MÈRE au NOURRISSON
Six pour cent
des femmes de
20 à 24 ans
sont incapables
de concevoir,
alors que
ce problème
atteint 30 % des
femmes âgées
de 35 à 39 ans7.
LLééggeennddee:: E2: œstradiol; FSH : hormone folliculo-stimu-
lante; LH : hormone lutéinisante; M : menstruation; P: pro-
gestérone. Adapté avec la permission de la référence 3.
Figure 1

Pour y voir plus clair dans le traitement de l’infertilité
Québec Pharmacie vol. 52, no5, mai 2005 309
On débute le traitement de cinq jours au jour 3 à 5 du
cycle et l’ovulation devrait avoir lieu de 5 à 10 jours après
la dernière dose4,5,11. Le fait de débuter au jour 3 par rapport
au jour 5 présente l’avantage de limiter les effets
antiœstrogéniques au niveau de l’endomètre et du mucus
cervical, et d’intervenir dans un meilleur temps pour le
recrutement des follicules primordiaux. S’il n’y a pas de
grossesse, on reprend la médication au cycle suivant. S’il n’y
a pas eu de conception après six cycles, on doit envisager
une autre option de traitement. L’ovulation est confirmée
par le dosage urinaire de la LH, le dosage sérique de proges-
térone vers le jour 21 ou, encore, en confirmant la dispari-
tion du follicule dominant à l’échographie. Puisque le
clomiphène peut augmenter la température basale, la
mesure de cette dernière n’est pas un indicateur fiable d’ovu-
lation. Dans des cas complexes d’induction de l’ovulation,
on peut utiliser l’hCG pour déclencher la ponte de l’ovule.
Les effets indésirables comprennent les bouffées de
chaleur (11 %), les troubles visuels (2 %) tels que des sco-
tomes, une vision floue ou une photosensibilité, les
douleurs abdominales, la mastalgie et le syndrome d’hyper-
stimulation ovarienne habituellement léger4,5,11. Les trou-
bles visuels sont généralement réversibles, mais quelques
cas ont résulté en des symptômes persistants ou des neu-
ropathies optiques11. Ainsi, on recommande l’arrêt du
clomiphène si des troubles visuels surviennent. Une
grossesse multiple est également possible dans 5 % à 12 %
des cas, découlant du recrutement de plusieurs follicules4,5.
Le létrozole
Le létrozole est un inhibiteur de l’aromatase, l’enzyme
responsable de la transformation des androgènes en
œstrogènes. Ce mécanisme permet de lever l’inhibition de
la libération de GnRH, de FSH et de LH. Quelques études
ont montré qu’il avait une efficacité similaire à celle du
clomiphène, mais, pour l’instant, le létrozole demeure un
traitement de deuxième recours13-15. Par rapport au
clomiphène, les avantages de ce médicament sont une
demi-vie plus courte (deux jours), une absence d’effets
antiœstrogéniques au niveau de l’endomètre, moins d’effets
indésirables et moins de risque de grossesse multiple15.
D’autres études sont nécessaires pour déterminer la poso-
logie optimale du létrozole pour cette utilisation.
Le tamoxifène
On a montré que l’efficacité du tamoxifène est similaire à
celle du clomiphène pour les taux d’ovulation et de
grossesse16. Son mécanisme d’action serait similaire à celui
du clomiphène. On l’utilise rarement puisque son efficacité
et son innocuité sont moins bien attestées.
Les médicaments utilisés lors des techniques
de reproduction assistée
Les gonadotrophines
On administre les gonadotrophines (FSH, LH) afin de
favoriser le recrutement et la maturation de plusieurs fol-
licules. La fonction ovarienne doit être adéquate afin de
répondre normalement à l’action de la FSH et de la LH.
Les gonadotrophines utilisées en pratique sont les
ménotrophines et des gonadotrophines issues de la tech-
nologie de l’ADN recombinant.
Les ménotrophines proviennent de l’urine de femmes
ménopausées et elles contiennent de la FSH et de LH. Vu
leur provenance, il existe une certaine variation d’un lot à
l’autre, elles présentent un faible risque allergène et le pro-
duit peut être en rupture d’approvisionnement. Les
gonadotrophines provenant de la technique de l’ADN
recombinant limitent ces inconvénients, mais elles sont
plus coûteuses. Ces dernières contiennent seulement de la
FSH, ce qui peut représenter un avantage chez certaines
patientes puisque la LH peut amener une maturation trop
rapide des follicules si des quantités significatives sont
présentes tout le long de la phase folliculaire4. L’absence de
LH peut être un avantage, entre autres, pour les patientes
ayant un syndrome des ovaires polykystiques, puisque ces
femmes ont déjà un ratio LH/FSH élevé dans 60 % des cas9.
La posologie varie selon la technique de reproduction
assistée utilisée. À titre d’exemple, on pourrait débuter les
injections de gonadotrophines au jour 3 ou 4 du cycle et
poursuivre jusqu’à l’administration d’hCG4,5. Elles peuvent
aussi être utilisées lors d’induction d’ovulation. Les effets
indésirables incluent une réaction allergique, surtout à la
suite de l’utilisation des ménotrophines, une mastalgie, une
réaction fébrile, des nausées, des vomissements, de la diar-
rhée, des douleurs abdominales et le syndrome d’hypersti-
mulation ovarienne4,5.
La gonadotrophine chorionique (humaine) (hCG)
L’hCG est une molécule dont la structure et l’activité sont
1) Suppression ovarienne :
• Contraceptif oral combiné pendant 14 à 21 jours.
• Un agoniste de la GnRH est débuté après le contraceptif oral et poursuivi
pendant 14 jours.
2) Stimulation ovarienne :
• Lorsque les concentrations d’œstradiol sont suffisamment basses,
on débute l’administration des gonadotrophines.
• L’agoniste de GnRH est poursuivi à dose réduite pendant 7 à 12 jours
additionnels.
3) Déclenchement de l’ovulation :
• Lorsque les follicules sont en nombre suffisant et que le diamètre des plus
gros follicules est de 19 à 22 mm, l’hCG est administrée en une dose unique.
4) Prélèvement d’ovule :
• De 34 à 36 heures après l’hCG.
• Incubation de l’ovule avec le sperme (fertilisation in vitro).
5) Support lutéal :
• Deux jours après le prélèvement d’ovule, on débute l’administration
de la progestérone.
6) Transfert d’embryon :
• De trois à cinq jours après le prélèvement d’ovule, on transfère de un
à trois embryons, le plus souvent au niveau utérin.
7) Test de grossesse :
• Effectué deux semaines après le transfert d’embryon. Si le résultat
est positif, on poursuit l’administration de la progestérone pendant
8 à 10 semaines additionnelles.
Tableau I : Techniques de reproduction assistée :
exemple de protocole4,5

310 Québec Pharmacie vol. 52, no5, mai 2005
de la MÈRE au NOURRISSON
semblables à celles de la LH, mais avec un temps de demi-vie
plus long. On l’utilise en dose unique pour finaliser la matu-
ration des follicules et déclencher l’ovulation4,5. Les effets
indésirables les plus fréquents sont les céphalées, l’irritabilité,
la fatigue, la douleur au point d’injection et, plus rarement,
une rétention liquidienne4,5. L’hCG provient de l’urine de
femmes enceintes, mais une nouvelle forme d’hCG issue de
la technologie de l’ADN recombinant (OvidrelMD) a été com-
mercialisée depuis peu.
Les agonistes de la gonadolibérine (GnRH)
On utilise ces médicaments pour diminuer la libération de
gonadotrophines et prévenir ainsi un pic de LH prématuré et
améliorer la qualité de l’ovule. Il y a une augmentation de la
libération de LH et de FSH au début du traitement, mais,
après une administration soutenue, les récepteurs hypophy-
saires sont désensibilisés et il y a diminution de la libération
des gonadotrophines4,5. En conséquence, il se produit une
diminution des concentrations sériques d’œstradiol, puis une
désensibilisation ovarienne.
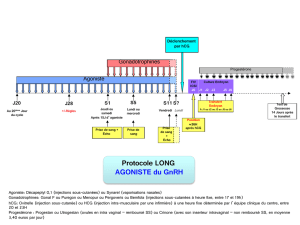
On débute leur administration 14 à 21 jours après avoir
introduit les contraceptifs oraux ou au jour 1 du cycle où les
techniques de reproduction assistée seront utilisées4,5. On
obtient la suppression de la fonction ovarienne après environ
14 jours de traitement4,5. Lorsque les concentrations d’œstra-
diol sont suffisamment basses, on peut débuter l’admi-
nistration des gonadotrophines. Toutefois, on ne cesse pas
l’agoniste de GnRH, mais sa dose est diminuée et on le pour-
suit jusqu’à l’administration de l’hCG. Les effets indésirables
pouvant survenir après l’augmentation initiale de FSH et de
LH comprennent des saignements vaginaux et une douleur
pelvienne. Il y a aussi un risque d’environ 15 % de dévelop-
per des kystes ovariens. Par la suite, après la diminution
d’œstrogènes, la femme pourra avoir des céphalées, des bouf-
fées de chaleur et une sécheresse vaginale4,5.
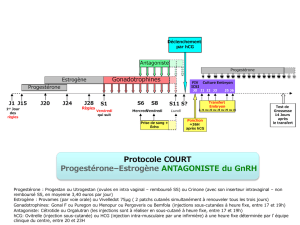
Les antagonistes de GnRH
On utilise ces médicaments pour les mêmes raisons que les
agonistes de GnRH, sans avoir d’effet stimulant initial sur
la libération de LH et de FSH. Ainsi, on les administre
après l’introduction des gonadotrophines4,5. Ces agents ont
été moins étudiés et utilisés en clinique, mais ils représen-
tent des options de traitement prometteuses pour l’avenir.
Les contraceptifs oraux
On utilise les contraceptifs oraux combinés monophasiques
pendant une période de 14 à 21 jours avant la suppression
ovarienne, afin d’améliorer la désensibilisation ovarienne et
de permettre une flexibilité dans la planification des cycles
de reproduction. Ils permettent aussi de diminuer l’inci-
dence de la formation de kystes ovariens observés avec les
agonistes de la GnRH.
La progestérone
L’utilisation des gonadotrophines et des agonistes de
GnRH peut rendre la phase lutéale plus courte et l’en-
domètre moins favorable à l’implantation embryonnaire.
On utilise la progestérone pour mieux préparer l’endomètre
et favoriser le maintien de la phase lutéale. On débute son
administration 2 jours après le prélèvement d’ovule, on la
poursuit pendant 2 semaines, puis pendant 8 à 10 semaines
additionnelles si le test de grossesse est positif4,5.
Les effets indésirables liés aux techniques
de reproduction assistée
Le syndrome d’hyperstimulation ovarienne est un effet
indésirable exigeant un suivi particulier17. On l’associe
surtout à l’administration des gonadotrophines exogènes
et à une augmentation de la taille des follicules et de la
perméabilité capillaire. Les symptômes sont souvent
légers, mais ils peuvent progresser jusqu’à une forme grave
dans 1 % à 3 % des cas. Lors de manifestations légères, les
patientes présentent des douleurs abdominales, des
nausées, des vomissements ou des diarrhées. Une ascite,
un gain de poids rapide, une hypovolémie, des déséqui-
libres hydroélectrolytiques et un syndrome de détresse res-
piratoire peuvent aussi accompagner les cas les plus
graves. Les symptômes apparaissent habituellement de
3 à 10 jours après l’ovulation. Il faut adresser rapidement
la patiente à son médecin traitant si l’on soupçonne ce
syndrome. Pour le prévenir, il est possible de limiter le
nombre de follicules recrutés, de diminuer de moitié la
dose d’hCG et/ou de retarder son administration jusqu’à
ce que les concentrations d’œstradiol soient plus faibles
ou, encore, de reporter l’implantation de l’embryon dans
un prochain cycle naturel. Les naissances multiples sont
une autre conséquence des traitements d’infertilité. Dans
le cas des techniques de reproduction assistée, elles peu-
vent atteindre 25 %, la majorité étant des grossesses
gémellaires5.
Les autres médicaments
La metformine
On utilise la metformine chez les femmes ayant un syn-
drome des ovaires polykystiques, afin de diminuer l’hyper-
insulinémie, renversant ainsi l’excès de production d’an-
drogènes et de LH, et restaurant les cycles ovulatoires. Les
posologies utilisées dans les études sont de 500 mg per os
trois fois par jour ou de 850 mg per os deux fois par jour,
pris de façon continue5. S’il n’y a toujours pas conception
après trois mois, on peut envisager l’ajout de clomiphène.
Comme il y a un risque d’avortement spontané chez ces
femmes, on doit poursuivre la metformine s’il y a
grossesse. On la cesse habituellement à la fin du premier
trimestre, bien que dans certaines études, on l’ait pour-
suivie pendant toute la grossesse.
La bromocriptine
La bromocriptine est un agoniste dopaminergique utilisé
lors d’hyperprolactinémie. La posologie de départ est de
1,25 mg per os une fois par jour, puis elle est augmentée
selon la prolactinémie de la patiente5. S’il n’y a pas eu de
conception après trois mois, on peut associer le
clomiphène ou les gonadotrophines à la bromocriptine.
On la cesse lorsqu’une grossesse est confirmée.

Pour y voir plus clair dans le traitement de l’infertilité
Québec Pharmacie vol. 52, no5, mai 2005 311
Tableau II : Les principaux médicaments utilisés dans le traitement de l’infertilité féminine
Nom, formes pharmaceutiques et posologie4,5 Place dans le traitement et commentaires4,5
Médicaments pour induire ou stimuler l’ovulation
Clomiphène (ClomidMD, SeropheneMD), comprimé de 50 mg18
• 50 mg po die pendant 5 jours, à débuter au jour 3 à 5 du cycle. En l’absence
d’ovulation, augmenter la dose de 50 mg par jour à chaque cycle
(max : 250 mg par jour).
Utilisé seul ou en association avec l’insémination
intra-utérine.
Létrozole (FemaraMD), comprimé de 2,5 mg18
• 2,5 mg à 5 mg po die pendant 5 jours, à débuter au jour 3 du cycle.
Les gonadotrophines
Ménotrophines, source urinaire (RepronexMD), fiole de 75 UI de FSH + 75 UI de LH18
• Poudre à reconstituer. Conserver à la température de la pièce. Croissance et maturation de plusieurs follicules
ovariens.
Utilisé seul (lors d’échec au clomiphène ou au
létrozole) ou associé à l’insémination intra-utérine
ou les techniques de reproduction assistée.
Dose de départ généralement de 75 à 150 UI die,
S.C. ou I.M., à débuter au jour 3 ou 4 du cycle.
Poursuivre jusqu’à ce que les concentrations
sériques d’œstradiol, le nombre et la taille des
follicules soient adéquats (généralement pour
un maximum de 12 jours de traitement).
La posologie varie selon ces paramètres.
Produits recombinants
Follitrophine alpha (Gonal-FMD)18,19
• Poudre à reconstituer. Conserver à la température de la pièce.
• Seringues de 75 ou 450 UI de FSH.
• Fiole multidoses de 1050 UI de FSH : stable 28 jours après reconstitution
Follitrophine bêta (PuregonMD)18.
• Prêt à l’administration. Conserver au réfrigérateur. Stable 3 mois à la tempéra-
ture de la pièce.
• Cartouches de 300 UI ou de 600 UI de FSH pour administration avec le Puregon
PenMD (stylo injecteur), stable 28 jours après perforation.
• Fioles de 50 UI ou 100 UI de FSH.
Gonadotrophine chorionique (humaine) (hCG)
hCG, source urinaire (Gonadotrophine chorioniqueMD), fiole de 10 000 UI20
• Poudre à reconstituer. Conserver à la température de la pièce.
• 10 000 UI S.C. pour une dose.
Maturation finale du follicule dominant et ponte
de l’ovule.
Lors d’utilisation associée au clomiphène :
administration de 3 à 4 jours après la dernière
dose de clomiphène.
Techniques de reproduction assistée : administra-
tion lorsque le follicule dominant a un diamètre
de 19 à 22 mm.
hCG recombinant (OvidrelMD), seringue préremplie de 250 mcg19
• Conserver au réfrigérateur. Stable 30 jours à la température de la pièce.
• 250 mcg S.C. pour une dose.
Agonistes de la GnRH
Buséréline (SuprefactMD), fiole multidoses de 5,5 mg (1 mg/mL)18
• Prêt à l’administration. Conserver à la température de la pièce.
• 500 mcg S.C. die jusqu’aux gonadotrophines, puis 200 mcg S.C. die.
Prévient un pic de LH prématuré.
Doit être débuté pendant le cycle précédent ou au
jour 1 du cycle où les techniques de reproduction
assistée seront utilisées.
Leuprolide (LupronMD), fiole multidoses de 14 mg (5 mg/mL)18
• Prêt à l’administration. Conserver au réfrigérateur.
• 500 mcg S.C. die jusqu’aux gonadotrophines, puis 250 mcg S.C. die.
Nafaréline (SynarelMD) (200 mcg/vaporisation, 60 vaporisations par inhalateur)18
• Conserver à la température de la pièce.
Antagonistes de GnRH
Cétrorélix (CetrotideMD), fioles de 250 mcg ou 3 mg18
• Poudre à reconstituer. Conserver au réfrigérateur ou à la température de la pièce.
• 250 mcg S.C. die : À débuter au jour 5 du cycle, à poursuivre jusqu’à hCG OU
3 mg S.C. en une seule dose au jour 7 du cycle.
Prévient un pic de LH prématuré (utilisé à la place
de l’agoniste de GnRH). Ils n’amènent pas
d’augmentation initiale de FSH et de LH.
Pour la dose de 3 mg, si l’hCG n’est pas
administrée 4 jours plus tard, il faut administrer
250 mcg S.C. die. Maximum de 30 heures entre
la dernière dose de 250 mcg et l’hCG.18
Ganirelix (OrgalutranMD), seringue préremplie de 250 mcg18
• Conserver à la température de la pièce.
• 250 mcg S.C. die. À débuter au jour 5 du cycle, à poursuivre jusqu’à hCG.
Progestérone
Progestérone pour injection, fiole de 500 mg (50 mg/mL)18
• Prêt à l’administration. Conserver à la température de la pièce.
• 50 mg I.M. die.
Maintien de la phase lutéale.
Débuter 2 jours après le prélèvement d’ovule.
Cesser si le test de grossesse est négatif.
Poursuivre pour 8 à 10 semaines additionnelles
si le test de grossesse est positif.
Progestérone micronisée (PrometriumMD), capsule de 100 mg
• 200 mg intravaginale TID.
Progestérone gel vaginal (CrinoneMD), gel 8 %18
• 1 application (90 mg) intravaginale die.
 6
6
1
/
6
100%