•Couv.1 2009-2

42
Bull. Soc. Vét. Prat. de France, avril/mai/juin 2009, T. 93, no2
Communication
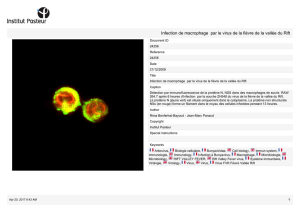
La Fièvre de la Vallée du Rift
menace-t-elle l’Europe ?
Is Rift Valley fever a threat for Europe ?
par Jean-Lou Marié
Secteur vétérinaire de Marseille, Caserne Rendu,
35 boulevard Schlœsing, BP 30182, 13276 Marseille Cedex 9 ([email protected])
et Bernard Davoust
Direction régionale du service de santé des armées de Toulon,
BP 20549, 83041 Toulon Cedex 9, France ([email protected])
RÉSUMÉ
La fièvre de la Vallée du Rift est une arbovirose à l’origine d’épizooties et d’épidémies,
essentiellement en Afrique subsaharienne et en Égypte. La propagation de la maladie à la
Péninsule arabique en 2000 pose la question d’une extension à l’Europe. D’autres arboviroses
comme la fièvre catarrhale ovine en Europe et le West Nile aux États-Unis, ont démontré leur
capacité à émerger dans de nouvelles régions. L’analyse des causes d’apparition des foyers passés
de fièvre de la Vallée du Rift et l’examen des différents modes possibles de transfert de l’agent,
conduisent à considérer comme hautement probable l’introduction du virus en Europe, à une
échéance impossible à évaluer. Dès lors, il est impératif de préparer cet événement et de faire
preuve d’une grande vigilance afin de détecter précocement l’introduction du virus et de mettre
en œuvre les actions de lutte appropriées.
Mots-clés
fièvre de la Vallée du Rift - émergence - arbovirose - réchauffement climatique - mondialisation - Europe

Introduction
Au cours de la dernière décennie, des
maladies infectieuses et parasitaires ont
émergé dans de nouvelles régions du
monde, principalement sous l’effet de la
mondialisation qui accroît les mouvements de
personnes et d’animaux et les échanges de den-
rées et de marchandises mais aussi sous l’effet du
réchauffement climatique qui influe sur la biologie
des arthropodes vecteurs.
L’introduction de la fièvre catarrhale ovine dans le
nord de l’Europe en 2006 et sa diffusion explosive
ultérieure dans plusieurs pays démontre la capa-
cité pour certaines arboviroses connues de longue
date, de s’implanter puis de se propager dans des
régions nouvelles. L’introduction du virus du West
Nile à New-York en 1999 et son extension dra-
matique dans une grande partie du territoire des
États-Unis illustre également la capacité d’émer-
gence des arboviroses dans l’espace.
La fièvre de la Vallée du Rift (FVR) est une arbo-
virose zoonotique qui sévit dans une grande partie
de l’Afrique subsaharienne, en Égypte et dans la
Péninsule arabique. En 2000, la première appa-
rition de foyers à l’extérieur du continent africain,
en Arabie Saoudite et au Yémen, a démontré la
capacité de la FVR à se propager à d’autres conti-
nents.
Une étude de la Food and Agriculture Organi-
zation (FAO) a montré que la FVR fait partie des
principales maladies animales susceptibles de tra-
verser les frontières, avec la fièvre aphteuse et
l’influenza aviaire hautement pathogène (5). En
France, un groupe d’experts de l’Agence française
de sécurité sanitaire des aliments (AFSSA) a
identifié prioritairement six maladies susceptibles
d’impacter significativement la santé animale, de
par l’intensification des échanges mondiaux et le
réchauffement climatique. Il s’agit de la fièvre
catarrhale ovine, de la FVR, de l’infection à virus
West Nile, de la leishmaniose viscérale, de la lepto-
spirose et de la peste équine (6).
Rappels sur cette arbovirose sévère
La FVR a pour agent étiologique un virus à ARN du
genre Phlebovirus et de la famille des Bunyavi-
ridae.
La maladie touche essentiellement les ovins,
bovins, caprins et camélidés qui sont aussi les
principales espèces présentes dans les zones
d’endémie. La maladie se traduit par de la fièvre,
une hépatite et un taux d’avortement élevé (10). La
mortalité peut atteindre 30 % chez les adultes et
100 % chez les jeunes. Dans les cas moins sévères,
les animaux présentent une conjonctivite, des
écoulements nasaux, de l’asthénie et des baisses
de production laitière.
La plupart des cas humains sont bénins (syndrome
pseudo-grippal) mais des formes graves peuvent
survenir : atteintes oculaires (0,5-2 % des cas),
méningoencéphalites (moins de 1 %) conduisant
43
Key word
Rift Valley fever - emergence - arbovirose - global warming - globalization - Europe
SUMMARY
Rift Valley fever is an arbovirose responsible for epizootics and epidemics, mainly in sub-
Saharan Africa and Egypt. The spreading of the disease to the Arabian peninsula in 2000,
raises the question of a further extension to Europe. Other arboviroses such as Bluetongue in
Europe and West Nile in the USA, have demonstrated their ability to emerge in new areas. The
analysis of past Rift Valley fever outbreaks and the study of the potential route of transfer, make
the introduction of the virus in Europe highly probable, although it is not possible to predict
when it will occur. Consequently, it is necessary to prepare this event and to be aware enough to
make an early detection of the virus once introduced, in order to implement adequate control
measures.

parfois à la mort ou laissant des séquelles ner-
veuses et fièvres hémorragiques (moins de 1 %).
La transmission de la FVR au sein des populations
animales est essentiellement vectorielle. De nom-
breuses espèces de moustiques ont une compé-
tence vectorielle, notamment Aedes, Culex,
Mansonia, Anopheles et Eretmapodites (11). En
outre, la maladie peut être transmise mécanique-
ment par des culicoïdés et des mouches hémato-
phages (12), notamment à la faveur de repas
sanguins interrompus. Comme la virémie est géné-
ralement élevée chez les animaux, l’infection des
vecteurs est facilitée et l’amplification virale entre
les ruminants et les arthropodes peut se produire.
La transmission à l’homme survient principalement
par contact avec du sang, des tissus, produits de
sécrétion et d’excrétion d’animaux infectés. Les
aérosols générés lors de l’abattage rituel sont
également contaminants (10). La maladie touche
essentiellement les personnes qui entretiennent
des contacts étroits avec les ruminants, comme les
éleveurs, les ouvriers d’abattoirs, les vétérinaires et
les personnes qui vivent à proximité des animaux.
La transmission du virus à l’homme peut éga-
lement résulter de piqûres de moustiques (11)
ainsi que de l’ingestion de lait non pasteurisé (2).
Pour le diagnostic, l’anatomopathologie des
lésions hépatiques est pathognomonique (10).
Néanmoins le diagnostic de certitude passe par la
sérologie (ELISA, séroneutralisation) ou la RT-PCR
à partir de différents organes (foie, rate, rein…) et
du sang.
La prévention des épizooties repose sur la vacci-
nation des animaux, réalisable à l’aide d’un vaccin
atténué. Il existe aussi un vaccin inactivé, utilisable
sur les femelles gestantes, mais qui nécessite deux
injections et qui s’avère plus coûteux (10). Un
vaccin humain est produit aux États-Unis et peut
être utilisé chez les personnes particulièrement
exposées (10).
Les principaux foyers au cours
de l’histoire
La maladie a été décrite sur du bétail, au Kenya, en
1912. Le virus a été identifié pour la première fois
en 1931 au cours de l’investigation de cas humains
et animaux, dans une ferme de la vallée du Grand
Rift, au Kenya (3).
Sur la figure 1 ont été positionnés les principaux
foyers de FVR qui sont survenus à ce jour. La
maladie est enzootique dans une grande partie de
l’Afrique subsaharienne et des épizooties souvent
suivies d’épidémies, surviennent périodiquement,
notamment après des précipitations abondantes
qui favorisent la pullulation des moustiques. La
persistance de l’agent étiologique entre les épizoo-
ties a pu être attribuée à la transmission verticale
du virus aux œufs de moustiques, puis au maintien
dans le sol des œufs en état de dormance, pendant
des années. À la faveur d’une pluviométrie favo-
rable, les œufs de moustiques peuvent éclore et
donner naissance à des imagos infectés, capables
d’initier un nouveau cycle épizootique (2).
En 1950, une épizootie en Afrique du Sud a provo-
qué la mort de 100 000 moutons et 500 000 avorte-
ments ovins (7).
En 1977 et 1978, un important foyer est apparu en
Égypte (18 000 cas humains, 600 décès), en rapport
avec la construction du barrage d’Assouan qui a
provoqué des inondations et des proliférations de
moustiques (2). Un second foyer est apparu 15 ans
plus tard, en 1993, probablement en rapport avec
le commerce de bétail depuis des pays africains
d’endémie (2, 10).
En Afrique de l’Est, le fardeau humain du foyer de
2006-2007 s’élève à 684 cas (dont 155 mortels) au
Kenya, 114 cas (dont 51 mortels) en Somalie et
264 cas (dont 109 mortels) en Tanzanie (7). Dans
cette partie du continent africain, il a été démontré
une forte corrélation entre une pluviométrie supé-
rieure à la moyenne et l’apparition de foyers de
FVR. Pour le Kenya, l’utilisation de données satel-
lites sur la végétation combinée avec les données
44
Figure 1 – Principaux foyers de la Fièvre de la Vallée du Rift
(adapté de P. Fromenty, 2008).

sur la température des eaux de surface des océans
Pacifique et Indien, permettent de prédire de façon
fiable, les foyers de FVR (1, 13). Ce modèle ne
s’applique néanmoins pas directement dans les
autres zones à risque pour la FVR.
En Afrique de l’Ouest, il n’existe pas de corrélation
entre l’abondance des précipitations et les foyers
de FVR (8). Dans cette région, le premier foyer
important de FVR est survenu en Mauritanie en
1987, causant 220 décès (8). En 1998, un autre
foyer a frappé le sud-est de la Mauritanie, causant
300 à 400 cas humains dont 6 décès (8).
Le foyer, qui est apparu en Arabie saoudite en
2000-2001, a touché 882 personnes et provoqué
124 décès (2). Il est fort probable que le virus ait
été introduit dès 1998, alors qu’une épizootie
majeure touchait l’Afrique de l’Est. En effet, les
souches sont génétiquement très proches, l’Arabie
Saoudite et le Yémen ont été touchés par des
foyers simultanés et des cas cliniques auraient été
rencontrés dès 1998. L’explosion de la maladie en
2000 s’explique par une pluviométrie inhabituel-
lement élevée.
Une capacité d’extension certaine
Le foyer majeur qui est apparu en Égypte en 1993,
ainsi que l’extension de la FVR à la Péninsule
arabique en 2000, résultent très probablement de
l’introduction d’animaux infectés (2, 10). Le foyer
humain et animal qui s’est déclaré en Mauritanie
en 2003 était dû à une souche proche des souches
circulant en Afrique de l’Est et en Afrique Centrale.
Il ne s’agissait donc pas d’une résurgence des
accès passés mais d’une nouvelle introduction du
virus, probablement par l’intermédiaire de mouve-
ments d’animaux ou de personnes infectées (8).
Par ailleurs, les moustiques ont une capacité à voler
sur plusieurs kilomètres ou peuvent être transportés
passivement, sur de longues distances, dans des
avions ou des bateaux (15). Le transport de mous-
tiques par le vent, sur des centaines de kilomètres,
est à l’origine de l’extension de foyers (10).
En raison du large spectre de vecteurs compétents,
la propagation du virus, à partir de son point
d’introduction, est souvent possible. Une étude
entomologique a d’ailleurs montré que des Culex
pipiens constituent des vecteurs compétents dans
le sud de la France (14). De plus, des mouches
hématophages sont capables de réaliser des
transmissions mécaniques (12).
L’introduction du virus de la FVR en Europe ne
peut être écartée. En effet, il est difficile ou impos-
sible d’agir sur les facteurs qui sont à l’origine de
l’expansion mondiale de la maladie, à savoir le
réchauffement climatique et l’accroissement des
mouvements de personnes, d’animaux et de mar-
chandises. On peut même affirmer que l’introduc-
tion de ce virus en Europe surviendra et que cet
événement n’est qu’une question de temps.
Une étape intermédiaire pour le virus pourrait être
l’atteinte d’îles de la Méditerranée comme Chypre,
ou de pays du Maghreb, qui pour le moment et de
façon étonnante, ont pu échapper à la maladie. Si
le Maroc venait à être touché, les portes de
l’Europe ne seraient plus qu’à quelques kilomètres.
La densité du transport de passagers entre le sud
de la France et les pays du Maghreb, ainsi que
l’importation clandestine d’ovins, pourraient per-
mettre un transfert de la FVR en France, depuis la
Tunisie, l’Algérie ou le Maroc.
Face à ces risques, la plus grande vigilance des
professionnels de la santé humaine et animale
s’impose, afin de pouvoir identifier le plus tôt
possible les premiers cas. L’identification précoce
des premiers cas devrait permettre de combattre
efficacement la maladie en mettant en place les
mesures suivantes : surveillance de l’infection sur
les populations humaines et animales, restriction
des mouvements d’animaux sensibles, information
de la population et des personnes à risque, lutte
anti-vectorielle, vaccination des troupeaux in-
demnes.
Habituellement, les cas humains sont précédés de
cas animaux. En cas d’introduction en Europe de
la FVR, il est probable que le diagnostic soit
d’abord réalisé sur des animaux. L’exposition
d’animaux naïfs, au plan immunologique au virus
de la FVR, devrait conduire à une expression cli-
nique nettement visible (10), ce qui devrait faciliter
l’identification précoce de la maladie.
L’expérience africaine montre que les cas humains
qui peuvent être nombreux, surviennent à l’occa-
sion de contacts étroits avec le sang et les tissus
d’animaux infectés. Dans nos pays européens, la
proportion de personnes qui seraient ainsi expo-
sées, est faible, ce qui devrait limiter l’impact
humain de la maladie. Il n’existe pas en effet de
contamination de personne à personne, ce qui
limite la propagation, notamment en milieu urbain.
Par contre, l’implantation du virus dans un nouvel
écosystème peut difficilement être anticipée, en
raison du nombre important de facteurs impliqués
et de leurs interrelations : densité d’espèces sen-
sibles, présence de vecteurs et données clima-
tiques. 쮿
45

46
Références bibliographiques
1. Anyamba A., Chretien J.P., Small J., Tucker C.J., Formenty
P.B., Richardson J.H., Britch S.C., Schnabel D.C., Erickson
R.L., Linthicum K.J. - Prediction of a Rift Valley fever
outbreak. Proc. Natl. Acad. Sci., 2009, 106 (3), 955-959.
2. Balkhy H.H., Memish Z.A. - Rift Valley fever : an
uninvited zoonosis in the Arabian peninsula. Int. J.
Antimicrob. Agents., 2003, 21 (2), 153-157.
3. Daubney R., Hudson J.R., Garnham P.C. - Enzootic
hepatitis or Rift Valley fever. An undescribed virus
disease of sheep, cattle and man from East Africa. J.
Pathol. Bacteriol., 1931, 34, 545-579.
4. Digoutte J.P.,Peters C.J. - General aspects of the 1987 Rift
Valley fever epidemic in Mauritania. Res. Virol., 1989,
140 (1), 27-30.
5. Domenech J., Lubroth J., Eddi C., Martin V., Roger F. -
Regional and international approaches on prevention
and control of animal transboundary and emerging
diseases. Ann. N. Y. Acad. Sci., 2006, 1081, 90-107.
6. Dufour B., Moutou F., Hattenberger A.M., Rodhain F. -
Global change: impact, management, risk approach and
health measures - the case of Europe. Rev. Sci. Tech.,
2008, 27 (2), 529-550.
7. Duse A.G. - After the floods… : the Rift Valley Fever
(RFV) outbreak, Kenya, 2006-2007. Communication
orale prononcée le 14 février 2009 lors de l’Interna-
tional Meeting on Emerging Diseases and Surveillance
(IMED), Vienne, Autriche.
8. Faye O., Diallo M., Diop D., Bezeid O.E., Bâ H., Niang M.,
Dia I., Mohamed S.A., Ndiaye K., Diallo D., Ly P.O., Diallo
B., Nabeth P., Simon F., Lô B., Diop O.M. - Rift Valley
fever outbreak with East-Central African virus lineage
in Mauritania, 2003. Emerg. Infect. Dis., 2007, 13 (7),
1016-1023.
9. Fromenty P. - Outbreaks of Rift Valley fever in Africa
2006-2007. Communication orale prononcée le 18 mars
2008 dans le cadre de la conférence internationale sur
les maladies infectieuses émergentes, Atlanta, USA.
10. Gerdes G.H. - Rift valley fever. Vet. Clin. North Am.
Food Anim. Pract., 2002, 18 (3), 549-555.
11. Gould E.A., Higgs S. - Impact of climate change and
other factors on emerging arbovirus diseases. Trans. R.
Soc. Trop. Med. Hyg., 2009, 103 (2), 109-121.
12. Hoch A.L.,Gargan T.P., Bailey C.L. - Mechanical transmis-
sion of Rift Valley fever virus by hematophagous
Diptera. Am. J. Trop. Med. Hyg., 1985, 34 (1), 188-193.
13. Linthicum K.J., Anyamba A., Tucker C.J., Kelley P.W.,
Myers M.F., Peters C.J. - Climate and satellite indicators
to forecast Rift Valley fever epidemics in Kenya.
Science, 1999, 16, 397-400.
14. Moutailler S., Krida G., Schaffner F.,Vazeille M., Failloux
A.B. - Potential vectors of Rift Valley fever virus in the
Mediterranean region. Vector Borne Zoonotic Dis.,
2008, 8 (6), 749-753.
15. Service M.W. - Mosquito (Diptera : Culicidae) dispersal
- the long and short of it. J. Med. Entomol., 1997, 34
(6) : 579-588.
1
/
5
100%