Cas clinique Cas clinique M

269
Métabolismes Hormones Diabètes et Nutrition (XI), n° 6, novembre-décembre 2007
Cas clinique
Cas clinique
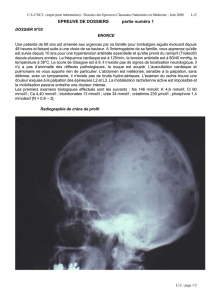
Figure 1. Scintigraphie au MIBI
99
-Tech
123
I en faveur de la présence d’un adénome parathyroïdien ectopique en position médiastinale antérieure,
à proximité de la naissance de l’aorte.
M
onsieur H., âgé de 27 ans, est “roulant” dans une
entreprise de transport. Il a récemment rencontré
le médecin du travail auquel il a confirmé n’avoir
aucun antécédent médical ou chirurgical en dehors de
l’extraction de dents de sagesse deux ans auparavant, et
signalé ne suivre aucun traitement. Lors de cette visite une
hypertension artérielle est mise en évidence. Un examen
par bandelette réactive d’un échantillon urinaire retrouve
une protéinurie. Ces deux symptômes, qui n’avaient pas
été identifiés antérieurement, conduisent monsieur H. en
consultation spécialisée d’hypertension artérielle.
Discrète asthénie et persistance de douleurs gingivales
malgré l’intervention stomatologique sont les seuls
symptômes signalés par le patient. Le poids est stable,
à 65 kg pour une taille de 168 cm. La pression artérielle
est mesurée à 150/90 mmHg et le rythme cardiaque à
116 pulsations par minute. L’examen de la cavité buccale
ne révèle aucune anomalie et le reste de l’examen clinique
est sans particularité.
La créatinine plasmatique est mesurée à 133 mmol/l et
sa clairance à 60 ml/mn. Il existe une protéinurie d’ordre
glomérulaire atteignant 2,74 g/24 heures. La kaliémie est
normale à 4,3 mmol/l et la réserve alcaline est mesurée
à 23 mmol/l. L’échographie objective des reins hyper-
échogènes, partiellement dédifférenciés, associés à de
multiples calcifications parenchymateuses médullaires
en faveur d’une néphrocalcinose.
La calcémie atteint 3,22 mmol/l et s’associe à une hypo-
phosphorémie à 0,50 mmol/l. La calciurie des 24 heures,
mesurée à 2,38 mmol, s’inscrit dans la norme mais
doit être interprétée en fonction du déficit de la fonc-
tion rénale. Le taux d’hormone parathyroïdienne atteint
455 ng/l (N : 10-55) et la vitaminémie D est normale.
Le diagnostic est donc celui d’hyperparathyroïdie
primaire d’évolution suffisamment prolongée pour avoir
été responsable d’une néphrocalcinose et d’une insuf-
fisance rénale. Cette dernière a été révélée par l’hyper-
tension artérielle associée à une protéinurie. À ce stade,
plusieurs questions se posent : quelle est la cause de
cette hyperparathyroïdie primaire ? existe-t-il un reten-
tissement extrarénal ? la maladie est-elle sous-tendue par
une anomalie génétique ? quelle attitude thérapeutique
adopter ?
L’échographie cervicale ne retrouve aucune anomalie. La
scintigraphie au MIBI-99Tech-123I oriente vers la présence
d’un adénome parathyroïdien ectopique en position
médiastinale antérieure (figure 1). À la première ques-
tion, la réponse semble être claire et correspondre à la
situation la plus fréquente en pédiatrie : adénome para-
thyroïdien sporadique. En outre, l’hyperparathyroïdie
primaire, six fois moins fréquente avant 40 ans qu’après,
est à prédominance masculine dans cette tranche d’âge :
trois garçons versus deux filles. Néanmoins, la jeunesse
du patient et l’ancienneté de l’hyperparathyroïdie (elle
doit évoluer depuis au moins dix ans pour avoir engendré
un tel retentissement rénal) doivent rendre prudent,
Comme dans le temps… hélas !
Jean-Marc Kuhn*
* Service d’endocrinologie et maladies métaboliques, CHU de Rouen.

270
Métabolismes Hormones Diabètes et Nutrition (XI), n° 6, novembre-décembre 2007
Cas clinique
Cas clinique
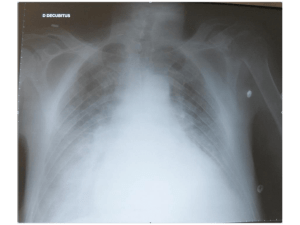
Figure 2. Aspect scanographique d’une des lésions osseuses du bas-
sin témoignant de la présence d’une “tumeur brune”, manifestation
squelettique de l’hyperparathyroïdie primaire.
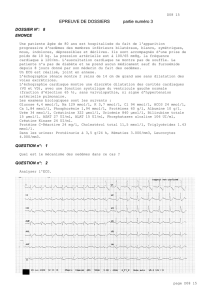
Figure 3. Résultats de la mesure des taux de PTH sériques (ng/l) sur
des prélèvements effectués au cours d’un cathétérisme sélectif des
sites veineux suivants : sous-clavières droite (SCD) et gauche (SCG),
vertébrales (VD et VG), jugulaires (JD et JG), tronc veineux innominé
(TVI), veines caves supérieure (VCS) et inférieure (VCI), oreillette
droite (OD) et abouchement sus-hépatique (VSH).
l’hypothèse d’une pathologie génétiquement déterminée
impliquant l’ensemble des parathyroïdes ne pouvant a
priori être exclue.
La réponse à la deuxième question est fournie par les
examens radiologiques. Le panoramique dentaire est
normal. La radiographie des mains ne montre pas de
signe de résorption des houppes phalangiennes. Le cliché
thoracique met en évidence un discret élargissement
des espaces acromioclaviculaires avec présence d’une
lésion lytique multiloculaire. Enfin, le scanner du bassin
retrouve des lésions osseuses multifocales (figure 2),
images de tumeurs brunes telles qu’elles étaient décrites
“dans le temps” comme un des symptômes cliniques de
l’hyperparathyroïdie primaire et qu’heureusement on ne
voit plus jamais, cette dernière étant depuis des décen-
nies diagnostiquée bien avant leur tardive apparition dans
l’évolution non traitée de la maladie.
La réponse à la troisième question, concernant le contexte
génétique, est déterminante car elle conditionne les
options thérapeutiques. L’élimination urinaire des caté-
cholamines et de leurs dérivés métaboliques est normale
chez ce patient dont la clairance de la créatinine est réduite
de 50 %. Le taux plasmatique de chromogranine A atteint
256 mg/l (N < 98). Hyperparathyroïdie primaire et insuf-
fisance rénale peuvent à elles seules expliquer l’élévation
de ce marqueur non spécifique d’une pathologie neuro-
endocrine particulière. L’échographie rénale réalisée chez
ce patient de poids normal n’a pas retrouvé d’anomalie au
niveau des aires surrénaliennes, résultat confirmé par le
scanner. La calcitoninémie est à 5 ng/l (N < 10) et l’écho-
graphie cervicale est normale. Enfin, tous les marqueurs
biologiques de la fonction hypophysaire et du pancréas
endocrine s’inscrivent dans leurs normes respectives.
Bien qu’il n’y ait pas d’antécédent familial évocateur
de néoplasie endocrinienne multiple, un prélèvement
pour étude du gène de la ménine est réalisé. À ce jour, le
résultat de la recherche de mutation du gène MEN1 n’est
pas encore connu et il n’est pas question de l’attendre
pour aborder l’étape thérapeutique, compte tenu des chif-
fres de calcémie et du retentissement déjà sévère de cette
hyperparathyroïdie primaire.
Afin de répondre à la question de l’étendue du geste
chirurgical, il est impératif de préciser si la source de
production de parathormone (PTH) est unique ou non.
La scintigraphie l’évoque, mais le contexte rend néces-
saire de disposer d’arguments supplémentaires. Dans
cet objectif un cathétérisme sélectif a été réalisé afin
de mesurer en différents points le taux plasmatique
d’hormone parathyroïdienne. Les résultats, représentés
dans la figure 3, confirment que la production de PTH
est exclusivement médiastinale et drainée dans le tronc
veineux innominé. L’intervention, réalisée sous throra-
coscopie, a permis l’ablation de cet adénome parathyroï-
dien. L’hyperparathyroïdie primaire une fois traitée, les
lésions squelettiques se recalcifieront progressivement.
A contrario, monsieur H. gardera insuffisance rénale et
hypertension artérielle comme conséquences de la néph-
rocalcinose. Même si l’on doit ne la souhaiter à personne,
une “bonne” crise de colique néphrétique aurait au moins
eu le mérite de révéler l’affection avant qu’elle n’ait,
hélas, exercé son sévère retentissement viscéral.
•
Root AW, Diamond FB Jr. Disorders of calcium metabolism in the child and
adolescent. Pediatric Endocrinology, MA Spelding Eds. Philadelphia USA:
Saunders, 2002:629-69.
1
/
2
100%