D É C O

La Lettre du Neurologue - n° 1 - vol. VII - janvier 2003
18
DÉCOUVERTES
es récepteurs dopaminergiques sont classés en deux
sous-familles, récepteurs de la sous-famille D1et D2.
Cette classification repose sur des critères fonctionnels,
pharmacologiques et d’organisation génique. Le récepteur D3de
la dopamine appartient à la sous-famille des récepteurs D2et il
est exprimé dans le cerveau, principalement dans des régions où
la dopamine est impliquée dans le contrôle des émotions, de la
motivation et dans les effets des drogues. Cette expression
restreinte aux zones limbiques du cerveau a permis de proposer
ce récepteur comme une cible pour les antipsychotiques (1).
De plus, chez le rongeur, l’administration chronique de neuro-
leptiques ne modifie pas son expression (1),ce qui est cependant
le cas du récepteur D2. L’étude de la régulation de l’expression
du récepteur D3a montré que, chez le rat normal, elle est indé-
pendante de la dopamine, alors que, chez le rat hémiparkinsonien
traité par des injections répétées de L-dopa, on observe une
induction de ce récepteur dans le striatum dénervé sous l’effet
d’une stimulation des récepteurs D1(2, 3). La régulation génique
de ce récepteur paraît donc paradoxale à double titre :
– elle est opposée à celle du récepteur D2;
– elle est indépendante en situation normale de la dopamine et
dépendante de cette amine dans un modèle pathologique. Les
études post mortem chez les patients souffrant de maladie de
Parkinson, de schizophrénie et de dépendance à la cocaïne
confirment que l’expression du récepteur D3est opposée à celle
du récepteur D2(4-6).
Les neurotrophines constituent une famille de protéines dont le
chef de file est le Nerve Growth Factor (NGF) et qui comprend
le Brain-Derived Neurotrophic Factor (BDNF), la neurotrophine 3
(NT-3) et la neurotrophine 4/5 (NT-4/5). Cette famille est définie
par une haute homologie de séquence entre ses membres et une
haute affinité pour une famille de récepteurs tyrosine kinase, les
Trk (tropomyosin-related kinase) (7). Le rôle du BDNF dans la
survie et la différenciation des neurones périphériques au cours
du développement est bien établi (7). Dans le système nerveux
central, plusieurs résultats semblent indiquer que cette neuro-
trophine pourrait agir comme un neurotransmetteur (8).
Nous avons montré que l’expression du récepteur D3était
contrôlée par le BDNF. En effet, chez des souris dont le gène du
BDNF est invalidé, la synthèse de la protéine et de l’ARNm du
récepteur D3est absente au cours du développement et à l’âge
adulte. De plus, la destruction des neurones dopaminergiques de
l’aire tegmentale ventrale entraîne une diminution de l’ARNm et
de la protéine du récepteur D3dans le noyau accumbens qui est
restaurée par l’apport exogène de BDNF. En utilisant un anta-
goniste spécifique du BDNF, nous avons montré, dans le striatum
dénervé de rats hémiparkinsoniens traités par des injections répétées
de L-dopa, que l’induction du récepteur D3était abolie et que
* Unité de neurobiologie et pharmacologie moléculaire de l’INSERM,
centre Paul-Broca, Paris, et service hospitalo-universitaire de santé mentale
et de thérapeutique, centre hospitalier Sainte-Anne, Paris.
Le BDNF contrôle la transmission dopaminergique :
implications dans la maladie de Parkinson
●O. Guillin*
L
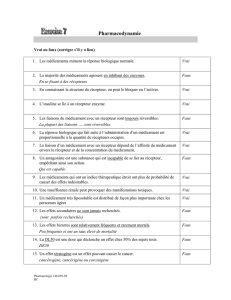
Figure. Le BDNF déclenche la sensibilisation comportementale à la L-dopa
en contrôlant l’expression du récepteur D3.
a. Signaux obtenus en hybridation in situ pour l’ARNm du récepteur D3
chez des animaux qui reçoivent une infusion continue d’IgG ou d’un
antagoniste du BDNF (IgG-TrkB) dans le striatum dénervé* pendant
7 jours. Du côté lésé, l’injection répétée de L-dopa (50mgk, I.P. pendant
5 jours) induit une surexpression du récepteur D3 (côté gauche chez
l’animal qui reçoit l’IgG). b. L’infusion de l’antagoniste du BDNF prévient
l’apparition de cette induction. c. L’injection répétée de L-dopa entraîne
une sensibilisation comportementale qui s’exprime par l’augmentation
du nombre de rotations mesuré (nombre de rotations à la première injection
vs celui à la dernière injection dans le groupe ne recevant pas d’IgG-TrkB).
L’infusion de l’antagoniste du BDNF empêche l’expression de la sensibi-
lisation comportementale à la L-dopa.
a
b4
3
2
1
0
D3receptor
Rotations
Première injection de L-dopa
Dernière injection de L-dopa
[IgG-TrkB] (µg/h) [IgG-TrkB] (µg/h)
0 0,05 0,5 0 0,05 0,5
125
100
75
50
25
0
c

La Lettre du Neurologue - n° 1 - vol. VII - janvier 2003 19
Découvertes
Découvertes
l’expression de la sensibilisation comportementale à la L-dopa
n’était plus possible. Nous avons donc conclu que le BDNF
contrôlait l’expression du récepteur D3induite par la L-dopa et
celle de la sensibilisation comportementale. Nous avons ensuite
montré que l’expression du récepteur D3,induite par la L-dopa
dans le striatum dénervé, résultait de la synthèse de BDNF dans
le cortex frontal sous l’effet d’une stimulation des récepteurs D1.
Ces résultats mettent en évidence un nouveau rôle du BDNF,
celui qui consiste à moduler la transmission dopaminergique en
contrôlant le niveau d’expression de l’un des récepteurs de ce
neurotransmetteur.
Les dyskinésies observées pendant un traitement par la L-dopa
chez les patients souffrant de maladie de Parkinson répondent
aux critères d’une sensibilisation comportementale car :
– elles n’avaient jamais été observées avant l’utilisation de ce
médicament (9) ;
– elles disparaissent lorsque l’effet du médicament cesse (9) ;
– elles apparaissent après une durée prolongée d’administration
du traitement (10). La démonstration du rôle de la surexpression
du récepteur D3dans l’expression de la sensibilisation compor-
tementale à la L-dopa indique donc qu’un traitement capable de
moduler la transmission dopaminergique, comme un agoniste
partiel et sélectif du récepteur D3,pourrait être utile dans le
traitement des dyskinésies induites par la L-dopa (11).■
RÉFÉRENCES BIBLIOGRAPHIQUES
1.
Sokoloff P et al. Molecular cloning and characterization of a novel dopamine
receptor (D3) as a target for neuroleptics. Nature 1990 ; 347 : 146-51.
2.
Lévesque D et al. A paradoxical regulation of the dopamine D3 receptor expres-
sion suggest the involvement of an anterograde factor from dopamine neurons.
Proc Natl Acad Sci USA 1995; 92 : 1719-23.
3.
Bordet R et al. Induction of dopamine D3 receptor expression as a mechanism
of behavioral sensitization to levodopa. Proc Natl Acad Sci USA 1997; 94: 3363-7.
4.
Staley JK, Mash DC. Adaptive increase in D3 dopamine receptors in the brain
award circuit of human cocaine fatalities. J Neurosci 1996 ; 16 : 6100-6.
5.
Gurevich EV et al. Mesolimbic dopamine D3 receptors and use of antipsychotics
in patients with schizophrenia. A post mortem study. Arch Gen Psychiatry 1997 ;
54 : 225-32.
6.
Ryoo HL, Pierrotti D, Joyce JN. Dopamine D3 receptor is decreased and D2
receptor is elevated in the striatum of Parkinson’s disease. Mov Disord 1998 ; 13:
788-97.
7.
Thoenen H. Neurotrophins and neuronal plasticity. Science 1995 ; 270 : 593-8.
8.
Altar CA, DiStefano PS. Neurotrophin trafficking by anterograde transport.
Trends Neurosci 1998; 21 : 433-7.
9.
Rascol O. Arguments en faveur du traitement précoce de la maldie de Parkinson
par les agonistes dopaminergiques. Rev Neurol 1999 ; 155 : 35-42.
10.
Marsden C. Parkinson’s disease. J Neurol Neurosurg Psy 1994 ; 57: 672-81.
11.
Pilla M. 11. Selective inhibition of cocaine-seeking behaviour by a partial
dopamine D3 receptor agonist. Nature 1999 ; 400 : 371-5.
Guillin O, Diaz J, Carroll P et al. BDNF controls dopamine D3receptor expression and triggers behavioural sensitization. Nature 2001 ; 411 (6833) : 86-9.
1
/
2
100%









![coursIFSIPark [Mode de compatibilité]](http://s1.studylibfr.com/store/data/004971978_1-50b10840de82468454d69d2cdfa109fd-300x300.png)