REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE

REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE
Ministère de l’Enseignement Supérieur et de la Recherche
Scientifique
Université des Sciences et de la Technologie d’Oran
-Mohamed Boudiaf-
Faculté des Sciences
Département d’Informatique
Thèse de Magister
Spécialité : Informatique
Option : Modélisation, Optimisation et Evaluation des
Performances des Systèmes (MOEPS)
Présenté par :
MERAD BADR
MÉTAHEURISTIQUES ET ANALYSE
DE DONNÉES MEDICALES
Soutenu le / /
Devant le jury composé de
Présidente: Dr. FIZAZI IZABATEN Hadria Maître de conférences A -USTO
Rapporteur : Dr. BELKADI Khaled Maître de conférences A -USTO
Examinateur: Dr. RAHAL Sid Ahmed Maître de conférences A -USTO
Examinatrice: Dr. MEKKI Rachida Maître de conférences A -USTO
2011
03/01/2012 à 9h00 à la salle de soutenances
2012

Remerciements
Je remercie tout d’abord Allah le tout puissant pour le courage et la volonté qu’il m’a
donné pour arriver à bout de ce travail.
Ce mémoire a été réalisé au sein du laboratoire «Modélisation, Optimisation et Evaluation
des Performances des Systèmes » du département informatique, Université des Sciences et de la
Technologies d’Oran.
Je tiens à remercier toutes les personnes qui ont contribué de manière directe ou indirecte
à l’aboutissement de ce travail.
J’exprime tout particulièrement mes remerciements et respects à Dr. BELKADI
Khaled, mon directeur et encadreur pour sa disponibilité. Son écoute et ses conseils qui m’ont
été toujours précieux, sa confiance, son investissement scientifique et humain ont été
essentiels à la réalisation de ce travail.
Je veux adresser tous mes remerciements à Dr. FIZAZI IZABATEN Hadria, qui m’a
fait l’honneur de présider le jury.
J’exprime également ma gratitude à Dr RAHAL Sid Ahmed et Dr. MEKKI Rachida,
qui ont accepté d’examiner ce travail et de me faire l’honneur de participer au jury.

Résumé
Dans ce travail on s'intéresse à la classification de datasets médicales en utilisant un
système immunitaire artificiel (SIA). On propose une amélioration de l'algorithme "AIRS" de
Watkins qui présente deux faiblesses: La première est le fait que l'activation de cellules
mémoires dans AIRS se fait par un seul antigène (qui peut présenter des données bruitées). Ce
mémoire présente une méthode pour activer les cellules par groupe d'antigènes homogènes.
La deuxième faiblesse est le fait qu'AIRS ne test que les cellules mémoires sollicitées par des
antigènes. On propose une méthode pour tester toutes les cellules mémoires et détruire celles
qui ne sont plus capable de défendre le système. Les résultats expérimentaux montrent une
amélioration de la précision de classification d'AIRS ainsi qu'une réduction (plus de 50%) des
données utilisées pour la classification après apprentissage.
Mots clés: Analyse de données médicales, classification, système immunitaire
artificiel, antigène, mémoire immunitaire.
Abstract
In this work we focus on the classification of medical datasets using an artificial
immune system (AIS). We propose an improvement of the Watkins’s algorithm "AIRS" who
has two weaknesses: One is the fact that the activation of memory cells in AIRS is done by a
single antigen (which may represent noisy data). This paper presents a method to activate the
cells by homogeneous antigen group. The second weakness is the fact that AIRS does not test
all memory cells. We propose a method to test all the memory cells and destroy those that are
no longer capable of defending the system. Experimental results show an improvement
classification accuracy of AIRS and reduction (over 50%) of the data used for classification
after learning.
Keywords: medical data analysis, classification, artificial immune system, antigen,
immune memory.

Table des matières
Introduction générale……………………………………………………………………….. 1
Chapitre I :Le système immunitaire naturel……………………………………….………3
I.1 Introduction....................................................................................................................4
I.2 Les différents types d'immunité .....................................................................................5
I.2.1 Le système immunitaire inné ...................................................................................5
I.2.2 Le système immunitaire adaptatif ............................................................................5
I.3 Les Organes du système Immunitaire............................................................................6
I.3.1 Organes lymphoïdes primaires.................................................................................6
I.3.1.1 Moelle osseuse (MO) ......................................................................................... 6
I.3.1.2 Thymus...............................................................................................................6
I.3.2 Les Organes lymphoïdes secondaires.......................................................................7
I.4 Les cellules du système immunitaire .............................................................................7
I..4.1 Cellules lymphoîdes (L)...........................................................................................8
I.4.1.1 Le récepteur des lymphocytes B (BCR).............................................................9
I.4.1.2 Le récepteur des lymphocytes T (TCR).............................................................9
I.5 Sélection clonale (Clonal selection)...............................................................................9
I.5.1 Activation des lymphocytes T..................................................................................9
I.5.2 Activation des lymphocytes B................................................................................10
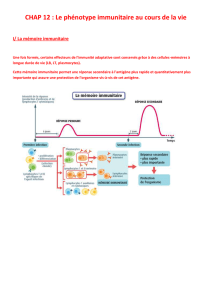
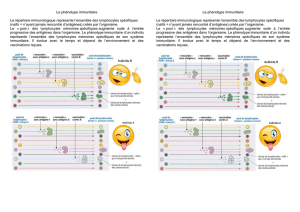
I.6 La mémoire immunitaire..............................................................................................10
I.7 La maturation de l’affinité............................................................................................11
I.8 Détection du soi et du non soi......................................................................................11
I.8.1 La sélection positive...............................................................................................11
I.8.2 La délétion clonale (sélection négative des lymphocytes B) .................................12
I.8.3 La sélection négative des lymphocytes T...............................................................12
I.9 La théorie du réseau immunitaire.................................................................................12
I.10 La théorie du danger.....................................................................................................13
I.11 Les étapes d’une réaction immunitaire.........................................................................13
I.11.1 Pénétration de l’antigène........................................................................................13
I.11.2 Réaction inflammatoire..........................................................................................14
I.11.3 La réponse immunitaire..........................................................................................14
I.11.3.1La réponse primaire..........................................................................................14

I.11.3.2Réponse secondaire et suivantes ......................................................................14
I.12 Caractéristiques du système immunitaire.....................................................................15
I.13 Conclusion....................................................................................................................16
ChapitreII: Le système immunitaire artificiel………………………...…...………...……18
II.1 Introduction..................................................................................................................19
II.2 Représentation et affinité .............................................................................................20
II.3 Les algorithmes du système immunitaire artificiel ......................................................21
II.3.1 La sélection négative..............................................................................................21
II.3.2 La sélection positive...............................................................................................22
II.3.3 Domaine d’application de la sélection négative et positive...................................22
II.3.4 La sélection clonale................................................................................................23
II.4 Les réseaux immunitaires artificiels.............................................................................24
II.5 La théorie du danger.....................................................................................................25
II.6 Les domaines d'application des AIS.............................................................................25
II.6.1 La classification......................................................................................................26
II.6.2 La sécurité des ordinateurs.....................................................................................26
II.6.3 La détection et l'élimination des virus informatiques.............................................26
II.6.4 Optimisation...........................................................................................................27
II.6.5 Robotique...............................................................................................................27
II.6.6 Autres domaines d'utilisation.................................................................................28
II.7 Conclusion....................................................................................................................28
ChapitreIII: Présentation de l'algorithme AIRS.………………………........…..…….…29
III.1 Introduction..................................................................................................................30
III.2 Définitions....................................................................................................................30
III.3 Tour de l’algorithme.....................................................................................................32
I.3.1 La phase d’initialisation .........................................................................................33
I.3.2 La phase d’Identification de la cellule mémoire et génération des ARBs .............34
I.3.3 La phase de Compétition des ressources et développement de la cellule mémoire
candidate...............................................................................................................................36
I.3.4 Introduction de la cellule mémoire.........................................................................39
I.3.5 Classification..........................................................................................................39
III.4 AIRS 2..........................................................................................................................40
III.5 Conclusion....................................................................................................................40
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
1
/
82
100%