PREMIER MÉMOIRE SUR L`ELECTRICITE

Document 1. Contamination à l’iode
« Lorsqu'un très grave accident nucléaire survient, plusieurs éléments radioactifs très nocifs (césium, strontium, gaz
rares tels le krypton et le xénon) sont susceptibles d'être rejetés dans l'atmosphère. Tous ces produits augmentant la
possibilité de mutations dans les cellules qu'ils irradient, le risque principal en cas de contamination est de développer
un cancer. A cet égard, le danger le plus grand est sans conteste celui d'une contamination par de l'iode radioactif. »
Le Monde 14.03.2011
Document 2. Lorsque l'organisme est exposé à de l'iode radioactif, la glande thyroïde l'absorbe tout comme s'il s'agissait
d'iode non radioactif. Cela augmente, bien entendu, la probabilité d'un cancer de la thyroïde. Cette éventualité est
d'autant plus grande qu'il s'agit d'isotopes à courte durée de vie, tels que 131I, aux flux radioactifs plus intenses.
L'iode ne compte pas moins de 37 isotopes, dont un seul, 127I, est stable. L'isotope 131I est utilisé en radiothérapie de
tumeurs cancéreuses et autres affections de la glande thyroïde. 123I et 125I servent à l'imagerie nucléaire des reins et de
la thyroïde, ainsi qu'à suivre l'assimilation d'iode par la thyroïde.
http://www.universalis-edu.com/encyclopedie/iode/
Document 3. L’iode 127 à la rescousse de la contamination
L'iode est un élément chimique de la série des halogènes, de symbole I et de numéro atomique 53. L'iodure de
potassium naturel est composé d'iode 127 stable. Il peut être utilisé en comprimés pour saturer temporairement la
capacité d'absorption d'iode de la thyroïde. Cela permet de bloquer pendant quelques heures la fixation éventuelle
d'iode 131 dans cette glande ; c'est notamment le cas pour se prémunir des conséquences des retombées d'iode
radioactif d'une bombe A ou d'un accident nucléaire. http://fr.wikipedia.org/wiki/Iode
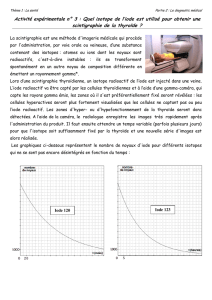
Document 4. Un spectrographe de masse est un appareil
permettant d'accélérer des cations et de les dévier plus ou
moins en fonction de leur masse. L'impact de chaque cation
sur un détecteur laisse une trace qui permet de déterminer
sa masse. On peut grâce à cet appareil observer, en cas
d'accident nucléaire, que l'iode peut être composé de
plusieurs types d'atomes qui n'ont pas la même masse.
D'après Physique-Chimie seconde, Microméga, Hatier
Questions :
1. Quel est le rôle des comprimés d'iode ?
2. L'organisme absorbe-t-il différemment l'iode
naturel et l'iode radioactif ?
3. Combien y a-t-il de protons dans le noyau d'un
atome d'iode ?
4. Trouver deux points communs et deux différences
entre l'iode 127 et l'iode 131.
5. Ecrire les symboles des noyaux d'iode 127 et 131.
6. Attribuer sur le doc 4 une trajectoire aux deux
isotopes précédents. Justifier.
7. Combien ces deux noyaux comptent-ils de
neutrons ?
Vocabulaire
- Les particules contenues dans le noyau s'appellent les
nucléons. Il en existe deux sortes : les protons et les
neutrons. Le nombre de nucléons d'un noyau est noté A.
- Le numéro atomique correspond au nombre de
protons dans le noyau. Il se note Z.
- Le proton et le neutron sont des particules de masse
voisine : 1,7.10-27 kg. Le proton possède une charge
positive alors que le neutron n'est pas chargé.
- Deux atomes sont isotopes lorsqu'ils ont le même
nombre Z de protons et des nombres N différents de
neutrons.
- Le symbole d'un noyau atomique X s'écrit
avec les lettres A et Z placées comme ceci :
X
A
Z
1
/
1
100%