Décollements de l`épithélium pigmentaire

Rétine
Images en Ophtalmologie
•
Vol. II
•
n° 4
•
octobre-novembre-décembre 2008
112
Légendes
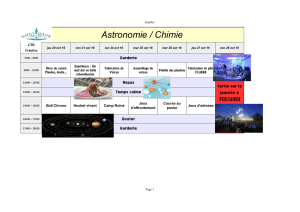
Figure 1. a. Angiographie en SLO. La fl èche
verte indique l’emplacement de la coupe et le
sens de l’OCT. Le caliper sur cette fl èche corres-
pond à la fl èche verte apparaissant sur l’OCT et
sur le graphe. b. L’OCT montre un décollement
de l’EP irrégulier fragmenté avec interruption
partielle de la limitante externe et infi ltration
de l’interface des segments internes et externes.
c. Épaisseur sur graphe de l’OCT fovéal. La ligne
verte indique l’ endroit le plus épais et corres-
pond à 597 μm. Ce scan d’OCT est fi xé comme
scan de référence. Tous les scans des examens
suivants, au cours de l’évolution passeront au
même endroit par eye tracking.
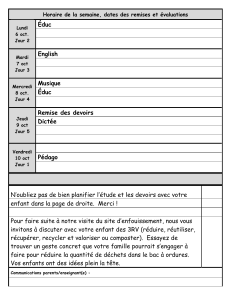
Figure 2. a. L’angiographie en SLO montre,
1 mois après la premières IVT de ranibizumab,
la disparition complète de l’hémorragie sous-
rétinienne, de la diff usion de la fl uorescéine et
un eff et fenêtre lié aux drusen et altérations
de l’EP. b. L’OCT montre un décollement de
l’EP moins marqué avec une infi ltration des
couches externes, plus localisée. Le fl uide est
en diminution en intrarétinien et a disparu en
sous-rétinien. c. Épaisseur sur graphe de l’OCT
fovéal. Une correction manuelle des lignes de
mesure peut être réalisée si des artéfacts se
présentent. La ligne verte indique l’endroit le
plus épais et correspond à 393 μm et note, en
vert et en chiff res (variation de – 206 μm), la
diminution par rapport au premier examen
avant traitement. Cette épaisseur étant
supérieure à la moyenne du fait du DEP actif
persistant, une 2e IVT est réalisée.
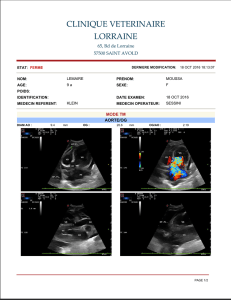
Figure 3. a. L’angiographie en SLO est d’as-
pect stable et inchangé. b. L’OCT montre la
disparition du DEP et la persistance de petits
drusen (bosselures de l’EP) et plages d’atro-
phie de l’EP localisées (disparitions de la limi-
tante externe et amincissement de l’EP). Le
fl uide est en diminution en intrarétinien et
a disparu en sous-rétinien. c. Épaisseur sur
graphe de l’OCT fovéal.
Figure 4. a. L’angiographie en SLO est
d’ aspect stable et inchangé. b. L’OCT montre
un aspect stable par rapport à l’examen
précédent. c. Épaisseur sur graphe de l’OCT
fovéal. La ligne verte indique l’endroit le plus
épais, de 299 μm (– 300 μm).
Cas clinique
Décollements
de l’épithélium pigmentaire :
les nouveaux procédés d’analyse
Pigment epithelial detachment:
new analysing and imaging ways
F. Coscas
(Centre ophtalmologique de l’Odéon, Créteil)
M. R.T., âgé de 75 ans, est adressé pour l’apparition d’une discrète baisse
d’acuité visuelle (AV) de l’œil droit avec une AV de 20/32 – score79 –
associée à des métamorphopsies depuis 8 jours. L’œil gauche présente des
drusen maculaires sans signe de complication.
Examen
L’angiographie en SLO, à la fl uorescéine
(fi gure 1a)
, montre l’apparition d’une hémor-
ragie sous-rétinienne juxtafovéale associée à une néovascularisation de type occulte
diffusant au cours de la séquence angiographique avec
pin points
et nombreux drusen.
L’angiographie en SLO, au vert d’indocyanine, ne montre pas de signe de déchirure
ni de vasculopathie polypoïdale mais un décollement de l’épithélium pigmentaire
(DEP) avec une anastomose choriorétinienne supérieure (ACR)
[1]
. L’OCT au Spec-
tralis
(fi gure 1b)
montre une importante réaction exsudative (logettes cystoïdes,
décollement séreux rétinien, fl uide intrarétinien), un épithélium pigmentaire (EP)
décollé, mais la ligne de la limitante externe est encore conservée, bien qu’épaissie,
et l’hémorragie sous-rétinienne apparaît sous l’aspect d’une hyperréfl ectivité dans
les couches internes. L’interface segments internes/ segments externes est densifi ée,
infi ltrée en avant de l’EP décollé et associée à des points hyperréfl ectifs. Cet aspect
sera à surveiller. Il n’existe pas non plus de déchirure de l’EP
(2)
. Le graphe
(fi gure 1c)
donne une épaisseur maximale à 597 μm. Aucune correction manuelle n’a été néces-
saire sur les coupes de ce patient pour enlever un éventuel artéfact. Une injection
intravitréenne d’anti-VEGF (ranibizumab 0,05 ml) a été alors effectuée.
Au premier contrôle à un mois de la première IVT, l’AV de cet œil droit est de 20/ 25,
•
associée à de moindres métamorphopsies. Il persiste encore un DEP en temporal,
des néovaisseaux en rétrofovéal, des exsudats de résorption, du fl uide, mais il y a une
nette diminution de l’épaisseur (393 μm soit – 206 μm) et de l’ensemble de la réaction
exsudative. Cette valeur est obtenue sur la même zone qu’à l’examen précédent grâce
à
l’eye tracker
du Spectralis HRA-OCT. Il est décidé d’effectuer une seconde IVT de
l’œil droit
(fi gure 2)
.
Au deuxième contrôle à deux mois du premier examen, après 2 IVT, l’AV de cet
•
œil droit de 20/ 25 – score 79 – est stable, avec disparition des métamorphopsies.
L’examen du fond d’œil met en évidence des remaniements de l’EP de type réticulé
avec migrations pigmentaires bien visibles sur le cliché en lumière rouge et des
exsudats profonds en temporal supérieur. L’angiographie en SLO, à la fl uorescéine,
objective des zones d’altérations de l’EP avec un point un peu plus hyperfl uorescent
sur onze heures au niveau de la zone vasculaire centrale, qui augmente au cours de
la séquence angiographique. Cela peut correspondre à une ACR résiduelle. L’angio-
graphie en SLO, au vert d’indocyanine, ne montre pas de lacis vasculaire visible,
mais on note en nasal inférieur une hyperfl uorescence un peu plus accentuée aux
temps tardifs. L’OCT au Spectralis montre une diminution d’épaisseur de 295 μm, soit
– 303 μm par rapport au premier examen. Les lignes de la limitante externe,

Rétine
1a
1b
1c
Thickness (μm)
Position (mm)
1 000
800
600
400
200
0
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 5,5 6,0 6,5 7,0 7,5 8,0 8,5
597
2a
2b
2c
Thickness (μm)
Position (mm)
1 000
800
600
400
200
0
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 5,5 6,0 6,5 7,0 7,5 8,0 8,5
393 (– 206)
3a
3b
3c
Thickness (μm)
Position (mm)
1 000
800
600
400
200
0
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 5,5 6,0 6,5 7,0 7,5 8,0 8,5
295 (– 303)
4a
4b
4c
Thickness (μm)
Position (mm)
1 000
800
600
400
200
0
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 5,5 6,0 6,5 7,0 7,5 8,0 8,5
299 (– 300)
Follow-up
Reference
Follow-up thinner
Follow-up thicker
Images en Ophtalmologie
•
Vol. II
•
n° 4
•
octobre-novembre-décembre 2008
113
Cas clinique

Rétine
Images en Ophtalmologie
•
Vol. II
•
n° 4
•
octobre-novembre-décembre 2008
114
Cas clinique
de l’inter face segments internes/ segments externes et de l’EP sont légèrement
irrégulières et épaissies localement. Bien qu’il soit proposé une série systématique
de 3 injections, il est décidé de ne pas réaliser la troisième IVT et d’instaurer une
surveillance à un mois
(fi gure 3)
.
Au troisième contrôle, après 2 IVT, l’AV de cet œil droit de 20/ 25 – score 79 – est stable. •
L’angiographie en SLO, à la fl uorescéine, confi rme l’absence de récidive néovasculaire
visible. L’OCT au Spectralis objective l’absence de DEP, de déchirure de l’EP, avec une
épaisseur sur la zone
trackée
de 299 μm, soit – 300 μm par rapport à l’examen initial. Cet
aspect est tout à fait satisfaisant. Aucune IVT n’est programmée et le patient sera
revu à 1 mois.
Au quatrième contrôle, quatre mois après le premier examen, 2 mois après 2 IVT,
•
l’AV de cet œil droit est remontée d’une ligne à 20/ 20 – score 84. L’angiographie en
SLO, à la fl uorescéine, objective des altérations de l’EP multiples, des plages d’atro-
phie et des drusen. Il n’existe pas, à ce jour, de réaction exsudative. L’OCT au Spec-
tralis objective la stabilité d’une rétine à plat avec un EP irrégulier associant petites
bosselures liées aux drusen, détachées de la Bruch, et la conservation sans zone
d’interruption des couches externes
(fi gure 4)
. Le traitement est fondé sur l’autosur-
veillance de chaque œil et des contrôles cliniques et paracliniques mensuels
(3)
. Le
patient est informé que, si de nouveaux signes fonctionnels (baisse d’AV ou métamor-
phopsies) apparaissaient, il serait amené à consulter en urgence.
Cet aspect illustre l’effet bénéfique d’un traitement débuté précocement dès
les premiers signes de décompensation. Il montre que le suivi précis de la zone
atteinte permet d’ajuster la thérapeutique pour limiter le nombre d’injections dans
ce cas. Les analyses, répétées grâce à l’
eye tracker
quantifi ent mieux la réaction
exsudative, et ce d’une manière totalement objective
(4, 5)
. La fi nesse de résolution
de cette nouvelle génération d’appareil permet une analyse de qualité des couches
externes (limitante externe, interface SI/ SE, EP), véritables éléments pronostiques
de ces pathologies
(3, 6)
. La tomographie en cohérence optique en domaine spec-
tral associée aux angiographies permet, par cette technologie, un suivi véritable et
aisément analysable sur une seule et même planche.
IIII
Références bibliographiques
Freund KB, Ho IV, Barbazetto IA et al. Type 3 neovascularization: the expanded spectrum of retinal
1.
angiomatous proliferation. Retina 2008;28(2):201-11.
Coscas F et al. Optical coherence tomography identifi cation of occult choroidal neovascularization
2.
in age-related macular degeneration. Am J Ophthalmol 2007;144(4):592-9.
Coscas F, Coscas G, Souied E, Soubrane G. Confocal (en face) optical coherence tomography in
3.
vascularized retinal pigment epithelium detachment. Retin Cases Brief Rep 2008;2:94-8.
Coscas G, Coscas F, Vismara S, Souied E, Soubrane G. Spectral Domain OCT in age-related macular
4.
degeneration: preliminary results with Spectralis HRA-OCT. J Fr Ophtalmol 2008;31(4):353-61.
Coscas G, Coscas F, Zourdani A. Atlas of Indocyanine green angiography, ICG angiography, and OCT
5.
correlation. Ed. Elsevier, 2004. Traduction anglaise 2005, italienne 2006.
Sakamoto A, Hangai M, Yoshimura N. Spectral-domain optical coherence tomography with multiple
6.
B-scan averaging forenhanced imaging of retinal diseases. Ophthalmology 2008;115(6):1071-8.
Pour en savoir plus…
Coscas G, Coscas F, Vismara S, Zourdani A, Li Calzi C. OCT dans la DMLA. Rapport annuel des
•
Sociétés de France. Ed. Lamy, 2008.
1
/
3
100%