TP de Physique

L’Univers
TP 11
Etude du spectre du soleil
Seconde
Objectif :
Interpréter le spectre de la lumière émise par une étoile : entités chimiques présentes dans l’atmosphère de l’étoile
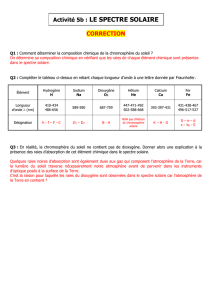
1- Documents
Document n°1 :
En 1802, un chimiste britannique, William Wollaston, observe l’absence de certaines couleurs dans le
spectre du Soleil. En 1814, à l’aide d’un spectroscope de son invention, le physicien allemand Joseph
Fraunhofer observe des raies sombres dans le spectre continu du Soleil. Il fait une mesure précise de la
position de plusieurs centaines de ces raies sombres en notant les plus intenses par des lettres.
En 1859, les physiciens et chimistes allemands Gustav Kirchhoff et Robert Bunsen mettent en évidence
qu’un gaz chaud sous basse pression émet une série de raies et que celle-ci est propre à la composition
chimique du gaz. Kirchhoff découvre ensuite que le spectre de la lumière blanche ayant traversé un gaz,
à basse pression et à basse température, présente des raies sombres aux mêmes longueurs d’onde que
celles émises par le gaz lorsqu’il est chaud. Il fait alors le parallèle entre sa découverte et le spectre de
Fraunhofer. Il en conclut que la lumière émise par la surface chaude du Soleil traverse une couche
gazeuse relativement froide, l’atmosphère solaire, et que pour certaines longueurs d’onde, les radiations
sont absorbées.
Document n°2 :
Ce document représente :
a. Les raies noires sur fond blanc correspondent aux raies noires observées par Fraunhofer, sur le
spectre du Soleil. Les principales raies d'absorption apparaissant sur cet extrait sont numérotées.
b. Les raies blanches sur fond noir correspondent aux raies émises par l'argon (élément chimique).
Ces raies, dont ont connaît les longueurs d'onde, servent de référence pour notre étude.
Document n°3 :
Un tableau renseigne sur les longueurs d'onde des radiations absorbées par certains éléments
chimiques.
H
434,0
486,1
656,3
Na
589,6
589,9
Mg
470,3
516,7
Ca
422,7
458,2
526,2
527,0
Ca2+
396,8
Fe
438,3
489,1
491,1
495,7
532,8
537,1
539,7
Ti
466,8
469,1
498,2
Mn
403,6
Ni
508,0

2- Origine de la présence de raies d'absorption dans le spectre du Soleil.
Photosphère : couche interne qui émet de la lumière blanche. Elle donne un spectre continu.
La lumière qui nous parvient a traversé la
chromosphère, donc a subit des absorptions.
Chromosphère : couche externe ou atmosphère, constituée d'éléments qui absorbent
certaines longueurs d'onde : le spectre est alors discontinu
3- Etude du spectre de l'argon.
Mesurer les distances L, en mm, entre la raie d'émission à 390 nm, qui servira de référence, et
toutes les autres raies du spectre d'émission de l'argon.
Distance L,
en mm
0
Longueur
d'onde λ,
en nm
390
A l’aide d’un tableur et sur une feuille de papier millimétré, tracez la courbe représentant la fonction f
qui à la longueur L associe la longueur d'onde λ. on peut écrire λ = f (L).
Prendre pour échelle : pour L, 1 cm ↔ 10 mm et pour λ, 1cm ↔ 10 nm
Cette courbe servira par la suite de courbe d'étalonnage.
Dans un tableur, rentrez les valeurs de la distance L et de la longueur d'onde λ ; tracez la courbe λ =
f (L), puis imprimez-la en faisant apparaître l’équation de la droite ainsi que le coefficient de
corrélation r2 ;
4- Etude du spectre du Soleil.
Mesurer les distances D, en mm, entre la raie représentée en pointillés, (qui correspond à la raie de
référence à 390 nm) et les différentes raies d'absorption apparaissant sur le sepctre visible du Soleil.
Raie n°
1
2
3
4
5
6
7
Distance D,
en mm
0
Longueur
d'onde λ, en
nm
390
Elément
chimique
Raie n°
8
9
10
11
12
13
14
15
Distance D,
en mm
Longueur
d'onde λ, en
nm
Elément
chimique
A l'aide de la courbe d'étalonnage, déduire les valeurs des longueurs d'onde correspondant aux
mesures de D. Ces longueurs d'onde correspondent aux raies absorbées.
A l'aide du doc n°3, relier chaque longueur d'onde absorbée à l'élément chimique responsable de
l'absorption.
1
/
2
100%