Acteur de la sécurité des médicaments en Europe

JEAN-MICHEL DOGNÉ
Acteur de la sécurité des
médicaments en Europe
Le professeur Jean-Michel Dogné (Département de pharmacie et NARILIS), a été
nommé à la nouvelle commission de pharmacovigilance (PRAC) de l’Agence euro-
péenne des médicaments (EMA). Un rôle et une responsabilité de taille puisque
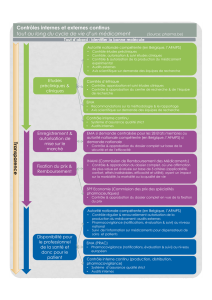
cette commission se charge du suivi de la sécurité des médicaments dès leur
demande d’autorisation de mise sur le marché. L’objectif est de favoriser un usage
optimal du médicament et d’évaluer, lorsque des effets indésirables sérieux sont
constatés, si l’utilisation du produit doit être adaptée afi
n de minimiser les risques
ou si celui-ci doit être retiré de la vente en Europe.
Quels sont les éléments qui
ont motivé votre nomination ?
Mes compétences en pharmaco-
logie et pharmacovigilance. Outre
mes recherches concernant ces
domaines, je collabore depuis plus
de cinq ans avec l’EMA et suis
expert auprès de l’Agence Fédérale
des Médicaments et des Produits
de Santé (AFMPS).
Pourquoi l’Europe a-t-elle
constitué cette nouvelle
commission ?
Au regard de l’importance grandis-
sante de la pharmacovigilance ces
dernières années et pour répondre
à la volonté d’avoir une commis-
sion totalement indépendante,
bien que complémentaire, de celle
chargée de l’autorisation de mise
sur le marché des médicaments.
La PRAC travaillera en totale
transparence et l’entièreté des
rapports des experts sera dispo-
nible sur le site Web de l’EMA,
une démarche inédite dans le
monde du médicament ! Bien
entendu on ne pourra contrôler
ce que font les firmes pharma-
ceutiques avec ces rapports, s’ils
s’en servent pour dévaloriser les
produits de leurs concurrents…
C’est aux médecins et pharma-
ciens d’être prudents quant à
l’utilisation de ces informations
et de fournir les renseignements
adéquats aux patients. De plus,
l’EMA communique directement
vers les professionnels de la santé,
notamment en leur envoyant une
lettre expliquant les risques liés à
tel médicament.
Quelles sont les raisons
de cet essor ?
Le renforcement de la pharma-
covigilance ne vient pas du fait
que nous prenons plus de médi-
caments ou qu’il y a plus de pro-
blèmes d’effets secondaires, mais
de deux facteurs. Le premier est
que nous profi tons du développe-
ment constant de techniques de
pharmacovigilance et de pharma-
coépidémiologie basées sur l’ana-
lyse de rapports d’effets indési-
rables et sur des données émanant
de patients.
Chaque patient est invité à expli-
quer aux médecins ou aux phar-
maciens les éventuels effets indé-
sirables et ces professionnels ont
le devoir de faire part de leurs
observations aux agences des
médicaments nationales qui les
rapportent à l’EMA et à l’organi-
sation mondiale de la santé (OMS).
Depuis peu, les patients des états
membres de la communauté euro-
péenne peuvent rapporter directe-
ment les effets indésirables sans
passer par les professionnels de la
santé, via le site Web de l’AFMPS.
Au total, cette récolte interna-
tionale de données permet une
analyse pointue des risques
médicamenteux.
Et le second ?
C’est la multiplication des médica-
ments d’une même classe pharma-
cothérapeutique offrant de nom-
breuses alternatives. Il est dès lors
parfois justifi é de limiter l’utilisation
de certains produits sans priver le
patient d’un accès à un traitement
tout aussi effi cace et moins dan-
gereux. Pensons par exemple aux
décisions, très médiatisés, relatives
au retrait de médicaments utilisés
dans le traitement du diabète, tel
que le mediator®. Ce retrait a in fi ne
eu un impact positif en termes de
santé publique.
En outre, il y a eu une prise de
conscience politique et publique
qu’il n’existe pas de médicaments
sans effets indésirables. Même
si, bien entendu, la
probabilité de déve-
lopper un effet indé-
sirable est souvent
faible. Ainsi, même
s’ils sont mention-
nés dans la notice
du médicament,
certains risques
graves doivent être
relativisés. Vous
avez autant de
risque de dévelop-
per certains effets
indésirables très
rares, voire mortels,
que d’être touché
par la foudre en mar-
chant dans la rue !
La question réside
dans la balance du
risque-bénéfi ce…
C’est bien là
que se situe tout
votre travail ?
En effet, si nous constatons un
problème, nous regardons si le
bénéfi ce est supérieur au risque
encouru en prenant le médica-
ment. S’il l’est, nous laissons le
médicament sur le marché et sui-
vons son utilisation, en particulier
par la population la plus concer-
née par les risques. S’il ne l’est
pas, plusieurs possibilités doivent
être envisagées pour minimiser les
risques. Il peut s’agir de nouvelles
contre-indications ou précautions
particulières d’utilisation. Par
exemple, si nous constatons qu’un
médicament entraîne un décès sur
10 000 patients traités, nous regar-
dons si l’on peut restreindre l’uti-
lisation à une certaine population
où le risque est moindre, voire
absent. Lorsque ces mesures
s’avèrent ineffi caces, le retrait du
marché doit être envisagé lors
d’une réévaluation complète du
bénéfi ce-risque du produit.
Notre commission s’intéresse plus
particulièrement aux effets indé-
sirables graves, c’est-à-dire ceux
qui ont nécessité une hospitalisa-
tion ou une prolongation de celle-
ci, ont mis la vie en danger, ont
entraîné un décès, une invalidité
ou incapacité durable ou impor-
tante ou une anomalie ou mal-
formation congénitale. Et/ou aux
effets inattendus, c’est-à-dire ceux
dont la nature, la sévérité et/ou
l’évolution ne correspond pas à ce
qui est mentionné dans le résumé
des caractéristiques du produit.
Au niveau belge, une attention
particulière est portée au rap-
port spontané des médecins et
pharmaciens sur des effets indé-
sirables survenus pour des popu-
lations sensibles (enfants, femmes
enceintes ou allaitantes, per-
sonnes âgées, insuffi sants rénaux
ou hépatiques), ou lors de l’admi-
nistration de vaccins, ou en cas
d’usage « inapproprié » ou « hors
indication » de médicaments.
La responsabilité
est donc lourde…
Tout à fait. Le PRAC joue un rôle
majeur en santé publique et pour
les firmes pharmaceutiques car
nous devons prendre une décision
objective, indépendante des pres-
sions populaires, médiatiques,
politiques, et de l’industrie phar-
maceutique elle-même. Le coût de
développement de certains médi-
caments peut atteindre le milliard
de dollars. Il est inutile de préciser
que le refus de la mise sur le mar-
ché, ou le retrait d’un produit, peut
avoir des conséquences majeures
pour les fi rmes… L’argument ne
manque pas d’être directement
ou indirectement avancé lorsqu’on
envisage une telle décision.
En outre, nous intervenons tou-
jours sur base de cas d’effets
indésirables rapportés dans des
situations dramatiques et nous
devons travailler rapidement pour
des raisons évidentes de santé
publique mais sommes tenus de
baser nos décisions sur base de
rapports robustes et complets qui
nécessitent la prise en compte de
nombreuses données.
L’aspect ‘communication’ est
donc également une diffi culté ?
Lorsqu’une décision est prise, l’exer-
cice de la communiquer est en effet
particulièrement délicat. Prenons le
cas d’une jeune fi lle en Grande-Bre-
tagne, décédée deux heures après
avoir pris le vaccin
contre le col de l’uté-
rus Cervarix®. La
presse s’est immé-
diatement emparée
de l’affaire… Fina-
lement, l’autopsie
-dont les résultats
ont été obtenus
après 48 heures- a
montré que la jeune
fille souffrait d’une
pathologie car-
diaque responsable
de son décès. Mais
entretemps, l’EMA
était sur la sellette…
La difficulté est de
faire comprendre
que la vraie vie du
médicament com-
mence avec sa mise
sur le marché, donc
en quelque sorte,
nous sommes tous
des cobayes ! Ce
n’est pas toujours facile à accep-
ter. Bien entendu, tout médica-
ment a déjà été analysé et testé au
cours d’une ou plusieurs(s) étude(s)
clinique(s) avant sa mise sur le
marché, mais celles-ci sont réali-
sées sur des populations limitées
en nombre (4000-8000), homogènes
et sélectionnées soigneusement.
Par exemple, les patients âgés
sont fréquemment sous-représen-
tés et les prises concomitantes
d’autres médicaments ne sont
pas fréquentes. Donc il reste une
foule d’incertitudes sur la sécu-
rité du produit lorsque celui-ci
est mis sur le marché, mais il est
impossible de fonctionner autre-
ment aujourd’hui. C’est pourquoi la
pharmacovigilance est essentielle.
Elle propose des plans de gestion
de risques identifi és et potentiels,
ainsi que des études pharmacoé-
pidémiologiques permettant d’éva-
luer les risques « plus rares dans la
vraie vie ».
Utilise-t-on trop
de médicaments ?
Je pense qu’on utilise certains
médicaments de manière inap-
propriée, trop longtemps ou
trop dosés. Des campagnes de
l’AFMPS récurrentes mettent en
avant les excès d’utilisation de
certaines classes de médicaments
comme les anxiolytiques, hypno-
sédatifs, antidépresseurs et anti-
biotiques pour ne citer qu’eux. Et
cela fait partie aussi de la pharma-
covigilance de réguler l’utilisation
du médicament et de prévenir les
abus. Certains produits ont été
retirés du marché uniquement
parce qu’ils avaient été mal utili-
sés : par exemple, des médecins
ont prescrit des médicaments
pour maigrir à des personnes qui
n’étaient pas obèses ! Non seule-
ment l’effi cacité n’était pas prou-
vée dans ces populations mais les
risques restaient bien présents.
Doit-on avoir peur du
médicament en Europe ?
Non, nous sommes bien protégés et
peut-être même mieux qu’ailleurs.
Le fait que 27 pays à la sensibilité
et aux pratiques différentes votent
est évidemment source de richesse.
Par exemple, si la Suède met en
avant un risque médicamenteux
détecté sur base de cas rapportés
en raison d’une utilisation plus
importante sur son sol, les déci-
sions éventuelles prises au niveau
européen seront d’application éga-
lement dans les autres pays où ce
risque n’avait pas été identifi é. En
effet, dès que la commission a pris
une décision, tous les pays doivent
l’accepter, même les pays minori-
taires qui avaient éventuellement
voté contre.
Une harmonisation mondiale
existe-t-elle ?
Il y a une harmonisation de la
majorité des règles de pharmaco-
vigilance entre l’Europe, les États-
Unis, le Canada, le Japon et dans
une moindre mesure, l’Australie,
mais les décisions sont propres à
chacun. Cependant les commis-
sions des agences européennes et
américaines communiquent acti-
vement, même si une harmonisa-
tion des décisions reste utopique à
ce jour.
Propos recueillis par E.D.
TRIMESTRIEL N°87 NOVEMBRE 2012 5
INNOVATION
Cette nomination favorise les recherches en pharmacovigilance
menées par le Département de pharmacie en collaboration avec le
CHU Mont-Godinne, notamment sur les anticoagulants dans le cadre de la
plateforme de NARILIS, le Namur Thrombosis and Hemostasis Center (NTHC).
Jean-Michel Dogné
représente, pour un
mandat de 3 ans, la
Belgique au sein de la
PRAC comme membre
effectif, et son suppléant
est Virginie Chartier,
ancienne étudiante
du Département de
pharmacie namurois qui
travaille à l’AFMPS.
1
/
1
100%