Basics PHY1_2013_V1

Bases 1
ère
PARTIE v.1.00
Formation MF2 2013
support de cours
Page 1/7
JPM
Basics PHY1_2013_V1
Sommaire
1
Définitions succinctes ..................................................................................................................... 2
1.1
Molécule : ................................................................................................................................ 2
1.2
Atome ...................................................................................................................................... 2
1.3
Etat de la matière .................................................................................................................... 2
1.3.1
État solide ........................................................................................................................ 2
1.3.2
État liquide ....................................................................................................................... 2
1.3.3
État gazeux ...................................................................................................................... 2
1.4
Température ............................................................................................................................ 3
2
Unités ............................................................................................................................................. 3
2.1 ...................................................................................................................................................... 3
2.2
Multiples, sous multiples des unités ........................................................................................ 4
2.2.1
Multiples : ......................................................................................................................... 4
2.2.2
Sous multiples .................................................................................................................. 4
3
Composition des forces .................................................................................................................. 5
3.1
Les forces, définitions ............................................................................................................. 5
3.2
Composition de forces ............................................................................................................ 5
4
Pressions ........................................................................................................................................ 6
4.1
Définition ................................................................................................................................. 6
4.2
Pression absolue : ................................................................................................................... 6
4.3
Pression relative ...................................................................................................................... 6
4.4
Pression hydrostatique ............................................................................................................ 6
4.5
Pression atmosphérique ......................................................................................................... 7
4.6
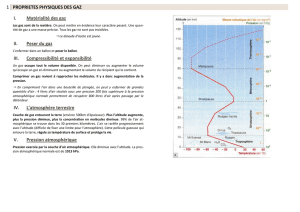
Variation de la pression atmosphérique en fonction de l’altitude ............................................ 7

Bases 1
ère
PARTIE v.1.00
Formation MF2 2013
support de cours
Page 2/7
JPM
Basics PHY1_2013_V1
1 Définitions succinctes
1.1 Molécule :
Une molécule est un assemblage chimique électriquement neutre d'au moins deux atomes, qui peut
exister à l'état libre, et qui représente la plus petite quantité de matière possédant les propriétés
caractéristiques de la substance considérée
Exemple :
Une molécule d’eau est composée de 2 molécules d’hydrogène et d’une molécule d’oxygène.
Elle est notée sous la forme « H
2
O ».
Une molécule d’oxygène est constituée de 2 atomes d’oxygène ; Elle est notée sous la forme « O
2 ».
1.2 Atome
Un atome], « que l'on ne peut diviser ») est la plus petite partie d'un corps simple pouvant se combiner
chimiquement avec une autre
1.3 Etat de la matière
Pour nos besoins nous ne parlerons que des trois états courants de la matière
1.3.1
État solide
L’état solide est caractérisé par l'absence de liberté entre les molécules ou les ions (métaux par
exemple).
Les critères macroscopiques de la matière à l'état solide sont que le solide a une forme propre et un
volume propre.
1.3.2
État liquide
L'état liquide est un état de la matière. Sous cette forme, la matière est facilement déformable mais
difficilement compressible.
Le liquide est une forme de fluide : les molécules y sont faiblement liées, ce qui rend les liquides
parfaitement déformables. Mais, à l'inverse du gaz, elles sont tout de même liées.
1.3.3
État gazeux
Dans l’état gazeux, la matière n'a pas de forme propre ni de volume propre : un gaz tend à occuper
tout le volume disponible.
Le changement d’état se fait par apport ou prélèvement d’énergie qui se traduit par une agitation
thermique plus ou moins importante.

Bases 1
ère
PARTIE v.1.00
Formation MF2 2013
support de cours
Page 3/7
JPM
Basics PHY1_2013_V1
1.4 Température
La température est une grandeur physique mesurée à l'aide d'un thermomètre et étudiée en
thermométrie. Dans la vie courante, elle est reliée aux sensations de froid et de chaud, provenant du
transfert de chaleur entre le corps humain et son environnement.
En physique, elle se définit de plusieurs manières : Nous nous en tiendrons à celle de la fonction
croissante du degré d'agitation thermique des particules (en théorie cinétique des gaz)
Les particules qui composent un système matériel (molécules ou atomes) ne sont jamais au repos.
Elles sont en vibration permanente et possèdent donc une certaine énergie cinétique. La température
est une mesure indirecte du degré d'agitation microscopique des particules.
2 Unités
Les grandeurs physiques portent un NOM qui correspond à une définition et ont chacune une unité
de mesure
Elles sont reliées entre elles .par des relations et le système d’unité (l’ensemble des unités) doit être
HOMOGENE
MESURE UNITE SYMBOLE
NOTA
Temps Seconde t s
Longueur Mètre L m
Surface mètre carré S m
2
Volume mètre cube V m
3
Masse Kilogramme M kg
Masse volumique Kilogramme
par mètre
cube
mv
Kg/m
3
Densité
(sans)
d Rapport entre la masse volumique du corps
et la masse volumique de l’eau douce pour
les solides et la masse volumique de l’air
pour les gaz
Vitesse Mètre par
seconde v m/s
Accélération Mètre par
seconde par
seconde
γ
m/s
2
Température absolue
Kelvin T K Mesure de la température par rapport au
zéro absolu(plus d’agitation thermique)
Force Newton F N 1 N = 1 kg x 1 m/s/s
NB : le poids est une force particulière
Température degré Celsius T° 0°C = 273,15 K
Pression pascal
bar p Pa
bar Répartition d’une force exprimée en Newton
sur une surface exprimée en m
2
, utilisée
plus couramment sous forme hecto pascal
(hPa) et tolérance pour le bar qui est égal à
1000 hPa

Bases 1
ère
PARTIE v.1.00
Formation MF2 2013
support de cours
Page 4/7
JPM
Basics PHY1_2013_V1
2.1 Multiples, sous multiples des unités
Comme certaines unités ne sont pas adaptées à l’échelle humaine en fonction des grandeurs
mesurées, nous utiliserons couramment des multiples ou sous multiples des unités de base.
2.1.1 Multiples :
Déca x10 Décamètre
Hecto x100 Hectolitre Hectopascal
Kilo x1000 Kilomètre
Méga x 1000 000 Mégahertz
Giga x 1000 000 000 Gigabit
2.1.2 Sous multiples
déci 1/10 décimètre
centi 1/100 centimètre cube (cm
3
)
milli 1/1000 milli…mètre
micro 1/1000 000 µfarad (capacité électrique)
nano 1/1000 000 000 nanomètre (longueur d’onde)

Bases 1
ère
PARTIE v.1.00
Formation MF2 2013
support de cours
Page 5/7
JPM
Basics PHY1_2013_V1
3 Composition des forces
3.1 Les forces, définitions
Les forces sont représentées par des vecteurs, leur intensité est représentée par la longueur du
vecteur, et leur direction par la droite portant le vecteur, et le sens par le sens de la flèche
L’unité est le Newton. (N)
Si nous appliquons une force de 1N sur une masse de 1kg, la vitesse de cette masse augmentera de
1m/s à chaque seconde.
Cette force peut être décomposée (entre autre) en une décomposition de 2 forces portées par deux
axes représentant le plan où agit cette force. Ces deux axes sont liés entre eux par un angle droit.
Le poids est une force particulière qui s’applique sur le centre de gravité de l’objet
3.2 Composition de forces
Plusieurs forces qui s’appliquent sur un point peuvent être réduites en une seule force résultante.
Cas particuliers, les deux forces sont portées par le même axe (même direction), la valeur de la force
résultante est égale à la somme algébrique des forces
Valeur de la force
Direction de la force
Sens de la force
F1 F2
FR
 6
6
 7
7
1
/
7
100%