Cours élève

Cours de Physique – Chimie Classe de Première S
Partie : Comprendre : Lois et modèles
Thème : Cohésion et transformations de la matière
Chap. X LA COHESION DE L A MATIERE
Compétences attendues :
✔Connaître les ordres de grandeur des dimensions des différentes structures des édifices organisés.
✔Connaître l'ordre de grandeur des valeurs des masses d'un nucléon et de l'électron.
✔Savoir que toute charge électrique peut s'exprimer en fonction de la charge élémentaire e.
✔Associer, à chaque édifice organisé, la ou les interactions fondamentales prédominantes.
✔Utiliser la représentation symbolique
X
Z
A
.
I. La matière à différentes échelles
1°) L'ordre de grandeur
2°) Ordre de grandeur des dimensions de différents édifices
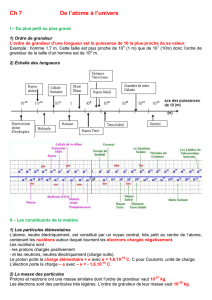
Les noyaux des atomes sont les plus petites structures dont l'ordre de grandeur de la taille est connue : 10-15 m.
Celle de l'atome a pour ordre de grandeur 10-10m.
La taille du système solaire est de l'ordre de 1013m, et celle de notre galaxie, la voie lactée, 1021m.
Document 1 : Echelle de mesure de dimension
II. Les constituants de la matière
1°) Les particules élémentaires
Tout édifice est constitué d'atomes, de molécules ou d'ions.
Ces entités sont elles-même formées à partir de particules plus petites dites élémentaires :
•les nucléons qui regroupent les protons et les neutrons ;
•les électrons.
1
10-15 10-10 10-5 1001051010 1015 1020 1025 Dimension
en m
Noyau Atome
Cellule
Être
humain
Distance
Terre -
Soleil
Voie
lactée
Rayon
de la
Terre
Rayon
du
Soleil
Système
solaire
Distance
Terre -
Lune

Cours de Physique – Chimie Classe de Première S
Les caractéristiques de ces particules élémentaires sont résumées dans le tableau suivant :
Particule Localisation Charge Masse Ordre de grandeur
de la masse
Proton Dans le noyau +e = 1,6x10-19C 1,673 x 10-27 kg 10-27 kg
Neutron Dans le noyau 0 1,675 x 10-27 kg 10-27 kg
Electron Autour du noyau -e = -1,6x10-19 C 9,1 x 10-31 kg 10-30 kg
2°) La charge élémentaire
La charge électrique
e
est appelée charge élémentaire. C'est la charge électrique d'un proton. C'est aussi l'opposé de la charge
électrique d'un électron.
La charge élémentaire est notée e et vaut
e=1,60⋅10−19 C
.
La charge électrique q d'un noyau atomique, d'un ion ou d'un objet chargé peut s'exprimer en fonction de la charge élémentaire e :
q=n.e
avec n, un nombre entier.
3°) Atome, ion et molécule
•L'atome est constitué d'un noyau et d'un nuage électronique. Le noyau d'un atome est représenté symboliquement par la
notation
X
Z
A
.
A, appelé nombre de masse, est le nombre de nucléons. Z, appelé nombre de charges ou numéro atomique, est le nombre
de protons.
Le nombre de neutrons est donné par la différence
A−Z
.
Le nuage électronique est chargé négativement et compte autant d'électrons qu'il y a de protons dans un atome, puisque
l'atome est une entité électriquement neutre.
•Un ion monoatomique est issu d'un atome qui a perdu ou gagné un ou plusieurs électrons, il est donc lui aussi constitué
de protons et le plus souvent de neutrons et d'électrons.
•Une molécule regroupe plusieurs atomes, elle est donc aussi constituée de protons, d'électrons et le plus souvent de
neutrons.
Les protons, les neutrons et les électrons constituent donc les « briques de base » de la matière de l'Univers.
III. Les interactions fondamentales
Tous les phénomènes physiques, chimiques et biologiques observés peuvent être expliqués grâce à quatre interactions
fondamentales.
1°) L'interaction gravitationnelle
Tous les corps qui possèdent une masse s'attirent mutuellement.
Deux objets A et B de masses respectives mA et mB, dont les centres sont séparés d'une distance d, exercent l'un sur l'autre des
actions mécaniques attractives, modélisées par des forces d'attraction gravitationnelle
⃗
FA/B
et
⃗
FB/A
dont les
caractéristiques sont :
•point d'application : centre de A pour
⃗
FB/A
et centre de B pour
⃗
FA/B
•direction : la direction de la droite (AB)
•sens : vers le centre A pour
⃗
FA/B
et B pour
⃗
FB/A
•norme :
FA/B=FB/A=G⋅mA⋅mB
d2
avec mA et mB, en kg
d en m
FA/B et FB/A en N
G = 6,67 x 10-11 N.m2.kg-2 constante de gravitation universelle.
L'interaction gravitationnelle est toujours attractive et de portée infinie. La loi de la gravitation universelle s'applique aux objets
dont la masse est répartie de façon sphérique c'est à dire de façon régulière à partir du centre.
2
d
A B
FB/A FA/B

Cours de Physique – Chimie Classe de Première S
2°) L'interaction électromagnétique
Deux corps chargés électriquement sont soumis à une interaction électrique s'ils sont au repos, à laquelle vient s'ajouter une
interaction magnétique s'ils sont en mouvement. On parle alors d'interaction électromagnétique.
3°) Interaction forte et interaction faible
➢
➢
4°) La cohésion de la matière
3
1
/
3
100%