revue L`entrée du virus de l`hépatite C dans ses cellules cibles

revue
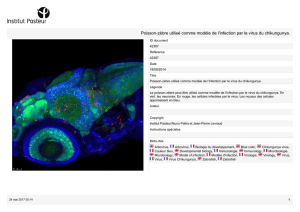
L’entrée du virus de l’hépatite C
dans ses cellules cibles
F. Helle
L. Cocquerel
Institut de biologie de Lille, CNRS-
UMR8161 Laboratoire Hépatite C,
1, rue Calmette,
BP 447,
59021 Lille
Résumé.Pour initier son cycle infectieux, une particule virale doit d’abord
traverser la membrane plasmique de la cellule hôte afin d’atteindre les compo-
sants cytosoliques et nucléaires nécessaires à sa réplication. Pour un virus
enveloppé, cela implique une liaison à la membrane plasmique suivie par une
migration du virion vers un microdomaine ou une vésicule d’endocytose où les
enveloppes virale et cellulaire vont fusionner. Le mécanisme exact par lequel le
virus de l’hépatite C (HCV) entre dans ses cellules cibles, les hépatocytes, reste
à élucider. Néanmoins, les données accumulées jusqu’à ce jour indiquent que le
mécanisme d’entrée du HCV est un processus lent et complexe faisant intervenir
plusieurs facteurs d’entrée. Dans une première étape, le virion s’attacherait à la
surface cellulaire par l’intermédiaire des glycosaminoglycanes et du récepteur
des lipoprotéines de faible densité. Cet événement serait ensuite suivi par une
série d’interactions avec le récepteur scavenger de classe B et de type I, la
tétraspanine CD81 et une protéine des jonctions serrées Claudine 1, 6 ou 9. Dans
cette revue, nous avons résumé l’essentiel des connaissances accumulées sur les
étapes d’entrée du HCV dans ses cellules cibles.
Mots clés :virus de l’hépatite C, entrée virale, glycoprotéines d’enveloppe,
facteur d’entrée, processus multiséquentiel
Abstract.To replicate its genome, a virus needs to cross the plasma membrane
of a host cell and get access to cytosolic and/or nuclear components. For an
enveloped virus, this involves binding to the plasma membrane, followed by
migration of the virion to a microdomain or an endosomal vesicle where fusion
between the virion envelope and a host cell membrane occurs. Although we are
still far from understanding the details of hepatitis C virus (HCV) entry, recent
data show that this virus enters into target cells in a slow and complex multistep
process involving the presence of several entry factors. Initial attachment of the
virion may involve glycosaminoglycans and the low-density lipoprotein recep-
tor, and it is followed by the sequential interaction with the scavenger receptor
BI, the tetraspanin CD81 and the tight junction protein Claudin-1, -6 or -9. The
current knowledge accumulated on HCV entry is summarized in this review.
Key words:hepatitis C virus, virus entry, envelope glycoproteins, entry factor,
virus attachment, multistep process
L’interaction sélective des virus animaux avec leur(s)
récepteur(s) spécifique(s) présent(s) à la surface des cellu-
les est une étape essentielle à l’initiation de leur cycle
infectieux. Une telle interaction détermine souvent le spec-
tre d’hôtes et le tropisme cellulaire ou tissulaire du virus et
joue un rôle essentiel dans la pathogénicité du virus. Si le
virus ne peut se lier à la surface cellulaire, l’infection ne
peut alors être initiée. Une connaissance détaillée des mé-
canismes impliqués dans l’entrée d’un virus permet non
Tirés à part : L. Cocquerel
Virologie 2008, 12 (2) : 105-16
doi: 10.1684/vir.2008.0163
Virologie, Vol. 12, n° 2, mars-avril 2008
105
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

seulement de comprendre comment ce virus infecte ses
cellules hôtes mais également d’entrevoir la possibilité de
développer de nouvelles drogues antivirales. Les mécanis-
mes régulant l’entrée du virus de l’hépatite C (HCV) dans
ses cellules cibles, les hépatocytes, sont aujourd’hui encore
mal connus.
L’hépatite C est un problème majeur de santé publique.
Cette infection touche environ 130 millions de personnes à
travers le monde [1]. En France, on estime que 600 000 à
1 million de personnes seraient atteintes par cette maladie.
L’infection par le HCV est généralement chronique (60 à
80 % des cas) et les aspects cliniques peuvent se caractéri-
ser par un portage asymptomatique, une hépatite chronique
active et une cirrhose qui est fortement associée au déve-
loppement d’un carcinome hépatocellulaire. À l’heure
actuelle, il n’existe aucun vaccin pour lutter contre le HCV
et les thérapies antivirales utilisées actuellement ont une
efficacité relativement limitée ([1]).
Le HCV est un petit virus enveloppé appartenant au genre
Hepacivirus de la famille des Flaviviridae [1]. Ce virus à
ARN de polarité positive est constitué d’une nucléocapside
entourée d’une enveloppe lipidique dans laquelle sont an-
crées deux glycoprotéines d’enveloppe, E1 et E2 (figure 1).
Ces deux protéines forment des hétérodimères non cova-
lents qui jouent un rôle majeur dans le mécanisme d’entrée
du HCV. Ces quinze dernières années ont été marquées par
l’absence d’un système de culture cellulaire permettant de
multiplier efficacement le HCV. Différents outils ont donc
été développés afin de pouvoir étudier l’entrée du HCV
dans ses cellules cibles. L’utilisation de tels outils a permis
A
B
Glycoprotéines
d'enveloppe
E1 et E2
ARN simple brin
de polarité positive
Enveloppe virale
Nucléocapside
E1 E2
CE1 E2 P
7NS2 NS3 NS
4A NS5ANS4B NS5B
Figure 1. A. Représentation schématique d’une particule du HCV. L’enveloppe virale est composée d’une bicouche lipidique (en vert) dans
laquelle sont insérées les deux glycoprotéines d’enveloppe E1 et E2 (en jaune). Cette enveloppe renferme une nucléocapside (en bleu)
à l’intérieur de laquelle se trouve la molécule d’ARN simple brin de polarité positive (en beige). B. Le génome du HCV code une
polyprotéine unique qui, après maturation par des protéases cellulaires et virales, va libérer une dizaine de protéines dont les deux
glycoprotéines d’enveloppe E1 et E2. Ces deux protéines présentent un large ectodomaine N-terminal hautement N-glycosylé et sont
ancrées dans les membranes par leurs domaines transmembranaires C-terminaux.
revue
Virologie, Vol. 12, n° 2, mars-avril 2008
106
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

de mettre en évidence des interactions avec un certain
nombre de protéines de surface cellulaire et a permis de
caractériser le rôle des glycoprotéines E1E2 dans l’entrée
virale. Le développement récent d’un système de produc-
tion du HCV en culture cellulaire permet aujourd’hui de
confirmer les données obtenues jusqu’à présent. Dans cette
revue, nous avons résumé l’essentiel des connaissances
accumulées sur les étapes précoces du cycle infectieux du
HCV.
Cycle infectieux du HCV
Un cycle viral du HCV, essentiellement basé sur le modèle
des Flavivirus d’autres membres de la famille des Flavivi-
ridae, est représenté dans la figure 2 [2]. La première étape
correspond à la liaison des virus à la surface des cellules,
sur le(s) récepteur(s) spécifique(s). Le virus est alors endo-
cyté par une voie dépendante de la clathrine. Ensuite, la
membrane virale fusionne avec la membrane des endoso-
mes précoces de la cellule, conduisant à la libération de
l’ARN viral dans le cytoplasme. Le génome sert alors à la
synthèse du brin négatif qui permet la production d’ARN
brin positif. En parallèle, les protéines virales sont synthé-
tisées sous forme d’une polyprotéine adressée dans le réti-
culum endoplasmique (RE). Finalement, les protéines de
structure vont s’assembler dans un compartiment encore
inconnu pour former de nouvelles particules virales qui
suivront la voie de sécrétion jusqu’à leur export hors de la
cellule.
Le passage d’un virus de l’extérieur vers l’intérieur de la
cellule est appelé entrée virale. Pour les virus enveloppés,
ce processus peut être divisé en plusieurs étapes : l’attache-
ment du virus à la surface des cellules, l’interaction avec
le(s) récepteur(s) spécifique(s) du virus et finalement la
fusion de l’enveloppe lipidique virale avec une membrane
cellulaire (plasmique ou endosomale) permettant l’intro-
1
2
3
4
7
6
5
(+) RNA
Figure 2. Cycle viral du HCV basé sur le modèle des Flavivirus. (1) Le virus se lie à la surface des cellules sur leur(s) récepteur(s)
spécifique(s). (2) Le virus est ensuite endocyté par une voie dépendante de la clathrine. (3) L’enveloppe virale fusionne alors avec la
membrane des endosomes précoces, permettant la libération de l’ARN viral dans le cytoplasme. (4) Le génome sert à la synthèse des
protéines virales dans le réticulum endoplasmique (RE). (5) En parallèle, le génome du HCV sert à la synthèse de brins négatifs qui
serviront de matrice pour la synthèse de nouvelles molécules d’ARN de polarité positive. (6) Les protéines structurales servent à
l’assemblage de nouvelles particules qui suivront la voie de sécrétion jusqu’à leur export hors de la cellule (7).
revue
Virologie, Vol. 12, n° 2, mars-avril 2008
107
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

duction du génome viral dans le cytoplasme de la cellule
infectée. Ces étapes du cycle viral mettent en jeu deux
grands acteurs : les protéines d’enveloppe à la surface du
virus et les récepteurs et co-récepteurs à la surface des
cellules.
Les glycoprotéines d’enveloppe du HCV
Les protéines d’enveloppe jouent un rôle prépondérant
dans l’entrée virale. En effet, en plus de permettre l’interac-
tion avec le(s) récepteur(s) cellulaire(s), ces protéines per-
mettent d’induire la fusion entre les enveloppes virale et
cellulaire. Le génome du HCV code une polyprotéine d’en-
viron 3 000 acides aminés qui est clivée de façon co- et
post-traductionnelle, par des protéases virales et cellulai-
res, pour produire une dizaine de protéines [1], dont les
deux glycoprotéines d’enveloppe, E1 et E2 (figure 1). Ces
deux protéines possèdent un large ectodomaine N-terminal
et sont ancrées dans les membranes par leurs domaines
transmembranaires (TM) C-terminaux [3]. Les ectodomai-
nes de E1 et E2 sont hautement N-glycosylés, et cette
glycosylation semble jouer un rôle important dans le replie-
ment des protéines, l’entrée virale et la protection contre
des anticorps neutralisants [4-6]. Durant leur synthèse, les
ectodomaines de E1 et E2 sont dirigés vers la lumière du RE
et leur domaine TM est inséré dans la membrane de ce
compartiment [3]. L’extrêmité C-terminale de la forme
immature de la protéine de capside (C) contient une sé-
quence signal responsable de la translocation de l’ectodo-
maine de E1 dans la lumière du RE, et les domaines TM de
E1 et E2 contiennent également un signal permettant une
réinitiation de la translocation dans la lumière du RE. Les
domaines TM de E1 et E2 sont multifonctionnels car, en
plus de leur rôle d’ancrage membranaire et de séquence
signal, ces domaines contiennent des signaux de rétention
stricte dans le RE et jouent un rôle majeur dans l’hétérodi-
mérisation de E1 et E2 [3]. Par ailleurs, la mutation de
certains résidus des domaines TM de E1 et E2 altère la
propriété de fusion des glycoprotéines d’enveloppe, suggé-
rant que ces domaines jouent également un rôle majeur
dans le mécanisme de fusion [7]. Une étude récente de
Lavilette et al. a également permis d’identifier trois régions
de E1 et E2 impliquées dans le mécanisme de fusion [8].
Systèmes d’étude de l’entrée du HCV
En 1989, le génome du HCV a été cloné par Choo et al. [9].
Cela a permis une analyse rapide de son organisation géno-
mique ainsi qu’une caractérisation biochimique de ses pro-
téines. Néanmoins, jusqu’en 2005, aucun système de cul-
ture cellulaire permettant de produire de manière efficace le
virus n’a pu être développé. L’absence d’un tel système a
donc constitué pendant plus de quinze ans un véritable
obstacle à l’étude du cycle réplicatif du HCV. Des particu-
les issues de sérum de patients infectés ont été utilisées par
certains groupes pour étudier l’entrée du HCV. Néanmoins,
du fait de leur faible taux de réplication et de leur grande
hétérogénéité, ce type de particules n’a permis qu’une
exploration partielle du cycle infectieux du HCV. C’est
pourquoi d’autres outils ont été par la suite développés. Une
forme soluble de la glycoprotéine E2 a permis d’identifier
un certain nombre de protéines de surface cellulaire poten-
tiellement impliquées dans l’entrée du HCV [10]. D’autres
laboratoires ont également utilisé des virus-like particles
(VLP) produites en cellules d’insectes ou des pseudoparti-
cules recombinantes du virus de la stomatite vésiculaire
(VSV) [10-12]. Néanmoins, ces systèmes n’ont pas permis
d’étudier l’étape de fusion faisant intervenir les hétérodi-
mères E1E2. En 2003, une avancée majeure dans l’étude de
l’entrée du HCV a été le développement de particules
rétrovirales pseudotypées avec les protéines d’enveloppe
du HCV (HCVpp) [13-15]. Ces pseudoparticules sont pro-
duites après transfection de cellules humaines 293T par
trois vecteurs d’expression : le premier exprime les glyco-
protéines E1 et E2 natives, le deuxième exprime les protéi-
nes codées par les gènes gag et pol du virus de la leucémie
murine (matrice, capside, nucléocapside, protéase, reverse-
transcriptase, intégrase) et le troisième exprime un ARN
codant un gène rapporteur, qui sera intégré dans le génome
des cellules infectées (figure 3). Les HCVpp sont sécrétées
dans le milieu de culture cellulaire et permettent une bonne
transduction des cellules qui est dépendante de la présence
des protéines E1 et E2 à la surface de ces particules. Du fait
de leur tropisme préférentiel pour les cellules d’origine
hépatique et de leur neutralisation spécifique par des anti-
corps monoclonaux reconnaissant la protéine E2 ainsi que
par des sera de patients infectés, ces pseudotypes ont repré-
senté pendant plusieurs années l’outil le plus proche des
particules natives du HCV. Toutefois, ces HCVpp ne reflè-
tent pas complètement le virus produit chez les patients. En
particulier, contrairement au virus natif dont la production
semble liée à l’assemblage et à la sécrétion des lipoprotéi-
nes de très faible densité (VLDL, very low density lipopro-
teins) [16], les HCVpp sont supposées s’assembler indé-
pendamment des VLDL. Par ailleurs, les HCVpp ne
contiennent pas de génome capable de se répliquer. Elles ne
permettent donc d’étudier que l’étape de l’entrée virale. En
2005, un clone du HCV isolé chez un patient japonais
atteint d’une hépatite fulminante a finalement permis le
développement d’un système de culture cellulaire permet-
tant de produire efficacement des particules infectieuses du
HCV [17]. Ce système est basé sur la transfection d’une
lignée d’hépatocarcinome humain (Huh-7) avec des ARN
de la souche JFH1 (génotype 2a). Ce système permet de
revue
Virologie, Vol. 12, n° 2, mars-avril 2008
108
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

produire de manière relativement efficace du virus natif,
appelé HCVcc, capable de réinfecter des cellules naïves
[17-19]. Les cellules Huh-7 peuvent être infectées de façon
chronique, même si des événements d’adaptation du virus
et des cellules ont lieu afin de favoriser leur survie. Ces
particules permettent une infection productive chez le
chimpanzé et chez des souris transplantées avec des hépa-
tocytes humains [20]. Depuis, des systèmes de culture
cellulaire permettant de produire des particules infectieuses
issues d’autres génotypes ont été décrits, mais l’efficacité
de ces systèmes de production est plus faible. Pour la
première fois depuis quinze ans, les différentes étapes du
cycle infectieux du HCV incluant l’entrée des particules
virales dans leurs cellules cibles, la réplication du génome
viral, l’assemblage et la sécrétion des particules néosynthé-
tisées, peuvent maintenant être étudiées.
Plasmide 2
Transfection de cellules 293T
Infection de cellules Huh-7
Quantification
de l'activité luciférase
CMV
CMV
CMV LTR LTR
luciférase
gag-pol
HCV-E1E2
PBS PPT
Intégrase
Transcriptase inverse
Glycoprotéines
d'enveloppe du HCV
E1 et E2
ARN codant la
luciférase
Capside du MLV
HCVpp
Plasmide 1
Plasmide 3
Figure 3. Représentation schématique de la production des HCVpp. Pour la production des HCVpp, des cellules de rein embryonnaires
humaines 293T sont transfectées avec trois vecteurs d’expression. Le premier code les glycoprotéines E1 et E2 du HCV qui sont
responsables du tropisme cellulaire. Le second vecteur exprime les protéines codées par les gènes gag et pol du virus de la leucémie
murine (matrice, capside, nucléocapside, protéase, transcriptase inverse, intégrase). Les protéines de matrice, capside et nucléocapside
permettent l’encapsidation de l’ARN grâce au signal d’encapsidation (w), l’assemblage de la particule et son bourgeonnement à la
membrane plasmique. Finalement, le troisième vecteur code l’ARN qui va être encapsidé dans les particules. Cet ARN contient des
séquences rétrovirales nécessaires à la transcription inverse et à l’intégration de l’ADN proviral dans l’ADN génomique de la cellule
infectée (LTR, long terminal repeat ; PBS, primer binding site ; PPT, polypurine track) et contient un gène rapporteur codant la luciférase.
Les HCVpp sont sécrétées dans le surnageant de culture des cellules 293T et sont utilisées pour infecter des cellules d’hépatocarcinome
humain Huh-7. Les cellules infectées vont intégrer le gène codant la luciférase dans leur ADN génomique grâce à la transcriptase inverse
et à l’intégrase, et par conséquent, vont exprimer la luciférase. L’infectiosité des HCVpp pourra alors être évaluée par quantification de
l’activité luciférase dans les cellules Huh-7.
revue
Virologie, Vol. 12, n° 2, mars-avril 2008
109
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%