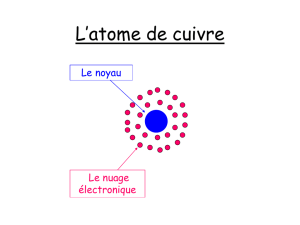
Formation des ions

Charge de l’atome de sodium
numéro atomique
Z = 11
L’atome est
électriquement neutre
Les électrons :
11 charges
négatives
Le noyau :
11 charges
positives
Charge : 11 –11 = 0

L’atome de sodium
Le nuage
électronique
Le noyau
L’ion sodium
Perte de 1 électron
Formation de l’ion sodium

Charge de l’ion sodium
Les électrons :
10 charges
négatives
Le noyau :
11 charges
positives 11 –10 = + 1
Sa charge est :
On le note :
Na+
L’ion sodium est un ion
chargé positivement

Charge de l’atome de chlore
numéro atomique
Z = 17
L’atome est
électriquement neutre
Les électrons :
17 charges
négatives
Le noyau :
17 charges
positives
Charge : 17 –17 = 0

L’atome de chlore L’ion chlorure
Le nuage
électronique
Le noyau Gain de 1 électron
Formation de l’ion chlorure
 6
6
 7
7
1
/
7
100%