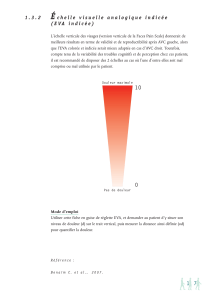
mélange de gaz

Eva Monteiro 1
Thermodynamique Avancée
Eva Monteiro
Éric Girard

Thermodynamique Avancée
Révisions de la thermodynamique
classique et thermodynamique de l’atmosphère
Eva Monteiro : (8 semaines)
Microphysique des nuages :
Éric Girard (7 semaines)

Eva Monteiro 3
Ce qu’il faut connaître
Système thermodynamique
loi des états d’équilibre
(équation d’état)
gaz parfait
mélange de gaz parfaits :
lois de Dalton
énergie interne
enthalpie
entropie
chaleur
travail
premier et deuxième
principes
processus isobare
processus adiabatique
changements de phase
saturation
vapeur saturante
équation de Clausius
Clapeyron
chaleur latente.
condensation/évaporation
lois de Kirchhoff

Eva Monteiro 4
La thermodynamique (révisions)
La thermodynamique est la science qui étudie les
transformations d’énergie des grands systèmes
en équilibre
Dans ce cours le système en étude c’est
l’atmosphère terrestre
http://www.pixheaven.net/html/geoman/apprendre/images/terre_atmosphere.jpg

Eva Monteiro 5
Air
atmosphérique
Air sec
Eau
aérosols
N2,O2,
Ar, CO2
Comp.
Const.
Solide
liquide
vapeur
variable
Rôle importante:
chimie,
physique des nuages
radiation
Composition de l’atmosphère dans les
premiers 110 km.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
1
/
40
100%