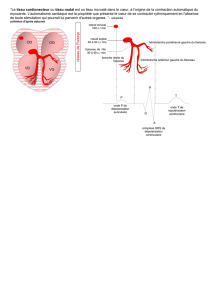
coeur automatisme cardiaque

Physiologie cardiaque : de
l’excitation à la contraction (1)
L2 Sciences de la vie et géosciences
semestre 4

Mise en évidence de l’automatisme cardiaque
liquide de
perfusion
coeur
isolé
stylet
Montage simple permettant
d’enregistrer les contractions
du cœur isolé de grenouille
Chez les mammifères, le cœur isolé doit être
maintenu à 37°C et le LP (oxygéné et glucosé) ne
perfuse pas les cavités cardiaques mais les
vaisseaux coronaires.
carbogène
(95% 025% CO2)
LP
pompe
eau à 37°C
pompe

Localisation du centre d’automatisme chez la grenouille
La 1ère ligature de Stannius
Avant la ligature
sor v
Après la ligature
Les ganglions intracardiaques
Remak
Ludwig
Bidder
Les battements du cœur ont-ils pour origine les neurones du ganglion
de Remak (théorie neurogène) ou les cellules musculaires du sinus
veineux (théorie myogène) ?
Après destruction localisée du ganglion de Remak, le cœur continue
de battre, ce qui n’est pas en accord avec la théorie neurogène.
Conclusion :
le centre d’automatisme se
trouve dans le sinus veineux

Hiérarchie entre centres d’automatisme chez la grenouille
Le ventricule bat à une fréquence plus basse que l’ensemble sinus veineux-oreillettes, ce qui met en
évidence l’existence d’un centre d’automatisme secondaire dans la paroi ventriculaire (ce n’est pas le
ganglion de Bidder). Dans les conditions normales, le centre le plus rapide, situé dans le sinus veineux,
impose son rythme à l’ensemble du cœur.
VV
OR
10 s
La 3e ligature de Stannius

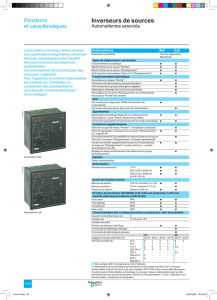
Le centre d’automatisme chez les mammifères : données histologiques
nœud
sinusal
nœud
septal
L’observation microscopique de toutes les régions du cœur permet de découvrir 2 zones particulères :
-le nœud sinusal ou sino-auriculaire, situé dans la paroi de l’OD, àla base de la veine cave supérieure
-le nœud septal ou auriculo-ventriculaire, situé dans la cloison inter-auriculaire, du côté droit.
milieu
interstitiel
myofibrilles
Ces 2 nœuds forment le tissu nodal.On y trouve des cellules musculaires pauvres en myofibrilles, avec
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%