THERMODYNAMIQUE – NOTES (#2)

THERMODYNAMIQUE – NOTES (#2) Dan Angelescu
Energie interne d’un gaz parfait (quelques éléments de théorie cinétique)
L’énergie interne d’un gaz parfait et la somme des énergies mécaniques (cinétiques) de
translation, rotation, vibration etc. de toutes les molécules composant le gaz. L’énergie est
repartie de manière égale entre les différents types de mouvement des molécules
(équipartition de l’énergie). Normalement, les modes de vibration ne sont excites que pour des
très hautes températures, alors on va juste considérer les translations et vibrations.
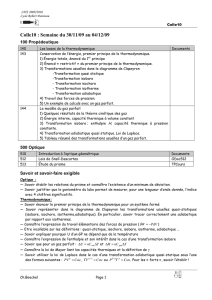
a b c
Figure 1a : Molécule monoatomiques (pour exemple, gaz noble) : 3 degrés de liberté (3 translations, pas
d’énergie de rotation, pas de vibration), Figure 1b : Molécule diatomique (azote, oxygène, air) : 5 degrés de
liberté (3 translations, 2 rotations (pas d’énergie de rotation autour de l’axe moléculaire)), Figure 1c : Molécule
poly atomique : 6 degrés de liberté (toutes les translations et rotations)
Alors on peut écrire :
RT
n
U
ν
2
=
ou n=3 pour le gaz monoatomique, et n=5 pour le gaz diatomique (les deux cas les plus
communs).
ν
est le nombre de moles de gaz, T la température absolue, et R la constante de
gaz, R=8.314 J/(mole K).
Capacité calorifique, chaleur spécifique
La quantité de chaleur qui est nécessaire pour élever la température d’un système par 1K
s’appelle la capacité calorifique (ou bien capacité thermique) du système. Pour obtenir une
mesure qui ne dépende que du matériau, et pas de la forme, dimension ou masse du système,
on divise soit par la masse du système, soit par le nombre de moles. Dans ce cas on obtient la
capacité thermique massique ou, respectivement, molaire. Celles si sont aussi appelées
chaleurs spécifiques massiques, ou respectivement, molaires.
T
Q
m
C
m
∆
=1
(capacité thermique massique)
T
Q
C
∆
=
ν
ν
1 (capacité thermique molaire)

Pour un gaz parfait, la chaleur spécifique molaire dépend du type de transformation qu’on
impose au système pour le chauffer. On peut chauffer a pression constante (dans ce cas, on
mesure la chaleur spécifique a pression constante (isobare) C
p
) ou bien on peut chauffer au
volume constant (chaleur spécifique a volume constant C
V
(isochore)).
On peut calculer C
V
et C
p
pour un gaz parfait :
Figure 2 : On peut chauffer un gaz parfait du point A (a température T) a un point a température T+∆T soit par
une transformation isocore (AB) soit par une transformation isobare (AC). La température finale sera la même,
mais les chaleurs dépensés pour y arriver (et les états finaux du système) seront différentes.
Pour la transformation isochore AB,
0
=
AB
W
alors on a
TR
n
TTR
n
UQ
ABABAB
∆=−=∆=
νν
2
)(
2
et on obtient la chaleur spécifique molaire à volume constant :
R
n
T
Q
C
AB
V
2
=
∆
=
ν
.
Pour la transformation isobare AC,
TRTTRVVpW ACACAAC
∆
=
−
=
−
=
ν
ν
)()( . Dans ce cas
on obtient
TR
n
TTR
n
TRUWQ ABABACAC ∆
+
=−+∆=∆+=
ννν
2
2
)(
2
et on obtient la chaleur spécifique molaire à pression constante :
R
n
T
Q
CAC
p
2
2
+
=
∆
=
ν
.
On voit bien qu’on peut aussi écrire
RCC
Vp
+=
.

Transformation adiabatique
Lors d’une transformation adiabatique il n’y a pas de changement de chaleur, alors Q=0. Dans
ce cas, on a l’égalité:
0
=
+
∆
WU
Comme on a vu toute a l’heure,
RT
n
U
ν
2
=
et RTpV
ν
=
alors
)(
2
)(
2
VppV
n
pV
n
U∆+∆=∆=∆
VpW
∆
=
Alors on obtient l’égalité :
=
+
∆
=
WU0Vp
n
pV
n
VpVppV
n∆
+
+∆=∆+∆+∆
2
2
2
)(
2
On divise par
pV
n
2
pour obtenir :
)ln()ln()ln(
2
0
γ
γ
pVVp
V
V
n
n
p
p∆=∆+∆=
∆
+
+
∆
=
ou on a utilise la notation
n
n2
+
=
γ
.
On voit que dans une transformation adiabatique, le produit
γ
pV doit rester constant, ce qui
donne l’équation de l’adiabate :
.constpV =
γ
avec
...666.1
3
5==
γ
pour le gaz monoatomique et
4.1
5
7==
γ
pour le gaz diatomique.
On peut utiliser l’équation du gaz idéal pour écrire l’équation de l’adiabate en utilisant autres
coordonnées (p,T ou V,T au lieu de p,V). Alors :
==
=
.
.
constR
T
pV
constpV
ν
γ
En divisant les deux équations on obtient : .
1
constTV =
−
γ
et en élevant la deuxième équation
à la puissance
γ
puis en divisant par la première équation on obtient :
.
1
const
T
p=
−
γ
γ
On peut utiliser l’équation la plus convenable, selon les variables connues dans le problème.

Transformation isochore
Dans la transformation isochore il n’y a pas de changement de volume, donc pas de travail
mécanique. Alors, on peut écrire :
TCTR
n
UQ
V
∆=∆=∆=
νν
2
ou on se rappelle que C
V
est la chaleur spécifique a volume constant.
Transformation isobare
Dans la transformation isobare il n’y a pas de changement de pression. Alors, on peut écrire :
TRVpW
∆
=
∆
=
ν
TCTR
n
WUQ
P
∆=∆
+
=+∆=
νν
2
2
ou on se rappelle que C
P
est la chaleur spécifique a pression constante.
Transformation isotherme
Dans le cas ou la température est constante, on a 0
=
∆
Uet alors la première loi s’écrit :
)ln(
B
B
B
A
B
A
V
V
RTdV
V
RT
pdVWQ
ν
ν
∫∫
====

Cycles thermodynamiques – Moteurs thermiques
Rendement d’une machine thermique
Le rendement d’une machine thermique est défini comme le rapport entre le travail
mécanique utile (produit) dans le cycle, et la chaleur d’entrée Q
entree
.
entree
Q
W
=
η
Comme après un cycle complet on revient au même état du système, pour un cycle on a
0
=
∆
totale
U
et alors
sortieentreetotale
QQQW
−
=
=
. Dans ce cas, on voit que
11 <−==
entree
sortie
entree
Q
Q
Q
W
η
Alors, le rendement de tout moteur thermique est inferieur à l’unité. Mais, en plus, on verra
qu’il est même plus limite que ca !!
Cycle CARNOT
Le cycle idéal, avec l’efficacité (le rendement) maximum pour tout moteur qui fournit du
travail mécanique a partir de deux réservoirs de température (T
f
et T
c
>T
f
), est constitue de
deux isothermes et deux adiabates et a été invente par Sadi Carnot.
 6
6
1
/
6
100%