P2-UE8-Poubeau-Les_antiviraux (word)

1
UE8 – De l’agent infectieux à l’hôte
Date : 20/04/2016 Plage horaire : 10h45-12h45
Promo : 2015/2016 Enseignant : Dr POUBEAU
Ronéistes : Arnaudleplusbeau GUBEREK
Chloé VILLARET Les Antiviraux
I. Généralités
1. Introduction
2. La chimiothérapie antivirale
A. Développement des antiviraux
B. Cible des antiviraux
C. Limite de la chimiothérapie antivirale
II. Les anti-herpétiques
1. Les infections à HSV
2. Les infections à VZV
A. L’Aciclovir
B. Le Valaciclovir
C. Le Famciclovir
3. Les infections à CMV
A. Le Ganciclovir
B. Le Valganciclovir
C. Le Foscarnet
D. Le Cidofovir
III. La grippe
1. Les inhibiteurs de la protéine M2
2. Les inhibiteurs de la neuraminidase
IV. Les hépatites virales : traitements du VHC
1. Les interférons
2. La Ribavirine
3. Le Télaprévir
4. Le Bocéprivir
5. Nouveaux traitements
V. Les hépatites virales : traitements du VHB
1. La Lamivudine
2. L’Adéfovir
3. Telvibudine
4. L’Entécavir
5. Le Ténofovir
Ce qui apparaît en gris dans la ronéo n’a pas été cité par le professeur, cependant ce sont des informations
présentes sur le pdf du cours…

2
I. Généralités
1. Introduction
La plupart des infections virales guérissent spontanément : on n’a pas toujours besoin de traitement. Au
cours de la plupart des infections virales, les signes cliniques apparaissent après que le virus se soit multiplié
dans les cellules et que les lésions se soient constituées (diagnostic tardif).
Ce qu’il faut savoir pour les antiviraux, c’est qu’on a peu de molécules : la thérapeutique antivirale
progresse avec lenteur, cependant le nombre de médicaments antiviraux a fortement progressé au cours des
dernières années, principalement en réponse au développement du SIDA.
Le développement lent et difficile de la chimiothérapie antivirale est du à 3 propriétés intrinsèques des
virus : - Leur parasitisme intracellulaire strict (il n’est pas toujours facile de trouver des molécules qui
rentrent facilement dans les cellules)
- Leur incapacité à s’auto-répliquer
- Leur diversité (virus à ADN, à ARN)
2. La chimiothérapie antivirale
La chimiothérapie va se heurter à 3 obstacles:
- L’interférence avec le métabolisme cellulaire normal (risque de cytotoxicité de certaines molécules)
- La variabilité génétique des virus (surtout les virus à ARN)
- Son incapacité à éradiquer l’infection virale latente (ex du zona et de la varicelle)
Les antiviraux ont une action virostatique et non virucide ! (ex du VIH : on ne tue pas le virus, on tente de
contrôler sa multiplication). On a développé pas mal de vaccins contre les virus (on a assisté à une
diminution des maladies virales), donc on a eu moins de recherche sur les antiviraux.
A. Développement de la chimiothérapie antivirale
La chimiothérapie antivirale a été grandement facilitée par l’avènement des techniques de biologie
moléculaire, en particulier la compréhension des cycles de multiplication virale. Ce qui fait qu’on connaît
mieux les enzymes virales et qu’on a des cibles spécifiques. Mais surtout, on a des techniques de diagnostic
rapide (notamment PCR) qui ont été élaborées et qui permettent la prescription précoce d’une thérapeutique
antivirale adéquate favorisant ainsi son efficacité.
Avant on n’avait que la sérologie, il fallait attendre en général 3 semaines avant d’avoir une idée du stade
de développement de la maladie donc on instaurait les traitements un peu à l’aveugle en espérant que ça
marche. Aujourd’hui des techniques permettent de mesurer la charge virale et donc de savoir beaucoup
plus rapidement si un traitement est efficace ou non.
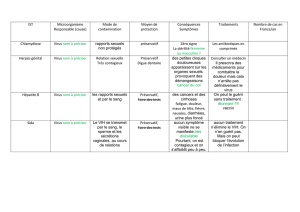
Voici une liste des maladies pour lesquelles on dispose ou non de traitements antiviraux :
Mais on n’a pas de traitement pour la plupart des maladies infections virales (Ebola : pas de traitement).
Dans ce cas, on a un traitement symptomatique.

3
B. Cible des antiviraux
Le cycle de réplication virale se décompose en 6 étapes :
- Attachement du virus sur des récepteurs de la membrane cellulaire
- Pénétration (endocytose, fusion)
- Décapsidation et libération du génome viral
- Réplication (transcription et traduction des protéines précoces de régulation, suivi de la synthèse des
acides nucléiques viraux et de la production des protéines virales tardives structurales)
- Assemblage et la maturation des nouveaux virus
- Libération des virions néoformés
Ces 6 étapes sont des cibles potentielles pour les molécules antivirales :
Quelques exemples :
Ici il a rajouté une
diapositive pour nous
montrer comment un
virus fait pour rentrer
dans une cellule, on
peut voir qu’il y a des
ADN/ARN polymérase
(virus à ADN ou à
ARN), des intégrases,
des transcriptases, etc...
Tout un tas d’enzyme
qui constituent autant
de cibles potentielles.
Précisions sur le fonctionnement des antiviraux sur les étapes du cycle de réplication virale (il n’insiste pas):
- l’attachement (ici on va agir en saturant les récepteurs viraux à la surface de la cellule) :
• On peut avoir des oligopeptides reproduisant une partie de la séquence de la gp120 du VIH et donc qui
empêche l’attachement du virus à la cellule.
• D’autres oligopeptides reproduisant une partie de la séquence de l’hémaglutinine des virus de la grippe.
- la pénétration :
• Pour le virus de la grippe : L’amantadine (Mantadix), une amine cyclique bloque l’activité de la
protéine M2 prophylaxie de la grippe et des infections respiratoires dues au virus de la grippe A. Elle
est inactive sur les virus influenza B (les nouvelles molécules agissent sur ce groupe B).

4
• Pour le VIH, on distingue 3 étapes:
=> Liaison de la gp120 du virus à la protéine CD4 située à la surface cellulaire
=> Liaison de la gp120 à un corécepteur, le CCR5 ou le CXCR4
=> Fusion entre la membrane cellulaire et la membrane virale, faisant intervenir la protéine virale
gp41.
Ex : L’inhibition est possible par les inhibiteurs de la fusion (T20: Enfuvirtide) et anti récepteurs
CCR5. Les 29 pages de la ronéo sur les antis rétro viraux décrivent très bien tout ceci.
- la réplication : la plupart des antiviraux actuels agissent sur cette étape (la réplication du génome utilise
parfois des enzymes d’origine virale qu’on ne trouve donc qu’à l’intérieur des cellules infectées). C’est le
cas en particulier des molécules dirigées contre les virus à ARN (VIH) avec les transcriptases, mais aussi
contre les gros virus à ADN comme l’herpès virus ainsi que les adénovirus.
- l’intégration (« 7ème étape ») : certains virus insèrent leur génome dans celui de la cellule-hôte, cette
insertion pouvant constituer une étape obligatoire de leur cycle de multiplication, comme dans le cas des
rétrovirus. Donc pour les rétrovirus on retrouve des anti-intégrases. Ça se voit aussi dans le cas des
papillomavirus, des herpès virus ou du virus de l'hépatite B.
- l’assemblage et la maturation de nouveaux virions = morphogénèse virale : de nombreuses protéines
virales sont synthétisées sous forme de précurseurs géants qui sont ensuite découpés en protéines de
structure ou en enzymes par une protéase virale. Les inhibiteurs de protéases virales empêchent
l’assemblage et la maturation des virions et la cellule infectée ne produit plus que des virions défectifs.
C. Limite de la chimiothérapie antivirale
La majorité des antiviraux exercent une action sélective et ciblée sur les composants viraux (action à spectre
étroit). Si on les utilise mal (doses suboptimales d’antiviral avec des traitements prolongés, répétés et/ou mal
adaptés) il peut y avoir émergence de virus résistants. Cette résistance est observable sur les antirétroviraux
et antiherpétiques.
De plus, du fait de ce spectre étroit, il est nécessaire d’avoir un diagnostic étiologique très précis (herpès,
VIH, CMV, etc) et rapide pour avoir une action thérapeutique (≠ des ATB à large spectre) ! Souvent, on a
notre diagnostic en rétrospectif… On a également des difficultés à contrôler la réplication virale à haut
niveau (VIH : on y arrive au bout d’un mois avec les anti-protéases mais parfois la CV n’est détectable
qu’au bout de 3 à 6 mois) et il y a certaines maladies qu’on ne peut pas éradiquer du fait de l’infection
latente (VIH avec les réservoirs et Varicelle avec le zona).
La chimiothérapie présente aussi une toxicité cellulaire, surtout si on utilise des antiviraux toxiques à forte
dose (sauf aciclovir: remarquable index thérapeutique avec une efficacité antivirale puissante et une toxicité
minimale). Se pose également le problème du coût (PVD) : les molécules antivirales en général (aciclovir)
sont très chères (bien plus chères que les ATB) et enfin le problème de l’émergence de la résistance.
II. Les anti-herpétiques
1. Les infections à HSV (pas très important juste retenir qu’on traite les formes graves et les IDs)
On a l’herpès buccal : HSV-1 et génital : HSV-2.
=>HSV-1 :
– Tropisme bouche, œil, cerveau
– 67% des adultes
– Acquisition enfants, jeunes adultes par voie salivaire
=>HSV-2 :
– Tropisme sphère génitale, méninges
- 17% des adultes

5
Infection à HSV-1
On voit sur ces photos une gingivo-stomatite, une récurrence labiale (bouton de fièvre), des formes très
évoluées : syndrome de Kaposi-Juliusberg. On a aussi des formes systémiques comme la méningo-
encéphalite herpétique (enfant : primo-infection ; adulte : 2/3 sérologie+ = réactivation ou réinfection
exogène). On peut également avoir des kérato-conjonctivite et des herpès néonataux.
Chez l’immuno-déprimé (en gros c’est chronique et plus grave)
– Récurrences++
– Mucite, œsophagite
– Pneumonie
– Hépatite cytolytique lors des virémies
Infection à HSV-2 (gros problème de santé publique)
• Herpès génital
– Primo-infection
– Infection initiale non primaire (protection partielle par Ac anti-HSV-1)
– Récurrences (immunodéprimé++)
– Excrétion génitale asymptomatique
• Méningite, méningo-radiculite
• Hépatite chez la femme enceinte
Donc globalement les antiviraux vont être utilisés dans les formes graves ou chez l’immunodéprimé. Dans
les infections plus banales à herpès on n’utilise pas ce genre de médicaments.
2. Les infections à VZV (les détails des pathologies et les complications ne sont pas très
importants, c’est surtout à titre indicatif)
La varicelle est un virus proche de l’HSV. Elle est relativement fréquente (600 000
cas/an en France) et bénigne, mais elle peut devenir grave chez une personne
immunodéprimée. On a des complications dans 3 à 5% des cas (0,2% nécessitent une
hospitalisation). Ces complications peuvent être bactériennes (1 à 4%) (Surinfection
cutanée, cellulite, arthrite, otite, pneumopathie) ou virales (cérebellite, méningo-
encéphalite, syndrome de Reye, pneumopathie interstitielle).
➔ Elle ne nécessite pas de traitement, sauf chez les immunodéprimés.
Le zona est une réactivation du virus varicelle/zona, souvent à l’occasion d’une immunodépression et est
plutôt rencontré chez les sujets âgés. On peut utiliser des traitements pour diminuer les douleurs et
l’évolution des éruptions cutanées. Attention, le zona est unilatéral ! Anecdote : il existe un vaccin.
- Douleur: habituellement le premier signe
• absente dans 5 à 10 % des cas
• peut être présente sans éruption
• souvent vive, en éclair, à type de brûlure
• modérée à intense dans 80 % des cas
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%