Partie II Propriétés optiques des tissus Fluorescence Fluorophores

68
Partie II Propriétés optiques des tissus Fluorescence
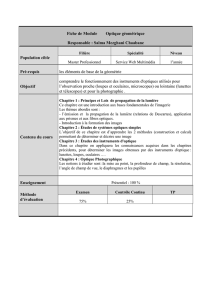
Fluorophores intrinsèques dans les tissus biologiques
Biomedical optics, Lihong V.W Wiley Ed 2007
?

69
Partie II Propriétés optiques des tissus Fluorescence
Pourquoi observet-on des spectres d’émission continus?
Les probabilités de transition d’un état
vibratoire de l’état So vers un état
vibratoire de l’état S1 suivent le
principe de Franck-Condon
Distribution de probabilité
des électrons dans les états
vibratoires des niveaux S1 et
S0
Spectre d’émission de la fluorescence
= histogramme des probabilités de transition
de l’état basal de S1vers les différents états
vibratoires de S0

70
Partie II Propriétés optiques des tissus Fluorescence
Pourquoi les spectres d’absorption et d’émission sont ils symé
triques?
La structure des niveaux d’énergie autorisés pour les deux états S0 et S1 est identique
pour de nombreux fluorophores, par conséquent comme les même règles gouvernent les
probabilités de passage de l’état basal s0 vers un état excité ou le retour de S1 vers un
des états vibratoires de S0 les spectres d’absorption est d’émission sont globalement
symétriques

71
Partie II
Propriétés optiques des tissus
Contrôle des propriétés optiques des tissus ?
Enjeu principal: augmenter la transparence des tissus
-Possibilité d’augmenter la transmission de la lumière par compression ou
étirement des tissus (Mécanisme = diffusion du sang et de l’eau hors de la
zone comprimée)
-Application locale de glucose, propylene glycol, polyethylene glycol,
Verografin….(Mécanisme = diminution de la diffusion par adaptation d’indice
entre le milieu et les diffuseurs)
-Effets thermiques :si T°C augmente la taille et la forme des diffuseurs peut
etre modifiée; si changement non uniforme de température on peut observer
des changements d’indice locaux
-Adaptation d’indice par injection sous cutanée d’eau /glucose pour favoriser
la pénétration de la lumière à l’interface air/peau
Méthodes encore très prospectives

72
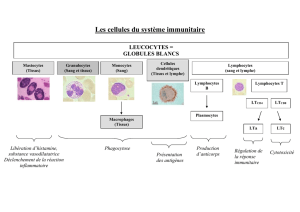
1- Les tissus biologiques = milieu très diffusant et absorbant.
2- Les principales sources d’absorption sont l’eau, le sang, la mélanine.
Les principales sources de diffusion sont les membranes (lipides), les mitochondries,
les noyaux des cellules, les fibres de collagènes.
3- Les propriétés optiques des tissus sont fortement dépendantes de la longueur d’onde.
4- L’absorption dans les tissus est la plus faible dans une fenêtre spectrale entre 450 et 850
nm.
5- Dans les tissus certains molécules sont naturellement fluorescentes et donne lieu au
phénomène d’autofluorescence
6- Certaines structures ordonnées (fibres) des tissus peuvent modifier la polarisation de
la lumière.
7- La propagation des photons lumineux dans les tissus est très anisotropique.
Partie II Propriétés optiques des tissus Résumé et Conclusions
Propriétés optiques des tissus : points clés
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
1
/
48
100%