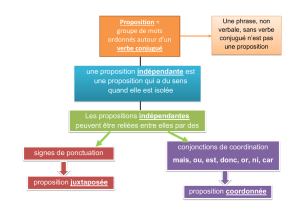
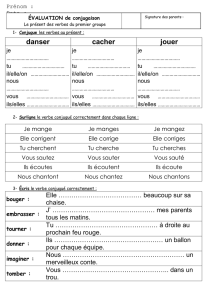
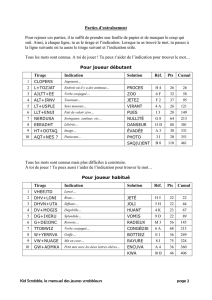
DCM045-7 T4 CE_fr

T4 pour analyses de routine
Détermination immunoenzymatique directe de la T4 dans le sérum ou le plasma humain
Voir l’étiquette externe Σ = 96 tests RÉF DKO045
USAGE PRÉVU
Méthode immunoenzymatique colorimétrique par
compétition pour la détermination quantitative de la
concentration de la T4 dans le sérum ou le plasma
humain.
Le kit T4 est destiné exclusivement à un usage en
laboratoire.
1. SIGNIFICATION CLINIQUE
L'hormone thyroïdienne, la thyroxine (T4), est
produite par la thyroïde. L'iode est un composant
important de la synthèse. La forme principale des
hormones thyroïdiennes dans le sang est la thyroxine
(T4). La thyroxine est convertie en T3 active (trois à
quatre fois plus puissante que la T4) à l'intérieur des
cellules par les déiodinases (5'- iodinase).
La globuline liant la thyroxine (TGB) est la protéine
porteuse de l'hormone thyroïdienne circulante. Seule
une fraction très petite de l'hormone est libre - T4
0,03%. Les hormones thyroïdiennes agissent sur
l'organisme de façon à augmenter le métabolisme
basal, elles affectent la synthèse protéique et elles
augmentent la sensibilité du corps aux
catécholamines (comme l'adrénaline). Les hormones
thyroïdiennes sont essentielles au développement et
à la différenciation des cellules du corps humain. Ces
hormones régulent de plus le métabolisme des
protéines, des graisses et des carbohydrates ; elles
sont impliquées dans la régulation de l'utilisation des
résidus énergétiques de la part des cellules. Les
stimuli physiologiques et pathologiques influencent la
synthèse de l'hormone thyroïdienne.
Les hormones thyroïdiennes agissent à travers un
mécanisme inconnu afin d'inhiber l'activité neuronale ;
l'un des effets est la chute de la température
corporelle. Tant la T3 que la T4 sont employées dans
le traitement de la carence des hormones
thyroïdiennes (hypothyroïdie).
La mesure des concentrations totales de la T3 du
sérum est un étalon et une épreuve confirmée du bon
fonctionnement de la thyroïde.
2. PRINCIPE DE LA MÉTHODE
Méthode immunoenzymatique par compétition pour la
détermination de la T4. L'enzyme-T4 conjugué ne doit
présenter aucune liaison mesurable avec les
protéines du sérum, en particulier la TBG et
l'albumine. La méthode suivante a les
caractéristiques ci-dessous. Après avoir ajouté à
l'anti-sérum immobilisé l'enzyme-T4 conjugué et le
sérum contenant l'antigène T4 natif, on obtient une
réaction compétitive entre la T4 native et l'enzyme-T4
conjugué pour un nombre limité de sites de liaison
immobilisés. Une fois l'équilibre atteint, le conjugué lié
à la phase solide est séparé de la fraction de
conjugué libre par décantation ou aspiration.
L'activité du conjugué lié à la phase solide est
inversement proportionnelle à la concentration de
l'antigène libre (T4). En utilisant les étalons avec une
concentration connue d'antigène, il est possible de
construire une courbe sur laquelle on peut interpoler
un échantillon avec une concentration non connue de
T4.
3. RÉACTIFS, MATÉRIAUX ET INSTRUMENTS
3.1. Réactifs et matériaux fournis dans le
coffret
1. Étalons T4 (6 flacons, 1 mL chaque)
STD0 RÉF DCE002/4506-0
STD1 RÉF DCE002/4507-0
STD2 RÉF DCE002/4508-0
STD3 RÉF DCE002/4509-0
STD4 RÉF DCE002/4510-0
STD5 RÉF DCE002/4511-0
2. Contrôle T4 (1 flacon, 1 mL)
La concentration du contrôle est indiqué sur le
certificat de contrôle REF DCE045/4503-0
3. Tampon de conjugué (1 flacon, 12,5 mL)
Tampon rouge, conservateurs et inhibiteurs des
protéines de liaison RÉF DCE002/4501-0
4. Conjugué (1 flacon, 1,4 mL)
T4 conjugué avec de la peroxydase de raifort (HRP)
RÉF DCE002/4502-0
5. Microplaque coatée (1 microplaque sécable)
Anticorps anti-T4 adsorbé sur la microplaque
RÉF DCE002/4503-0
6. Substrat TMB (1 flacon, 15 mL)
H2O2-TMB (0,26 g/L) (éviter le contact avec la peau)
RÉF DCE004-0
7. Solution d'arrêt (1 flacon, 15 mL)
Acide sulfurique 0,15 mol/L (éviter le contact avec la
peau) RÉF DCE005-0
8. Solution de lavage conc. 50X (1 flacon, 20 mL)
NaCl 45 g/L; Tween-20 55 g/L RÉF DCE006-0
IVD
LOT

3.2. Réactifs nécessaires non fournis dans le
coffret
Eau distillée
3.3. Matériaux et instruments auxiliaires
Distributeurs automatiques.
Lecteur pour microplaques (450 nm).
Remarques
Conserver tous les réactifs à 2÷8°C à l'abri de la
lumière.
N'ouvrir le sachet du Réactif 5 (Microplaque Coatée)
qu'après l'avoir ramené à température ambiante et
refermez-le tout de suite après avoir prélevé les
bandes à utiliser ; une fois ouvert, il est stable
jusqu'à la date d'échéance du coffret.
4. AVERTISSEMENTS
• Ce coffret est exclusivement pour usage in vitro et
l'essai doit être exécuté par un personnel expert.
• Utilisez les dispositifs de protection individuelle
prévus pendant toute opération avec les réactifs
fournis.
• Le Chromogène TMB contient un irritant qui peut
être nocif si inhalé, ingéré ou absorbé à travers la
peau. Pour empêcher des lésions, éviter toute
inhalation ou ingestion par la peau ou les yeux et
tout contact cutané ou oculaire.
• La solution d'arrêt est constituée d'une solution
d'acide sulfurique dilué. L'acide sulfurique est
poison et corrosif et peut être toxique s'il est
ingéré. Pour prévenir toute brûlure chimique
possible, éviter le contact avec la peau et les yeux.
• Éviter l'exposition du réactif TMB/H2O2 à la lumière
directe du soleil, aux métaux et aux substances
oxydantes. Ne pas congeler la solution.
• La concentration de thyroxine total dans le sérum
dépend de plusieurs facteurs : de la fonction de la
thyroïde et de sa régulation, de la thyroxine liant la
globuline (TBG) et de la liaison entre thyroxine et
TBG. La concentration de la thyroxine totale est
toutefois insuffisante à elle seule pour surveiller
l'état clinique.
• Les valeurs de la thyroxine totale dans le sérum
peuvent augmenter pendant la grossesse ou suite
à l'administration de contraceptifs oraux. La table
des médicaments interférants et les conditions
dans lesquelles les valeurs de thyroxine totale
sont influencés et ont été remplis par le Journal of
the American Association of Clinical Chemists.
• Ne pas utiliser aux fins du dépistage chez les
nouveaux-nés.
5. PRÉCAUTIONS D'USAGE
• Observer rigoureusement l'ordre des passages
indiqué dans le présent protocole.
• Tous les réactifs doivent être conservés à une
température contrôlée de 2-8°C dans leurs
conteneurs originaux. Les exceptions sont
clairement marqués.
• Avant usage, laisser reposer tous les éléments
des coffrets et les échantillons à température
ambiante (22-28°C) et mélanger avec soin.
• Ne pas échanger des éléments du coffret
provenant de lots différents. Les dates d'échéance
rapportées sur les étiquettes des récipients
d'expédition et sur celles de tous les ampoules
doivent être observées. Ne pas utiliser d'éléments
au-delà de leur date d'échéance.
• Si vous utilisez des équipements automatisés est
de la responsabilité de l'utilisateur de s'assurer
que le kit a été correctement validées.
• Un lavage incomplet ou peu soigné et une
aspiration insuffisante du liquide dans les puits des
tests ELISA peuvent provoquer un manque de
précision et/ou un arrière-plan élevé.
• Il est important de maintenir constants les temps
de réaction dans chaque puits afin d'obtenir les
résultats susceptibles d'être répétés. Le pipetage
des échantillons ne doit pas durer plus de 10
minutes afin d'éviter tout résultat incorrect. S'il se
prolonge au-delà des 10 minutes, il est
recommandé de suivre l'ordre de distribution. Si
vous devez utiliser plus d’une microplaque, il est
conseillé de répéter la courbe dose-réponse.
• L’ajout de la solution de substrat donne lieu à une
réaction cinétique qui est interrompue par l'ajout
de la solution de blocage. Par conséquent, il est
nécessaire d'ajouter le substrat et la solution
bloquante dans la séquence même afin d'éliminer
toute variation temporelle pendant la réaction.
• Observer les instructions relatives à l'exécution du
contrôle de qualité dans les laboratoires cliniques
en testant les contrôles et/ou les groupes de
sérum.
• Observer la plus grande précision dans la
reconstitution et la distribution des réactifs.
• Ne pas utiliser des échantillons
microbiologiquement contaminés ou des
échantillons hautement lipémiques ou hémolysés.
• Les lecteurs de microplaques mesurent dans le
sens vertical. Ne pas toucher le fond des puits.
6. PROCÉDURE
6.1. Préparation des étalons (S0… ..S5)
Les flacons sont sérum de référence de thyroxine
avec des concentrations approximatives de :
S0 S1 S2 S3 S4 S5
μg/dL
0 2,0 5,0 10,0 15,0 25,0
Les taux exacts sont rapportés dans les étiquettes
pour chaque lot spécifique. Conserver à 2÷8°C. Prêts
à l'emploi.
6.2. Préparation du conjugué dilué
Diluer le conjugué 1:11 avec le tampon de conjugué.
Par exemple, diluer 160 μL dans 1,6 mL de tampon
de conjugué. Utiliser dans les 24 heures pour obtenir
le maximum de performance. Maintenir à une
température de 2÷8°C.
6.3. Préparation de la solution de lavage
Avant l'usage, diluer le contenu de chaque ampoule
de solution de lavage concentrée et tamponnée (50x)
avec de l'eau distillée jusqu'à un volume de 1000 mL.
Pour préparer des volumes moindres, respecter le
rapport de dilution de 1:50. La solution de lavage
diluée est stable à 2÷8°C pendant au moins 30 jours.

6.4. Préparation de l'échantillon
Recueillir l'échantillon au moyen d'une seringue de 10
mL dans des tubes de silicone. Observer les
précautions habituelles dans le recueil des
échantillons. Séparer les cellules de globules rouges
par centrifugation et utiliser le sérum pour la
détermination de la T4. Les échantillons peuvent être
réfrigérés à 2÷8°C (pendant une période maximale de
48 heures). Le conserver jusqu'à 30 jours à -20 °C s'il
ne peut pas être testé dans les 48 heures. Pour des
tests en double, 0,050 mL d'échantillon sont
nécessaires.
6.5. Procédure
Amener tous les réactifs, sérums de référence et
contrôles à température ambiante (22÷28°C).
Réactif Étalon Échantillon
/Contrôle Blanc
Échantillon
/Contrôle 25 μL
Étalon S0-S5 25 μL
Conjugué
dilué 100 μL 100 μL
Laisser incuber 1 heure à température ambiante
(22÷28°C). Retirer le contenu de chaque puits, laver
les puits trois fois avec 300 μL de solution de lavage
diluée.
Substrat
TMB 100 μL 100 μL 100 μL
Laisser incuber à température ambiante (22÷28°C),
pendant 15 minutes à l'abri de la lumière
Solution
d'arrêt 100 μL 100 μL 100 μL
Agiter doucement la microplaque.
Lire l'absorbance (E) à 450 nm contre le blanc dans
les 30 minutes après l'ajout de la solution d'arrêt
7. CONTRÔLE DE QUALITÉ
Chaque laboratoire devrait tester les contrôles avec
des taux d'hypothyroïde, d'euthyroïde et
d'hyperthyroïde pour surveiller les performances du
coffret. Ces contrôles doivent être traités comme
inconnus et les valeurs déterminées dans chaque
session.
Les tableaux de contrôle de la qualité devraient être
observés afin de suivre les prestations des réactifs
fournis. Des méthodes statistiques appropriées
doivent, de plus, être utilisées pour vérifier la
tendance. Chaque laboratoire devrait choisir les
limites d'acceptabilité des performances du coffret.
Les autres paramètres incluent les interceptions à 80,
50 et 20% de la courbe d'étalonnage pour la
reproductibilité inter-essai. De plus, l'absorbance
maximale devrait refléter les valeurs des séances
précédentes. Des déviations significatives par
rapport aux prestations établies peuvent indiquer une
altération inobservée des conditions expérimentales
ou une dégradation des réactifs du coffret. Utiliser
des réactifs frais pour déterminer les motifs des
variations.
7.1. Interprétation des résultats
Si un ordinateur a été utilisé pour calculer les
résultats, il faut impérativement que les valeurs des
calibrateurs tombent dans les 10% des
concentrations assignées.
8. RÉSULTATS
8.1. Remarques
Absorbance (S0) = > 1,0A.
8.2. Extinction moyenne
Calculer l'extinction moyenne (Em) de chaque point
de la courbe d'étalonnage (S0–S5) et de chaque
échantillon.
8.3. Courbe d'étalonnage
Sur un graphique des valeurs d'absorbance, tracer
les valeurs calculées des extinctions moyennes (Em)
de chaque étalon (S0–S5) en fonction des
concentrations. Tracer la meilleur courbe passant par
les points d'étalonnage (par ex. : tracé logistique à
quatre paramètres).
8.4. Calcul des résultats
Sur le graphique, faire une interpolation des valeurs
d'absorbance relatives à chaque échantillon et en lire
la concentration correspondante en μg/dL.
9. VALEURS DE RÉFÉRENCE
Une étude de population adulte euthyroïde a été
utilisée pour déterminer les valeurs prévues pour le
coffret EIA T4.
Moyenne
(μg/dL) SD Plage
(μg/dL)
Valeurs
normales 7,6 1,6 4,4 - 10,8
10. PARAMÈTRES CARACTÉRISTIQUES
10.1. Précision
10.1.1. Intra-essai
La variabilité à l'intérieur du même coffret a été
déterminée en répliquant (20x) la mesure de trois
contrôles différents. La variabilité intra-essai est ≤
8,16%. 10.1.2. Inter-essai
La variabilité entre dosages différents a été
déterminée en répliquant (10x) la mesure de trois
contrôles différents avec des coffrets appartenant à
des lots différents. La variabilité inter-essai est ≤
8,42%.
10.2. Exactitude
L'épreuve de récupération conduite sur des
échantillons enrichis avec 1,25 - 2,50 - 5,00 - 10,00
μg/mL de T4 a donné une valeur moyenne (±SD) de
97,8% ± 5%.

10.3. Sensibilité
La concentration minimale de T4 mesurable qui
pouvant être distinguées par l'étalon zéro est de 0,4
μg/dL avec une limite de confiance de 95%.
10.4. Spécificité
La réactivité croisée de l'anti-thyroxine avec certaines
substances a été déterminée en ajoutant les solutions
interférantes à une matrice de sérum à diverses
concentrations. La réactivité croisée a été calculée en
analysant le rapport entre la concentration de
substances interférantes et la concentration de
thyroxine nécessaire pour déplacer la même quantité
de conjugué.
Substance Réactivité
croisée Concentration
I-Thyroxine 1,0000 -
d-Thyroxine 0,9800 10 µg/dL
l-triiodothyronine 0,0300 100 µg/dL
d-triiodothyronine 0,0150 100 µg/dL
Monoiodo-Tyrosine N/D 100 µg/mL
Diiodo-Tyrosine N/D 100 µg/mL
Acide
triiodothyroacétique N/D 100 µg/mL
Acide
tétraiodothyroacétiq
ue 0,0001 100 µg/mL
10.5. Corrélation avec le dosage RIA
Le coffret de T4 (Diametra) a été comparé avec un
coffret disponible en commerce. 114 échantillons de
sérum ont été testés. La courbe de régression est :
(T4 Diametra) = 0,959*(T4 RIA) + 0,339
r2 = 0,936
11. DISPOSITIONS RELATIVES À L'ÉLIMINATION
DES DÉCHETS
Les réactifs doivent être jetés conformément aux lois
en vigueur.
BIBLIOGRAPHIE
1. Barker, S.B.,”Determination of Protein Bound
Iodine”Journal Biological Chemistry, 173, 175 (1948).
2. Chopra, I.J., Solomon, D.H., an Ho, R.S.,”A
Radioimmunoassay of Thyroxine, “J.Clinical
EndocrinoL, 33, 865 (1971).
3. Young, D.S., Pestaner, L.C., and Gilberman,
U.,”Effects of Drugs on clinical Laboratory Tests.”
Clinical Chemistry, 21, 3660 (1975).
4. Sterling, L., Diagnosis and Treatment of Thyroid
Disease, Cleveland CRC press, P.19-51 (1975).
Éd 07/2011 DCM045-7
DiaMetra S.r.l. - Siège social : Via Garibaldi, 18 –
20090 SEGRATE (MI) Italie
Tél. 0039-02-2139184 – 02-26921595
Fax 0039–02–2133354.
Fabricant : Via Giustozzi 35/35a – Z.I Paciana –
06034 FOLIGNO (PG) Italie
Tél. 0039-0742–24851
Fax 0039–0742–316197
Courriel : [email protected]

DIA.METRA SRL
Mod. PIS
NOTICE D'INFORMATION
Spiegazione dei simboli Explanation of symbols Explication des symboles Significado de los simbolos
Verwendete Symbole Explicaçao dos simbolos
DE
ES
FR
GB
IT
PT
In vitro Diagnostikum
Producto sanitario para diagnóstico In vitro
Dispositif medical de diagnostic in vitro
In vitro Diagnostic Medical Device
Dispositivo medico-diagnostico in vitro
Dispositivos medicos de diagnostico in vitro
DE
ES
FR
GB
IT
PT
Hergestellt von
Elaborado por
Fabriqué par
Manufacturer
Produttore
Produzido por
REF
DE
ES
FR
GB
IT
PT
Bestellnummer
Nûmero de catálogo
Réferéncès du catalogue
Catalogue number
Numero di Catalogo
Número do catálogo
yyyy-mm
DE
ES
FR
GB
IT
PT
Herstellungs datum
Fecha de fabricacion
Date de fabrication
Date of manufacture
Data di produzione
Data de produção
yyyy-mm-dd
DE
ES
FR
GB
IT
PT
Verwendbar bis
Establa hasta (usar antes de último día del mes)
Utiliser avant (dernier jour du mois indiqué)
Use by (last day of the month)
Utilizzare prima del (ultimo giorno del mese)
Utilizar (antes ultimo dia do mês)
DE
ES
FR
GB
IT
PT
Biogefährdung
Riesco biológico
Risque biologique
Biological risk
Rischio biologico
Risco biológico
DE
ES
FR
GB
IT
PT
Gebrauchsanweisung beachten
Consultar las instrucciones
Consulter le mode d’emploi
Consult instructions for use
Consultare le istruzioni per l’uso
Consultar instruções para uso
DE
ES
FR
GB
IT
PT
Chargenbezeichnung
Codigo de lote
Numero de lot
Batch code
Codice del lotto
Codigo do lote
Σ = xx
DE
ES
FR
GB
IT
PT
Ausreichend für “n” Tests
Contenido suficiente para ”n” tests
Contenu suffisant pour “n” tests
Contains sufficient for “n” tests
Contenuto sufficiente per “n” saggi
Contém o suficiente para “n” testes
DE
ES
FR
GB
IT
PT
Inhalt
Contenido del estuche
Contenu du coffret
Contents of kit
Contenuto del kit
Conteúdo do kit
Max
Min
DE
ES
FR
GB
IT
PT
Temperaturbereich
Límitaciôn de temperatura
Limites de température de conservation
Temperature limitation
Limiti di temperatura
Temperaturas limites de conservação
Cont.
IT
GB
FR
PT
ES
DE
 6
6
1
/
6
100%