DE L`ATOME À L`UNIVERS

62 LIVRE DU PROFESSEUR
© Éditions Belin, 2011
A. Le programme
Notions et contenus Compétences attendues
La matière à différentes échelles : du noyau à
la galaxie.
Particules élémentaires : électrons, neutrons,
protons.
Charge élémentaire e.
Interactions fondamentales : interactions forte
et faible, électromagnétique, gravitationnelle.
Cohésion du noyau, stabilité.
Connaître les ordres de grandeur des
dimensions des différentes structures des
édifi ces organisés.
Connaître l’ordre de grandeur des valeurs des
masses d’un nucléon et de l’électron.
Savoir que toute charge électrique peut
s’exprimer en fonction de la charge
élémentaire e.
Associer, à chaque édifi ce organisé, la ou les
interactions fondamentales prédominantes.
Utiliser la représentation symbolique Z
AX ;
défi nir l’isotopie et reconnaître des isotopes.
Commentaires ✔
Ce chapitre reprend un certain nombre de notions abordées en classe de seconde. À l’échelle
du noyau et de l’atome, les ordres de grandeur des dimensions et la valeur de la charge élémen-
taire sont introduits. Ce chapitre charnière introduit également les interactions fondamentales
– autres que l’interaction gravitationnelle, qui a été étudiée en seconde – indispensables à
l’étude de la radioactivité, au chapitre 8, en physique, et à la compréhension de la notion de
polarité des molécules et des propriétés qui en découlent ainsi que de la cohésion des solides
moléculaires, abordées en chimie, notamment au chapitre 9.
B. Commentaires sur les activités et documents proposés
Évaluer les acquis de la 2
de p. 134
Réponses aux questions ✔
– Dans les atomes, qui constituent la matière, les électrons se déplacent autour d’un noyau, et
l’espace où ces électrons se déplacent est vide.
– Les composants du noyau de l’atome (protons et neutrons) sont appelés nucléons. Un élé-
ment chimique est caractérisé par son numéro atomique, c’est-à-dire le nombre de protons pré-
sents dans son noyau.
Chapitre 7
DE L’ATOME À L’UNIVERS
5908_LDP_07.indd 15908_LDP_07.indd 1 13/09/11 17:35:0413/09/11 17:35:04

7. DE L’ATOME À L’UNIVERS 63
© Éditions Belin, 2011
Interpréter une expérience p. 134
– Des expériences de triboélectricité peuvent être réalisées en petits groupes en classe.
Prévoir : des tiges en verre, des règles en plexiglas ; des bouts de tissus en laine, soie, coton, nylon ;
des sachets plastique, feuilles d’aluminium, morceaux de polystyrène, confettis, etc. En frottant
entre eux deux matériaux, les élèves mettent en évidence la présence de charges électriques dans
la matière, observent et interprètent l’interaction entre les corps chargés obtenus après frottement.
On peut interroger les élèves sur la nature probable des charges en jeu, sur leur provenance.
Interprétation attendue ✔
– L’interaction électrostatique entre le verre et la fi celle, attractive, contrarie l’interaction gravi-
tationnelle entre la Terre et la fi celle.
Activité 1 p. 136
Cette activité sur les ordres de grandeur s’appuie sur un document décrivant les dimensions
des objets célestes, sur une recherche documentaire pour les objets plus petits que la taille de
l’homme, et enfi n sur un texte de Lévy-Leblond qui fait le lien entre l’infi niment grand et l’infi -
niment petit.
Réponses aux questions ✔
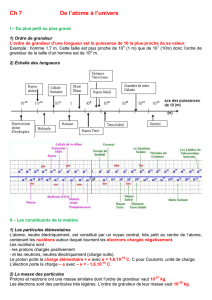
1. D’après le document 1, on détermine les ordres de grandeur suivants :
a. diamètre de la Terre : 107 m ;
b. extension du Système Solaire : 1013 m ;
c. taille d’une galaxie : 1021 m.
2. Grâce à une recherche documentaire, on détermine les ordres de grandeur suivants :
a. taille du plus petit objet discernable à l’œil nu : 10−4 m ;
b. taille d’une molécule : 10−8 m (ADN) ;
c. taille d’un atome : 10−10 m ;
d. taille du noyau d’un atome : 10−15 m.
3. Le nombre d’Avogadro NA est une estimation du nombre d’entités dans un échantillon conte-
nant une mole d’une espèce donnée. Sa valeur est environ NA = 6,02 · 1023 mol−1. Cette constante
est couramment utilisée en chimie pour dénombrer les atomes et les molécules d’une substance.
4. a. 10−10 ×107=3,3 ⋅ 10−2 m soit de l’ordre du centimètre.
b. C’est un peu plus petit que la taille d’un homme, qui est de l’ordre du mètre.
5.
Galaxie
Système solaire
Terre
Homme
Atome
Ordre de grandeur (m)
Noyau atomique
Molécule d’ADN
Plus petit objet observable à l’œil nu
10-15 10-10 10-51001051010 1015 1020 1025
5908_LDP_07.indd 25908_LDP_07.indd 2 13/09/11 17:35:0413/09/11 17:35:04

64 LIVRE DU PROFESSEUR
© Éditions Belin, 2011
Activité 2 p. 137
Dans un premier temps, les dimensions des différents constituants de l’atome sont dis-
cutées. En particulier, on s’interrogera sur la possibilité de représenter sur un même schéma
l’atome et son noyau. Les caractéristiques (nombre, charges et masses) de ces constituants font
l’objet d’une seconde étude.
Réponses aux questions ✔
1. L’atome est constitué d’électrons et de nucléons (neutrons et protons).
2. Le nuage électronique a un diamètre de l’ordre de 10−10 m et le noyau de 10−15 m.
3. 10−2/10−15 = 1013 noyaux
4. a. La masse est concentrée dans le noyau car un nucléon est environ 1 830 fois plus lourd
qu’un électron.
b. D’après la question 2., le rapport des volumes de l’atome et du noyau vaut :
(10−10)3/(10−15)3 = 1015.
c. Comme la masse est concentrée dans le noyau, d’après la question 4. a, le rapport des den-
sités de l’atome et du noyau est égal au rapport des volumes : ainsi, d’après la question 4. b, le
noyau est bien 1015 fois plus dense que l’atome.
5. On exploite le fait que deux isotopes radioactifs ont les mêmes propriétés chimiques.
6. La charge électrique est :
a. nulle pour le neutron ; b. +1,6 · 10−19 C pour le proton ; c. −1,6 · 10−19 C pour l’électron ;
d. nulle pour un atome.
7. Nuage électronique Noyau
Diamètre (m) 10−10 m10
−15 m
Masse (kg) presque nulle toute la masse de l’atome
Constituants Électron Neutron Proton
Charge (C) −1,6 · 10−19 0+1,6 · 10−19
8. a. Charge des noyaux : 3 × (1,6 · 10−19) = 4,8 · 10−19 C, identique pour les deux isotopes ;
masse du noyau de 3
7Li : 7 × (1,67 · 10−27) = 1,17 · 10−26 kg ;
masse du noyau de 3
6Li : 6 × (1,67 · 10−27) = 1,00 · 10−26 kg.
b. Charge du nuage électronique : 3 × (−1,6 · 10−19) = −4,8 · 10−19 C ;
Masse :
3 × 1,67 ⋅ 10−27
()
1 830 =2,74 ⋅ 10−30 kg.
Activité 3 p. 138
Cette activité de modélisation est fondée sur un article historique de Robert Millikan, dont
proviennent les valeurs numériques à exploiter (exprimées en coulomb pour plus de simplicité,
contrairement aux valeurs de Millikan obtenues en 1911).
La discussion du protocole expérimental mène les élèves à discerner plusieurs interactions
fondamentales intervenant au cours de la manipulation de Milikan. Le traitement informatisé
des données de Millikan, dans la partie B de l’activité, fait non seulement apparaître la quanti-
fi cation de la charge, mais donne aussi accès à une valeur expérimentale de la charge élémen-
taire, introduite à l’activité précédente.
Réponses aux questions ✔
1. L’interaction gravitationnelle.
2. L’interaction électromagnétique.
5908_LDP_07.indd 35908_LDP_07.indd 3 13/09/11 17:35:0413/09/11 17:35:04

7. DE L’ATOME À L’UNIVERS 65
© Éditions Belin, 2011
3. Δq vaut toujours à peu près 1,6 · 10−19 C (sauf entre la deuxième et la troisième plus grandes
valeurs mesurées : c’est le double).
4. Les nombres entiers correspondent à 4, 5, …, 13, 14, 16, 17.
5. Il s’avère que la charge électrique de toutes les gouttes observées est un multiple entier
d’une quantité constante. Cette quantité, notée e, est appelée charge élémentaire.
Activité 4 p. 139
Les activités précédentes ont introduit les interactions gravitationnelle et électromagnéti-
que et posé la question des distances entre objets, des plus grandes aux plus petites. Cette
dernière activité met en rapport interaction et distance, en proposant l’étude des quatre interac-
tions fondamentales, de leurs caractéristiques et de leur champ d’infl uence.
Les élèves pourront avec profi t être amenés à rechercher dans leur quotidien des exemples
de manifestations des interactions gravitationnelles et électromagnétiques.
Réponses aux questions ✔
1. a. Action entre deux objets.
b. Il y a quatre interactions fondamentales : l’interaction gravitationnelle, l’interaction électro-
magnétique, l’interaction faible et l’interaction forte.
2. a. La masse. b. La charge électrique.
3. Toujours attractive.
4. a. Non : à très courte distance (au sein du noyau uniquement).
b. Non : à très courte distance (au sein du noyau uniquement).
5. a. Interaction gravitationnelle ; b. Interaction forte ; c. Interaction électromagnétique.
6. Elle est associée à la radioactivité.
7. Interaction Portée Édifi ce organisé
Gravitationnelle Infi nie Galaxie
Électromagnétique Infi nie Cristaux de sel
Faible 10−17 m Noyau radioactif β
Forte 10−17 m Noyau atomique
C. Déroulement du cours
On peut compter pour ce chapitre une séances d’activités expérimentales en demi-groupe
d’une heure et deux séances en classe entière.
Exemple de progression :
Travail à la maison • Activités 1 et 2
Remarque : ces activités s’appuient sur des connaissances et savoir-faire
de la classe de seconde et peuvent donc constituer un travail en autonomie
préparatoire à la séance en classe entière.
Cours • Séance en classe entière : 1. La matière à différentes échelles ; 2. Les consti-
tuants de la matière ; exercices d’application (1 h à 1 h 30).
Séance de TP • Séance en demi-groupe : activité 3 (1 h).
Cours • Séance en classe entière : Activité 4 ; 3. Les interactions fondamentales ;
exercices d’application (2 h).
5908_LDP_07.indd 45908_LDP_07.indd 4 13/09/11 17:35:0513/09/11 17:35:05

66 LIVRE DU PROFESSEUR
© Éditions Belin, 2011
D. Réponses aux exercices p. 144
Les réponses aux exercices qui ne fi gurent pas ici sont à la fi n du manuel, p. 352.
13 Le nombre de charge serait alors
N=9 ⋅ 10−19
1,60 ⋅ 10−19 =5,6 , qui n’est pas entier.
Soit la précision sur la charge est insuffi sante,
soit l’information est erronée.
14 1. a. 92
238U.
b. Le noyau contient 238 nucléons dont
92 protons et 146 neutrons.
2. a. 92
235U.
b. 235 nucléons dont 92 protons et 143 neutrons.
3. Ces deux noyaux sont isotopes.
15 1. Il s’agit de l’électron.
2. La charge d’un électron est :
–e = –1,6 · 10−19 C ; il y en a 8.
16 1. Nombre moyen de nucléons contenus
dans le noyau :
3,79 · 10−25/(1,67 · 10−27 ) = 227.
2. Nombre de protons contenu dans son
noyau : Z = 88.
3. Par neutralité de l’atome de radium, le
nombre d’électrons est égal à Z = 88.
4. a. Dans 226Ra : 226 nucléons donc :
226 − 88 = 138 neutrons ;
dans 228Ra : 228 nucléons donc :
228 − 88 = 140 neutrons.
b. Le radium possède 226 nucléons en
moyenne, donc 226Ra est prédominant.
17 1. A = 4,5 · 10−26/1,67 · 10−27 = 27 ;
Z = 20,8/1,6 = 13.
2. 13 protons, 13 électrons et 14 neutrons. (Il
s’agit donc d’un atome d’aluminium Al.)
19 1.
Noyau Nombre de
neutrons
Nombre
de protons
19
39K20 19
19
40K21 19
4 1. a. 430 al.
b. 2,71 107 ua.
c. 4,07 1018 m.
2. 1018 m.
5 Ordres de grandeur :
Atome d’hydrogène : 10−10 m ; Globule rouge :
10−5 m ; Nouveau-né : 100 m ; Sommet du
Mont Everest : 104 m ; Terre : 107 m ; Soleil :
109 m.
6 1. a. 3,3 · 10−5 m ;
b. 4 · 10−10 m ;
c. 2,0 · 10−4 m ;
d. 9,0 · 10−8 m ;
e. 6,5 · 10−11 m.
2. a. 10−5 m ;
b. 10−10 m ;
c. 10−4 m ;
d. 10−7 m ;
e. 10−10 m.
7 1. Le diamètre du Soleil mesure :
D = 1,4 million de km.
2. R = 6,4 · 103/1,4 · 106 = 4,6 × 10−3 m
(c’est-à-dire moins de 5 mm).
3. 1 ua correspond sur la voie verte à
150/1,4 = 107 m.
4. « Mercure » est à 41 m du « Soleil » ; « Jupi-
ter » à 0,56 km ; « Pluton » à 4,2 km.
5. 11 000 × 1,4 · 106 = 15 · 109 km.
6. On pédale longtemps pour voir, de temps
en temps, quelques (11) corps célestes éloi-
gnés les uns des autres.
12 1. 25
55Mn2+ : 25 protons, 55 − 25 = 30 neu-
trons, 25 − 2 = 23 électrons.
2. 53
127I− : 53 protons, 127 − 53 = 74 neutrons,
53 + 1 = 54 électrons.
3. 9
19F− : 9 protons, 19 − 9 = 10 neutrons,
9 + 1 = 10 électrons.
5908_LDP_07.indd 55908_LDP_07.indd 5 13/09/11 17:35:0513/09/11 17:35:05
 6
6
 7
7
 8
8
 9
9
1
/
9
100%