Jumeau acardiaque acéphale : diagnostic prénatal et prise en

Jumeau acardiaque ace
´phale : diagnostic
pre
´natal et prise en charge a
`propos d’un cas
Acardiac headless twin: A case report and review of the
literature
H. Boufettal*,M. Noun, S. Hermas, N. Samouh
Service de gyne
´cologie-obste
´trique « C », CHU Ibn Rochd de Casablanca, Casablanca, Maroc
Disponible en ligne sur
www.sciencedirect.com
1. Introduction
Le jumeau acardiaque ace
´phale, forme particulie
`re du syn-
drome transfuseur-transfuse
´, est un fœtus qui se pre
´sente
sous forme de masse tissulaire informe, avasculaire sans cœur
et sans extre
´mite
´ce
´phalique identifiable. C’est une malfor-
mation rarissime, repre
´sentant moins de 1 naissance sur
35 000, qui se voit exclusivement au cours des grossesses
ge
´mellaires monochoriales, touchant moins de 1 % d’entres
elles [1]. Nous rapportons un cas de fœtus acardiaque ace
´-
phale diagnostique
´en e
´chographie a
`24 semaines d’ame
´nor-
rhe
´e (SA). Un diagnostic ante
´natal pre
´coce est ne
´cessaire
permettant d’organiser un suivi adapte
´, voire d’instaurer
une the
´rapeutique [2–4].
2. Observation
Il s’agissait d’une patiente de 36 ans, sans ante
´ce
´dent patho-
logique particulier, 3
e
geste, 3
e
pare, ayant 2 enfants vivants
Summary
Introduction. Monochorial twin pregnancies are characterised by
the presence of vascular connections between the twins. These
connections can be the cause of pathologies such as the twin-twin
transfusion syndrome or the TRAP syndrome, which is defined as the
association of a headless, acardiac twin with a healthy twin.
Case report. The case of an acardiac, headless twin diagnosed
during pregnancy at 24 weeks of amenorrhea is described.
Discussion. An acardiac headless twin is a rare phenomenon. Yet
early diagnosis is crucial during pregnancy to provide adequate
monitoring. It is associated with a high death rate in the healthy twin
caused by anaemia and heart failure. Therapeutic resources involve
interruption of vascular anostomoses between the twins in order to
perform a selective feticide.
Conclusion. Treatment of acardiac headless twin pregnancy ranges
from obstetric abstentionism to interventionism, which depends on
the prognosis for the healthy twin, dominated by the risk of preterm
birth and heart failure.
ß2009 Published by Elsevier Masson SAS.
Re
´sume
´
Les grossesses ge
´mellaires monochoriales se caracte
´risent par la
pre
´sence de connections vasculaires entre les jumeaux. Ces der-
nie
`res peuvent e
ˆtre a
`l’origine de pathologies comme le syndrome
transfuseur-transfuse
´ou le syndrome TRAP qui se de
´finit comme
l’association d’un jumeau acardiaque ace
´phale et d’un jumeau sain.
Ce syndrome est tre
`s rare et il est associe
´a
`une forte mortalite
´du
jumeau sain par ane
´mie et insuffisance cardiaque. Le diagnostic
ante
´natal est possible permettant la mise en place d’une surveillance
adapte
´e et de moyens the
´rapeutiques visant a
`interrompre les
anastomoses vasculaires entre les jumeaux de fac¸on a
`re
´aliser un
fœticide se
´lectif. La conduite a
`tenir obste
´tricale varie entre l’abs-
tentionnisme et l’interventionnisme, attitude qui de
´pend du pro-
nostic du jumeau sain domine
´par la pre
´maturite
´et l’insuffisance
cardiaque. Nous rapportons un cas de jumeau acardiaque ace
´phale
diagnostique
´en pe
´riode ante
´natale dont le suivi a permis une
e
´volution favorable du jumeau vivant.
ß2009 Publie
´par Elsevier Masson SAS.
Mots cle
´s: Jumeau acardiaque ace
´phale, Grossesse ge
´mellaire
monochoriale, Diagnostic ante
´natal, E
´chographie-Doppler
*Auteur correspondant.
53, rue Allal Ben Abdellah, Centre ville, 20000 Casablanca, Maroc.
e-mail : [email protected]
Rec¸u le :
10 avril 2009
Accepte
´le :
6 novembre 2009
Disponible en ligne
9de
´cembre 2009
Fait clinique
253
0929-693X/$ - see front matter ß2009 Publie
´par Elsevier Masson SAS.
10.1016/j.arcped.2009.11.004 Archives de Pe
´diatrie 2010;17:253-257

ne
´sa
`terme par voie basse. Sa grossesse e
´tait suivie par un
me
´decin ge
´ne
´raliste jusqu’a
`24 SA. L’e
´chographie faite dans le
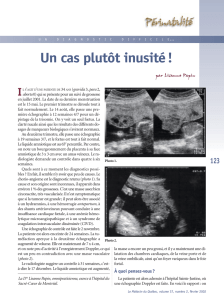
cadre d’un bilan morphologique a
`24 SA avait montre
´un
fœtus vivant et une formation entoure
´e d’une membrane
faisant e
´voquer le diagnostic d’une grossesse ge
´mellaire
monozygote avec un fœtus vivant normal et un second
jumeau acardiaque ace
´phale (fig. 1) pre
´sentant un liquide
amniotique tre
`s abondant (fig. 2). Une e
´chographie de
contro
ˆle a
`28 SA permettait de confirmer le diagnostic de
fœtus acardiaque. Elle montrait une discordance biome
´trique
des 2 jumeaux, un œde
`me sous-cutane
´diffus ou des anoma-
lies morphologiques sur le jumeau mort (fig. 2 et 3), d’autant
plus qu’il s’agissait d’un placenta monochorial biamniotique.
L’examen morphologique du fœtus mort ne trouvait pas de
po
ˆle ce
´phalique ni de structure cardiaque.
La surveillance e
´chographique hebdomadaire constatait la
persistance d’une vascularisation a
`faible de
´bit (fig. 2), compa-
rativement au jumeau donneur et ve
´rifiait l’absence de signes
d’insuffisance cardiaque chez le fœtus donneur, traduisant
une bonne adaptation he
´modynamique. L’œde
`me ge
´ne
´ralise
´
e
´tait devenu majeur au terme de 28 SA et, devant l’apparition
d’un hydramnios, un amniodrainage e
´tait re
´alise
´e
´vacuant
1500 ml a
`33 SA et 2000 ml a
`35 SA. La biome
´trie du fœtus
vivant e
´tait en parfaite concordance avec l’a
ˆge the
´orique a
`
28 SA, avec un diame
`tre biparie
´tal a
`69 mm, une longueur du
fe
´mur a
`52 mm et une estimation du poids fœtal a
`1116 g, sans
anomalie morphologique de
´celable ; l’index de Pourcelot e
´tait
a
`0,61 sur l’arte
`re ombilicale.
En raison de la pre
´sentation transverse du premier jumeau et
de l’aggravation du polyhydramnios, une ce
´sarienne e
´tait
re
´alise
´ea
`36 SA. Cette ce
´sarienne permettait l’extraction
d’un garc¸on vivant pesant 2260 g, avec un score d’Apgar a
`
10/10 a
`la 1
re
min. L’examen du nouveau-ne
´vivant ne montrait
aucune anomalie morphologique. L’extraction du 2
e
jumeau
montrait qu’il s’agissait d’un fœtus de sexe masculin pesant
1770 g et mesurant 28 cm de longueur, ne pre
´sentant pas de
po
ˆle ce
´phalique ni de thorax, se limitant ainsi a
`des membres
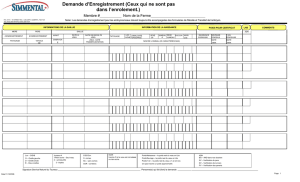
et un petit bassin. A
`la face ante
´rieure, on observait un cordon
ombilical sans relation avec le placenta (fig. 4).
L’examen anatomopathologique du fœtus malforme
´confir-
mait le diagnostic de jumeau acardiaque ace
´phale. Les
2 membres infe
´rieurs comportaient chacun un pied oriente
´
vers l’arrie
`re avec syndactylie. Le cordon du fœtus acar-
diaque contenait une arte
`re ombilicale unique et s’inse
´rait
sur celui du fœtus donneur. Il n’e
´tait pas identifie
´de struc-
ture cardiaque, ni de syste
`me veineux cave normal ; en
revanche, il existait une aorte avec 2 branches a
`ses extre
´-
mite
´sce
´phalique et caudale. Les organes ge
´nitaux e
´taient
en position normale et correspondaient a
`un pe
´nis malforme
´
(fig. 4).
L’examen du placenta qui pesait 670 g montrait qu’il s’agis-
sait d’un placenta monochorial biamniotique. On retrouvait
bien l’insertion placentaire du cordon ombilical du jumeau
H. Boufettal et al. Archives de Pe
´diatrie 2010;17:253-257
Figure 1. E
´chographie a
`24 semaines d’ame
´norrhe
´e : masse tissulaire sans
activite
´cardiaque.
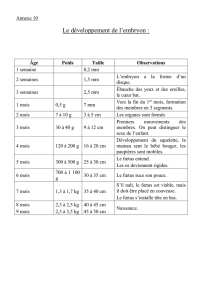
Figure 2. E
´chographie a
`28 semaines d’ame
´norrhe
´e : fœtus acardiaque
avec liquide amniotique tre
`s abondant et pre
´sence d’une vascularisation
a
`faible de
´bit.
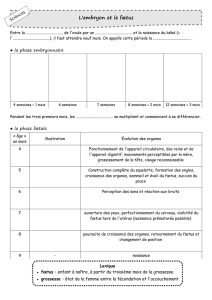
Figure 3. E
´chographie a
`28 semaines d’ame
´norrhe
´e : anomalies
morphologiques avec absence de structure cardiaque chez le fœtus
acardiaque.
254

sain mais pas celle du jumeau malforme
´. L’examen des
membranes, du cordon et du placenta ne montrait pas d’ano-
malie.
3. Discussion
Le fœtus acardiaque ace
´phale est une malformation raris-
sime, qui se rencontre exclusivement dans les grossesses
ge
´mellaires monozygotes dont la vascularisation est assure
´e
par un double jeu d’anastomoses vasculaires permettant au
jumeau normal de le perfuser a
`contre-courant par une arte
`re
ombilicale. Le jumeau acardiaque n’est plus vascularise
´par le
placenta mais uniquement par son jumeau [1,4]. Cette des-
cription correspond au twin reverse arterial perfusion (TRAP)
syndrome des anglo-saxons, phe
´nome
`ne qui semble e
ˆtre une
forme particulie
`re du syndrome transfuseur-transfuse
´;le
fœtus normal e
´tant le donneur, il de
´livre le sang pour lui-
me
ˆme et pour le fœtus acardiaque conside
´re
´comme le
receveur. Le retour veineux s’effectue par la veine ombilicale
du jumeau normal [1–5]. Dans le syndrome transfuseur-trans-
fuse
´, c’est le receveur qui e
´volue vers l’anasarque.
Les anomalies morphologiques, du po
ˆle ce
´phalique, des mem-
bres et des organes abdominaux, sont lie
´es a
`l’interruption de
l’organogene
`se due aux modifications du de
´bit sanguin chez
le jumeau acardiaque. L’inversion du flux sanguin, seule,
expliquerait le mieux la morphogene
`se incomple
`te voire la
re
´gression de certaines structures existantes, notamment de
l’appareil circulatoire fœtal. En effet, le fœtus acardiaque est
perfuse
´a
`contre-courant par du sang de
´sature
´en oxyge
`ne a
`
partir d’une arte
`re ombilicale souvent unique (50 % des cas).
Ce sang, de
´soxyge
´ne
´, arrivant du donneur a
`faible pression, au
lieu de retourner normalement au placenta, va directement
dans le jumeau acardiaque [1,2,4,6]. L’e
´tude fœtopatholo-
gique de Van Allen et al. [7],a
`partir d’une se
´rie de 14 fœtus
acardiaques, a montre
´que la morphogene
`se e
´tait corre
´le
´eau
de
´veloppement de l’appareil circulatoire. L’œde
`me sous-
cutane
´,e
´quivalent a
`une anasarque, est tre
`s fre
´quent, lie
´
aussi aux troubles circulatoires [1,4]. Une anomalie du caryo-
type est pre
´sente dans 50 % des cas [3]. Dans notre observa-
tion, l’e
´tude du caryotype n’a pu e
ˆtre re
´alise
´e.
Le diagnostic pre
´natal est possible de
`sle1
er
trimestre de la
grossesse [5,6,8]. L’analyse par doppler pulse
´permet de
l’affirmer en montrant une inversion du flux sanguin au
niveau des vaisseaux ombilicaux [7,8]. Une discordance bio-
me
´trique des 2 jumeaux, un œde
`me sous-cutane
´diffus ou
des anomalies morphologiques sur l’un des 2 jumeaux per-
mettent d’e
´voquer le diagnostic de fœtus acardiaque.
La discordance biome
´trique est un signe e
´chographique
constant et pre
´coce. Elle est visible de
`s9SA[8]. L’œde
`me
sous-cutane
´y est tre
`s fre
´quemment associe
´. Certains fœtus
acardiaques peuvent conserver une e
´bauche cardiaque ou
cœur rudimentaire qui explique la persistance d’une activite
´
cardiaque a
`des termes plus tardifs [7,8]. Le diagnostic diffe
´-
rentiel se fait avec la mort du second jumeau au cours des
premie
`res semaines de grossesse. Les e
´chographies ulte
´rieures
portent le diagnostic, dans ce cas, en montrant la poursuite de
la croissance du fœtus acardiaque [4,8].
Les anomalies devant faire e
´voquer le diagnostic sont : une
absence de boıˆte cra
ˆnienne, une holoprosence
´phalie, une
anence
´phalie, une absence de massif facial, une anophtalmie,
une fente palatine, des membres absents ou rudimentaires,
une atre
´sie diaphragmatique, une absence de thorax et de
cœur, une atre
´sie de l’œsophage, une absence de foie et de
ve
´sicule biliaire, un œde
`me cutane
´et une arte
`re ombilicale
unique. Il faut e
´galement rechercher chez le jumeau trans-
fuseur des signes de de
´faillance cardiaque a
`type d’ascite,
d’e
´panchement pleural, d’hydramnios ou d’œde
`me cutane
´
[1,8].
L’examen par doppler peut montrer un flux avec une re
´sis-
tance anormalement haute au niveau de l’arte
`re ombilicale
du jumeau acardiaque. Cet examen interpre
´te
´seul n’a pas de
valeur pre
´dictive de l’e
´volution du fœtus donneur. La diffe
´-
rence des indices de re
´sistance entre les jumeaux semble e
ˆtre
le mieux corre
´le
´e avec l’issue de la grossesse. Une grande
diffe
´rence de re
´sistance, supe
´rieure a
`0,20 entre le jumeau
donneur et l’acardiaque, est associe
´ea
`de bons re
´sultats, alors
qu’une diffe
´rence infe
´rieure a
`0,05 est associe
´ea
`l’apparition
de complications [1,7,8].
Le pronostic du jumeau acardiaque est fatal. La mortalite
´du
jumeau donneur est de l’ordre de 50 a
`75 %, le plus souvent par
de
´faillance cardiaque [7,9]. Dans notre observation, le jumeau
« donneur » n’ayant pas pre
´sente
´de de
´faillance cardiaque, le
pronostic e
´tait bon.
Nous avons opte
´initialement pour un amniodrainage afin de
re
´duire les contractions ute
´rines lie
´es a
`l’exce
`s de liquide
amniotique. Nous pensons que cette attitude attentiste e
´tait
justifie
´e devant l’absence de signes d’insuffisance cardiaque
chez le fœtus donneur. Moore et al. [10] ont montre
´que
la survenue d’un hydramnios, celle d’un accouchement
Jumeau acardiaque ace
´phale
Figure 4. Jumeau acardiaque : absence de structure ce
´phalique.
255

pre
´mature
´et les re
´sultats pe
´rinatals e
´taient fortement lie
´sau
rapport du poids du fœtus acardiaque sur le poids du donneur.
Ainsi, quand le jumeau acardiaque pe
`se moins de 25 % du
poids du donneur, l’e
´volution est ge
´ne
´ralement favorable. En
revanche, si le rapport est de plus de 70 %, l’incidence de
l’accouchement pre
´mature
´est de 90 %, celle de l’hydramnios
de 40 % et celle de la de
´faillance cardiaque du donneur de
30 % contre respectivement 75, 30 et 10 % lorsque le rapport
est infe
´rieur. En effet, l’augmentation de la perfusion ne
´ces-
saire a
`un « gros » acardiaque par rapport au jumeau normal
de
´termine le pronostic. Cependant, l’estimation du poids du
jumeau acardiaque est tre
`s difficile a
`cause de ses malforma-
tions et les mesures utilise
´es ont le plus souvent e
´te
´re
´alise
´es
re
´trospectivement en pe
´riode postnatale. Dans notre cas, bien
que ce rapport fuˆt de 80,5 %, il n’y a pas eu de de
´faillance
cardiaque du jumeau vivant mais un hydramnios.
Certains facteurs pronostiques e
´chographiques ont e
´te
´iden-
tifie
´s. Les variables e
´tudie
´es chez le fœtus sain sont le rapport
cardiothoracique et la fraction d’e
´jection du ventricule gau-
che. Chez le fœtus acardiaque, ce sont la longueur maximale,
la longueur et la taille des kystes secondaires a
`l’œde
`me, la
pre
´sence d’un cœur rudimentaire et, chez les 2 fœtus, l’index
de pulsatilite
´de l’arte
`re ombilicale. Ainsi, un index de pulsa-
tilite
´de l’arte
`re ombilicale du jumeau acardiaque augmente
´
par rapport a
`celui du jumeau normal, une augmentation de la
fraction d’e
´jection au 2
e
trimestre et une croissance rapide de
la masse sont associe
´sa
`un mauvais pronostic. Le rapport
cardiothoracique et la pre
´sence de kystes n’ont pas de valeur
pronostique [7,9]. Ainsi, ces grossesses ne
´cessitent une sur-
veillance e
´chographique re
´gulie
`re afin de rechercher des
signes de de
´faillance cardiaque du donneur.
Les traitements interventionnistes ont pour but d’interrompre
les communications vasculaires entre les 2 jumeaux [9,10].
Seeds et al. [11] ont propose
´un fœticide se
´lectif, mais l’injec-
tion d’une substance le
´tale pourrait aussi toucher le jumeau
sain. Une coagulation endoscopique par laser des vaisseaux
du cordon ombilical du jumeau acardiaque sous contro
ˆle
e
´chographique est une alternative permettant un arre
ˆt
complet de la perfusion arte
´rielle inverse et la disparition
de la re
´gurgitation tricuspidienne du jumeau normal en
2 semaines sans aucune complication par la suite [12,13].
Une re
´duction se
´lective du jumeau acardiaque par radiofre
´-
quence au niveau de l’insertion du cordon chez le jumeau
acardiaque peut e
ˆtre re
´alise
´e. Une aiguille est inse
´re
´e par voie
percutane
´e jusqu’a
`l’origine du cordon et l’e
´nergie est
envoye
´e jusqu’a
`ce que le flux sanguin soit stoppe
´chez
l’acardiaque [14]. Lewi et al. [3] ont montre
´re
´cemment sur
80 grossesses ayant be
´ne
´ficie
´l’efficacite
´d’un traitement par
coagulation a
`la pince du cordon ombilical du jumeau acar-
diaque. Pour Wong et Sepulveda [15], quand le jumeau acar-
diaque est petit, une simple surveillance e
´chographique est
recommande
´e, avec recherche de complications chez le
jumeau sain. En revanche, il faut envisager un traitement
invasif, par coagulation ou interruption par radiofre
´quence de
l’aorte abdominale ou des vaisseaux pelviens de l’acardiaque,
quand ce dernier est gros ou s’il grandit de fac¸on rapide.
4. Conclusion
Le jumeau acardiaque est une forme particulie
`re et rarissime
du syndrome transfuseur-transfuse
´compliquant une gros-
sesse ge
´mellaire monozygotique. Son diagnostic en pe
´riode
ante
´natale se fait gra
ˆce a
`l’e
´chographie-Doppler. Sa de
´cou-
verte implique une surveillance rapproche
´e de la grossesse
afin de de
´pister une insuffisance cardiaque chez le jumeau
donneur dont la mortalite
´reste importante. Les traitements
propose
´s visent a
`interrompre les communications vasculaires
entre les 2 jumeaux afin de re
´aliser un fœticide se
´lectif. En
pratique, la conduite a
`tenir obste
´tricale navigue entre l’abs-
tentionnisme et l’interventionnisme, attitude lie
´ea
`la pre
´-
maturite
´et l’insuffisance cardiaque dont de
´pend le pronostic
du jumeau sain.
Conflit d’inte
´re
ˆt
Aucun.
Re
´fe
´rences
[1] Guigue V, Schwetterle F, Arbez-Gindre F. Un cas de jumeau
acardiaque ace
´phale et revue de la litte
´rature. J Gynecol Obstet
Biol Reprod (Paris) 2007;36:293–7.
[2] Fatnassi R, Mestiri H, Karray T, et al. Le fœtus acardiaque
ace
´phale : diagnostic ante
´natal et modalite
´s the
´rapeutiques.
Imagerie de la Femme 2009;19:51–5.
[3] Lewi L, Gratacos E, Ortibus E, et al. Pregnancy and infant
outcome of 80 consecutive cord coagulations in complicated
monochorionic multiple pregnancies. Am J Obstet Gynecol
2006;194:782–9.
[4] Pouehe
´D, Galtier J-L, Rique M. Fœtus acardiaque ace
´phale et
grossesse ge
´mellaire : a
`propos d’un cas. J Gynecol Obstet Biol
Reprod (Paris) 1999;28:275–7.
[5] Coulam CB, Wright G. First trimester diagnosis of acardiac
twins. Early Pregnancy 2000;4:261–70.
[6] Kayalvizhi I, Dhall U, Magu S. Acardius acephalus monster: A
case report. J Anat Soc India 2005;54:26–8.
[7] Van Allen MI, Smith DW, Shepard TH. Twin reversed arterial
perfusion (TRAP) sequence: A study of 14 twin pregnancies with
acardius. Semin Perinatol 1983;7:285–93.
[8] Baron M, Verspyck E, Diguet A, et al. Se
´miologie e
´chographique
du fœtus acardiaque au premier trimestre de la grossesse. J
Gynecol Obstet Biol Reprod (Paris) 2000;29:684–6.
[9] Brassard M, Fouron JC, Leduc L, et al. Prognostic markers in twin
pregnancies with an acardiac fetus. Obstet Gynecol 1999;94:
409–14.
[10] Moore TR, Gale S, Benirschke K. Perinatal outcome of fortynine
pregnancies complicated by acardiac twinning. Am J Obstet
Gynecol 1990;163:907–12.
[11] Seeds JW, Herbert WN, Richards DS. Prenatal sonographic
diagnosis and management of a twin pregnancy with placenta
previa and hemicardia. Am J Perinatol 1987;4:313–6.
H. Boufettal et al. Archives de Pe
´diatrie 2010;17:253-257
256

[12] Hecher K, Reinhold U, Gbur K, et al. Interruption of umbilical
blood flow in an acardiac twin by endoscopic laser coagulation.
Geburtshilfe Frauenheilkd 1996;56:97–100.
[13] Deprest JA, Audibert F, Van Schoubroeck D, et al. Bipolar
coagulation of the umbilical cord in complicated monochor-
ionic twin pregnancy. Am J Obstet Gynecol 2000;182:340–5.
[14] Tsao K, Feldstein VA, Albanese CT, et al. Selective reduction of
acardiac twin by radiofrequency ablation. Am J Obstet Gynecol
2002;187:635–40.
[15] Wong AE, Sepulveda W. Acardiac anomaly: Current issues in
prenatal assessment and treatment. Prenat Diagn 2005;25:
796–806.
Jumeau acardiaque ace
´phale
257
1
/
5
100%