Physique chimie 3eme Chapitre 2 La constitution de la matière

Physique chimie 3eme
Chapitre 2
La constitution de la matière
Plan du cours:
Introduction: activité documentaire « Histoire du modèle de l’atome »
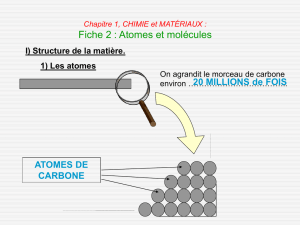
1. Observation au microscope a champ proche
2. La dimension des atomes
3. Constitution de l’atome
4. Le symbole des atomes
5. L’assemblage de la matière
6- Les ions
7. Liens entre la structure microscopique des matériaux et leurs
propriétés
Exercices: livre BELIN page 22 - 23
16-mai-05 Physique Chimie 3eme
Chapitre 2
La constitution de la matière 1

16-mai-05 Physique Chimie 3eme
Chapitre 2
La constitution de la matière 2

Dalton, Thomson, Rutherford.
Électrons (en 1881).
Oui (charge négative)..
Pudding de Thomson (l’atome est une sphère contenant des
charges positives et négatives parsemées ).
Que la charge positive de l’atome occupe un tout petit volume (qu’il
appelle le « noyau »).
Que la majorité de la masse de l’atome est concentrée dans le noyau.
L’atome est 100000 fois plus grand que le noyau.
Dans un atome, il y a autant de particules positives (proton) que d’électrons..
L’atome est électriquement neutre.
La masse de la matière est essentiellement concentrée dans le noyau et ce
noyau est 100000 fois plus petit que l’atome. Donc le reste est vide: la
matière est lacunaire.
16-mai-05 Physique Chimie 3eme
Chapitre 2
La constitution de la matière 3

Modèle planétaire.
Le modèle d’un noyau autour duquel gravitent des électrons formant un nuage
électronique
Le modèle de Rutherford ne permet pas d’expliquer tout les phénomènes.
(par exemple la fluorescence s’explique avec un modèle quantique de
l’atome)
Oui
On tente d’expliquer des phénomène grâce a un modèle. L’expérimentation permet
De le confirmer ou de le rejeter.
évolué
le modèle
limites.
16-mai-05 Physique Chimie 3eme
Chapitre 2
La constitution de la matière 4

16-mai-05 Physique Chimie 3eme
Chapitre 2
La constitution de la matière 5
Histoire du modèle de l’atome
Démocrite (-420) a l’intuition que la matière est formée d’atomes. Au I
er
siècle av-JC Lucrèce tente de démontre
r
l’existence de l’atome. Atome vient de tomos qui signifie couper et le préfixe a signifie
q
u’on ne
p
eut cou
p
er, insécable.
L’atome est décrit comme la particule la plus petite possible.
C’est la théorie des quatre éléments d’Aristote qui va s’imposer jusqu’au XIX
e
siècle. La combinaison de la terre, de
l’eau, de l’air et du feu explique la composition de la matière.
En 1805, John Dalton reprend la théorie atomique car elle rend bien com
p
te de ses observations. En 1881, J.J.
Thomson découvre les électrons. En 1904 il décrit l’atome comme des ensembles de charges
p
ositives occu
p
ant une
petit volume au milieu d’électrons. L’atome n’est plus insécable ! C’est le modèle du pudding de Thomson. Cha
q
ue
charge positive est égale à chaque charge négative, au signe près :
Charges positives
Electrons
En 1910, Rutherford montre
q
ue la matière contient essentiellement du vide et
q
ue le noyau
q
ui est 100 000 fois
p
lus
petit que l’atome représente presque toute sa masse.
Rutherford décrit un atome dont le modèle est cal
q
ué sur celui des
p
lanètes. La masse du soleil re
p
résente 99 % de l
a
masse du système solaire et son diamètre est très petit par rapport à celui du système solaire. Le noyau est au centre e
t
les électrons tournent autour sur des trajectoires fixes :
Electrons
Noyau qui contient
presque toute la masse
de l'atome
Ce modèle ne
p
ermet
p
as d’ex
p
li
q
uer de nouvelles observations. On doit admettre
q
ue la trajectoire des électrons es
t
plus compliquée.
Nuage électronique
Noyau central
Trajectoire d'un électron Modèle de l'atome contenant toutes
les tra
j
ectoires de tous les électrons
Le modèle actuel est très com
p
lexe et ne
p
eut
p
lus être re
p
résenté
p
ar un dessin. Néanmoins,
p
our ex
p
li
q
uer l
a
p
hysi
q
ue et la chimie élémentaire il est suffisant d’admettre un modèle de l’atome avec un noyau central
p
ositif très
petit et des électrons
q
ui tournent autour en formant un nuage s
p
héri
q
ue. On élabore un modèle conformément au
x
p
hénomènes observés, il doit
p
ermettre de
p
révoir d’autres
p
hénomènes. On modifie le modèle au fur et à mesure des
observations.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%