Introduction

Introduction
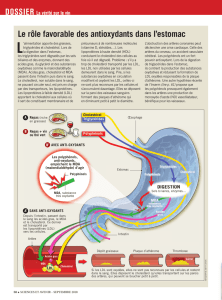
L'excès de cholestérol dans l'alimentation peut induire une pathologie appelée
athérosclérose.
La physiopathologie de cette maladie est la suivante: le cholestérol en excédent se
dépose dans la paroi artérielle. Le diamètre de l'artère diminue. Il y a aussi une
calcification qui réduit l'élasticité des artères et enfin le collagène sous endothélial est mis
à nu ce qui provoque des thromboses. Ce phénomène est particulièrement dangereux si
l'artère irrigue un organe vital (cœur, cerveau).
Le flux du cholestérol dans l'organisme est assuré par des lipoprotéines qui transportent
le cholestérol de l'intestin vers le foie ou les artères ou bien des artères vers le foie.
Pour évaluer le risque athérogène (risque de thrombose), on dose les différentes
lipoprotéines et on compare leurs quantités. Si les lipoprotéines qui transportent le
cholestérol vers les artères sont nombreuses, le risque est élevé. Ce risque est atténué
par la présence de lipoprotéines qui assurent le retour du cholestérol vers le foie.
Les lipoprotéines
a) Structure
Les acides gras et les lipides jouent un rôle fondamental dans le fonctionnement
des êtres vivants : ils sont les composants principaux des membranes cellulaires,
jouent un rôle dans la transmission nerveuse et certains lipides sont utilisés comme
précurseurs d'hormones.
Une grande partie de ces lipides est apportée par l'alimentation. Ils sont
distribués par voie sanguine et lymphatique à tous les organes du corps humain.
Un lipide est un ester (combinaison
d'un acide gras et d'un alcool). Il
possède donc dans sa formule
chimique de longues chaînes
carbonées peu ou pas polarisées. Cette
structure explique l'effet hydrophobe
des lipides : ceux-ci sont insolubles
dans l'eau . Or, le sang est le tissu qui
contient la plus grande proportion
d'eau de tout le corps humain.
Comment un milieu aqueux
pourrait-il transporter des
molécules hydrophobes (insolubles
dans l'eau ) ?
La solution réside dans la présence dans le sang de complexes macromoléculaires
appelés lipoprotéines. Ces lipoprotéines sont constituées d'une association lipide-
protéine. Ces protéines sont constituées d'acides aminés (AA) dont le résidu peut être
très hydrophile. Dans le cas de certains AA le résidu peut même être ionisé (aspartate,
asparagine, glutamate, glutamine, lysine, arginine). Ces AA présentent une grande
affinité pour l'eau qui est une molécule polaire. Les lipides, en association avec ces

protéines (appelées apolipoprotéines ou plus simplement, apoprotéines) peuvent ainsi
être aisément transportées dans le sang.
La disposition spatiale des divers composants des lipoprotéines est déterminée par la
polarité de ces composants : plus une molécule est polaire, plus elle sera située à la
périphérie de la lipoprotéine c'est à dire en contact avec l'eau. Par contre, les molécules
hydrophobes se retrouvent au centre.
Les lipides des lipoprotéines:
Dans une lipoprotéine, on trouve:
des phospholipides
Ce sont des esters d'acide phosphorique et de diglycérides.
Ils se situent à la périphérie de la lipoprotéine. Leur partie
hydrophile est tournée vers l'extérieur. Les phospholipides sont
d'importants éléments structuraux de la membrane cellulaire. Ils
n'interviennent pas directement dans les manifestations cliniques
des dyslipoprotéinémies.
des triglycérides
Formule générale :
Leur caractère franchement apolaire les relègue au centre des lipoprotéines.
Les triglycérides semblent n'être pas directement un facteur de risque
cardio-vasculaire. Toutefois, une hypertriglycéridémie pourrait constituer un
fait aggravant d'autres facteurs de risque reconnus (alcool , tabac,
diabète...).
Le cholestérol non estérifié (CL)
A cause de sa fonction alcool faiblement hydrophile, le cholestérol libre se situe à la
surface de la lipoprotéine. Dans le règne animal, le cholestérol est le stérol le plus
abondant et aussi le plus important au plan métabolique en tant que précurseur des
hormones stéroïdes (progestérone, aldostérone, cortisol et cortisone, testostérone,
oestradiol et oestrone). L'hypercholestérolémie est la cause de la genèse de l'athérome
artériel.
Le cholestérol estérifié (CE)
La fonction OH est liée à un acide gras supprimant ainsi tout caractère hydrophile. Le CE
se situe donc au centre de la lipoprotéine.
Acides gras non estérifiés
o Les apoprotéines :
Comme nous l'avons vu, ces apoprotéines ont un rôle structural important. Elles se
situent à la surface des lipoprotéines grâce à leurs AA hydrophiles. La partie hydrophobe
de ces protéines est tournée vers l'intérieur.

Ces apoprotéines ont une deuxième fonction: certaines jouent le rôle de liguant,
d'autres d'activateurs ou d'inhibiteurs enzymatiques (Voir section c, le métabolisme des
lipoprotéines ).
CARACTÉRISTIQUES
PHYSICO-CHIMIQUES ET FONCTIONS DES APOLIPOPROTÉINES MAJEURES
Apoprotéin
es
Acides
aminé
s
Poids
moléculair
e
Lieu de
synthèse
VLD
L
LDL
HD
L
concentratio
n
plasmatique
(g/l)
Fonction
apo A1
245
23 300
foie,
intestin
4%
67
%
1,00 à 1,20
activateur
LCAT.
Efflux de
cholestérol
apo AII
77x2
17 000
foie,
intestin
22
%
0,4
structure
des HDL
apo AIV
?
45 000
intestin
0,15
efflux de
cholestérol
apo B100
?
540 000
foie
35%
90
%
0,70 à 1,00
sécrétion
des VLDL.
ligand du
récepteur
LDL
apo B48
?
275 000
intestin
0,03 à 0,05
sécrétion
des
chylomicro
ns
apo C1
57
7 000
foie
+
+
0,04 à 0,06
activateur
LCAT in
vitro
apo C2
78
8 900
foie
40%
5-
9%
0,03 à 0,05
activateur
LPL, VLDL,
HDL
apo C3
79
8 700
foie
+
+
0,12 à 0,14
inhibiteur
LPL
apo D
169
33 000
gonades,
rein , foie,
placenta,
intestin
+
+
0,06 à 0,07
métabolism
e des
esters du
cholestérol
apo E
299
38 000
foie,
intestin,
surrénales,
macrophag
es
13%
0,03 à 0,05
ligand du
'récepteur
LDL' et du
récepteur
des
chylomicro
ns résiduels
b) Classification :
Il existe plusieurs sortes de lipoprotéines. On peut classer celles-ci selon :

leur composition chimique (quantité et nature des lipides et des protéines).
leur réactivité chimique vis à vis des polyanions et des lectines (Réaction de
précipitation).
leur réactivité immunologique vis à vis d'immuns sérums spécifiques (sérums
anti-apoprotéines)
leur origine ou devenir métabolique
leur pouvoir pathogène (pathogénie des lipidoses)
leurs propriétés physiques (dimension, mobilité élèctrophorétique , densité )
A l'heure actuelle, le classement est basé sur la densité des lipoprotéines par
ultracentrifugation de flottation.
On distingue les lipoprotéines suivantes :
Lipoprotéines
Densité (g/ml)
chylomicrons
<0,94
VLDL
0,94 à 1,006
LDL1 (IDL)
1,006 à 1,019
LDL2
1,019 à 1,063
HDL1
<1,063
HDL2
1,063 à 1,125
HDL3
1,125 à 1,21
VHDL
1,21 à 1,25
Lp(a)
1,055 à 1,085
Plus la fraction protéique est importante, plus la densité sera élevée.
Toutefois, les lipoprotéines de haute densité (HDL), par exemple, n'ont pas la même
composition lipidique que les lipoprotéines de basse densité. Cependant, ce n'est pas la
densité des lipoprotéines qui nous indique le rôle de chacune. En effet, les lipoprotéines
séparées en fonction de leur densité sont hétérogènes et leurs métabolismes très
différents au sein d'une même catégorie.
Nous avons vu que les apoprotéines jouent un rôle important dans le métabolisme de ces
lipoprotéines.
Il serait donc plus judicieux pour évaluer le risque athérogène de baser la
classification sur la teneur en apoprotéines. Toutefois, il y a quand même une
certaine corrélation entre la fonction et la densité des lipoprotéines.
c) Métabolisme
Le cholestérol a deux origines chez l'homme : une origine exogène (alimentation) et une
origine endogène (biosynthèse).
Cholestérol endogène :
La biosynthèse du cholestérol est, chez les vertébrés, microsomale. Elle est
régulée par un mécanisme de rétroinhibition par un métabolite du cholestérol (le 25
hydroxycholestérol) au niveau de la Bêta-hydroxy-bêta-méthyl-glutaryl-stérol coenzyme
A réductase. Cette rétroinhibition n'est jamais totale pour permettre la synthèse de
polyisoprénoïdes importants pour d'autres métabolismes comme les dolichols. En effet,
un précurseur du cholestérol peut également être métabolisé en dolichol.

Le foie est l'un des principaux sites de synthèse mais toutes les cellules du corps
humain peuvent synthétiser le cholestérol. Cependant, dans les conditions
physiologiques, l'apport exogène du cholestérol hépatique aux divers tissus est suffisant
pour que la synthèse endogène dans ces tissus soit inhibée.
Cholestérol exogène :
Au cours d'un repas, des matières grasses riches en triglycérides sont totalement ou
partiellement hydrolysées sous l'action de la lipase pancréatique en acides gras, glycérol,
mono et diglycérides. Le glycérol et les acides gras libres à courte chaîne (jusqu'à 10
atomes de carbone) vont aller vers le foie par la voie sanguine (en particulier par la veine
porte). Tous les autres acides gras à longue chaîne ainsi que les mono et diglycérides
servent à la reconstitution de triglycérides au niveau de la muqueuse intestinale.
Le cholestérol alimentaire subit une première transformation dans les cellules de
l'intestin, les entérocytes, où il est estérifié par l'acyl-coenzyme A transférase (ACAT).
Dans les entérocytes, le cholestérol estérifié est associé à des triglycérides, à des
phospholipides et à diverses apoprotéines dont l'APO B48 pour former de grosses
lipoprotéines désignées sous le nom de chylomicrons. L'APO B48 est appelée ainsi car sa
masse moléculaire est 48% celle de l ' APO B100.
Les APO C sont cédées par les HDL aux chylomicrons. Les APO C existent sous trois
formes: Cl, C2, C3. Ces APO C ont peu de rôle structural et leur activité est surtout
métabolique :
1. La forme C1 active la lecithine-cholestérol acyltransferase.
2. La forme C2 est activatrice de la lipoprotéine lipase.
3. La forme C3 inhibe cette même lipoprotéine lipase.
Ce sont principalement des APO C2 que les chylomicrons acquièrent .
L'APO E est un ligand pour le récepteur hépatique à APO E.
Les chylomicrons gagnent rapidement la circulation lymphatique puis la circulation
générale par l'intermédiaire du canal thoracique. Là, ils subissent l'action de la
lipoprotéine lipase (LPL) attachée à l'endothélium vasculaire des muscles et du tissu
adipeux. Cette action est rendue possible, rappelons-le, par l'APO C3. L'action de la LPL
confère aux chylomicrons une demie-vie très brève (30 minutes) ce qui fait qu'on ne les
trouve dans le sang qu'après un repas. Cette enzyme hydrolyse les triglycérides des
chylomicrons en mono et diglycérides ainsi qu'en acides gras qui sont utilisés pour la
production immédiate d'énergie ou mis en réserve.
Parallèlement, sous l'action d'une protéine de transfert spécifique (CETP), le cholestérol
estérifié est transporté vers les particules résiduelles formées lors du métabolisme des
chylomicrons, appelés chylomicrons remnants. Il s'agit là d'un échange puisque les
triglycérides qui restent dans les chylomicrons sont, en même temps, transférés aux
lipoprotéines de haute densité.
Il y a également un échange d'apoprotéines : nous avons vu que les HDL cédaient
des APO C et E aux chylomicrons. Ces chylomicrons libèrent des phospholipides et des
APO A qui sont récupérés par les HDL.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%