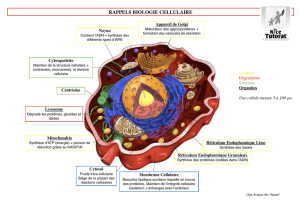
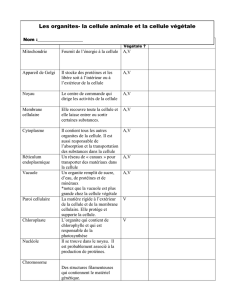
II - Les signaux impliqués dans la coopération cellulaire

M.Gaudin / Préparation au Capet / Immunologie
Coopération cellulaire – Fichier Coop_cellu_capet.doc
Version du 05/04/09
1
La coopération cellulaire
(dans le système immunitaire)
Questions préalables : "dans le SI" non explicité mais demandé par la prépa ; est-ce
qu'on inclut les effets généraux de la RI ? Est-ce qu'on inclut les coopérations avec
des cellules non immunes ? On profitera de ce cours pour élargir un peu le cadre
strict du sujet et compléter les apprentissages d'immunologie.
On parle parfois de "sixième sens circulant" pour le SI, qui participe assurément
à l'homéostasie (homéostasie du point de vue antigénique). Le SI repose sur des
cellules aux activités spécialisées voire très spécialisées, qui dépendent les unes des
autres. Le SI ne peut être efficace que si les cellules qui y concourent interagissent
les unes entre les autres. Au-delà, un grand nombre de cellules non immunitaires
participent aussi, directement ou indirectement, à cette fonction immunitaire.
Cette gigantesque coordination implique donc toute une série de coopérations
cellulaires, le plus souvent à faible distance, éventuellement à plus grande distance.
I - Coordination des phénomènes immunitaires :
A - Les trois temps de la réponse immune :
1) Premier temps - La réponse innée :
Deux intervenants principaux :
- les phagocytes – PRR/PAMP pattern recognition receptor ; pathogen
associated molecular pattern : par exemple le récepteur du mannose des
macrophages, les récepteurs "scavengers" (= éboueurs) qui fixent des
débris lipidiques, les Toll-like Receptors (TLR), une grande famille
moléculaire, qui reconnaissent chacun un motif donné (TLR4 à LPS
bactériens ; TLR3 à ARN double brin des virus, etc.), la protéine sérique de
liaison au lipopolysaccharide (LBP), protéine capable de reconnaître et de
se fixer sur un grand nombre de structures lipopolysaccharidiques de
bactéries, se fixe par ailleurs sur le CD14 des neutrophiles et peut
déclencher la phagocytose.
- le complément par la voie dite alterne – autoactivation du C3 en surface
de cellules.
Production de signaux (cytokines : IL-1, NO ; C3a et C5a) déclenchant d'autres
phénomènes, Cf. 2)
2) Deuxième temps – Les réponses induites non spécifiques :
En réponse aux signaux émis notamment dans la phase décrite ci-dessus, des
mécanismes se mettent en route :
- "un gros morceau" : l'inflammation (sans entrer dans les détails !! Cf. III)
- et aussi NK, interférons, …
L'inflammation permet de drainer un maximum d'antigènes (soit sous forme soluble,
soit sous forme "apprêtée" (CMH) vers les OLII et donc de stimuler ainsi l'immunité
spécifique.

M.Gaudin / Préparation au Capet / Immunologie
Coopération cellulaire – Fichier Coop_cellu_capet.doc
Version du 05/04/09
2
3) Troisième temps – Les réponses spécifiques :
En réalité presque toutes les réponses sont plus ou moins spécifiques ; par
immunité spécifique on entend donc une immunité capable de s'adapter très
précisément aux motifs antigéniques correspondants ("immunité adaptative").
Deux voies principales :
- la médiation cellulaire, impliquant les Ig produites par les LB
- la médiation humorale impliquant
o T8 cytotoxiques reconnaissant l'Ag par leur TCR
o Th1 inflammatoires
o NK, sous dépendance des autres intervenants.
B - Les nécessaires contrôles de la réponse immune :
1) La tolérance au Soi :
Anticorps (BCR) et TCR produits par des mécanismes aléatoires de
recombinaison génétiques entre segments complémentaires (Cf. CDJ dans H, VJ
dans L ; TCR analogue à Fab avec chaîne α=L et β=H). Ces remaniements ont lieu
dans les OLI.
Or en périphérie rarement reconnaissance des peptides du Soi, pourtant issus
de systèmes génétiques indépendants. Donc dans OLI il existe un système de "tri" et
d'élimination des cellules auto-réactives : "éducation du SI" ou "induction de la
tolérance au Soi". Ces systèmes sont au service d'une protection générale de
l'organisme.
2) La coordination d'activités cellulaires spécialisées :
En réalité il n'y a pas trois temps de la RI, mais un ensemble coordonné
d'évènements. Chaque temps est en lien avec les deux autres. Le macrophage est
par exemple au cœur de chacune de ces étapes, qui en réalité se superposent plus
qu'elles ne se succèdent.
Et Coordo RIS : CPA/T/B etc.!
II - Les signaux impliqués dans la coopération cellulaire immunitaire :
A - Les grands types de communication intercellulaire :
1) En terme de mode de transfert de l'information : pas de dia
On distingue la communication :
- par contact direct : par signaux membranaires (il vaut mieux éviter le terme
"paracrine" car il n'y a pas de sécrétion) ;
- par médiateur soluble : donc avec sécrétion d'un messager.
Dans tous les cas, la communication nécessite une cellule émettant le signal mais
aussi une cellule le recevant ; cette dernière doit disposer du récepteur adéquat (on
dit parfois qu'elle est compétente).
2) En terme de distance d'action du médiateur soluble :
On distingue :
- l'action autocrine, d'une cellule sur elle-même : exemple de l'IL2

M.Gaudin / Préparation au Capet / Immunologie
Coopération cellulaire – Fichier Coop_cellu_capet.doc
Version du 05/04/09
3
- l'action paracrine, d'une cellule sur une autre cellule, à faible distance, par
simple diffusion sans reprise par la circulation sanguine (donc par un
médiateur soluble, au sein d'un unique tissu) : le cas de la plupart des
exemples comme IL8 (chimioattractant des phagocytes)
- l'action endocrine, d'une cellule sur une autre cellule (plutôt de groupe
cellulaire à groupe cellulaire), à plus longue distance, avec reprise par la
circulation sanguine (donc par un médiateur soluble, avec des effets
généraux / systémiques) : exemple des cytokines inflammatoires que sont
IL1, IL6 et TNFα.
On parle parfois enfin d'action juxtacrine pour désigner des messages solubles émis
entre cellules au contact direct l'une de l'autre.
3) En terme d'effet :
Un même message peut avoir des effets très variables :
- effet activateur
- effet inhibiteur
- effet modulateur
Des messages différents peuvent interagir entre eux :
- effet agoniste
o synergie
o redondance
- effet antagoniste
Enfin un médiateur peut avoir un effet très spécialisé ou au contraire pléiotrope.
B - Médiateurs solubles :
1) Cytokines :
Définition :
- Première découverte : le "pyrogène endogène" (future IL1) en 1948. Terme
cytokine introduit en 1947 par Stanley COHEN.
- Les cytokines sont une famille de molécules peptidiques de poids
moléculaire modéré (8 à 50 kg.mol-1).
- Vaste famille assez diverse de protéines dont le point commun est
essentiellement d'être produites par des lymphocytes. La plupart ont une
action exclusivement locale, mais quelques unes ont malgré tout un effet
systémique sous certaines conditions.
- En général produites après activation et sécrétées immédiatement (?) –
demie-vie courte car peptides dégradables par protéases extracellulaires.
Nomenclature :
- n'a pas cessé d'évoluer ! bcp de vieilleries traînent encore.
o Monokines et lymphokines sont à éviter car en réalité la plupart
sont produites par des types cellulaires différents.
o Interleukine : de leuco à leuco ; en réalité pas toujours vrai mais le
terme est désormais conservé. Symbole " Il " + n°
o Chimiokines (chemokine en anglais) : petites prot basiques de 70 à
125 AA, à effet chimioattractant… mais certaines IL aussi ! Et les
chimiokines ont parfois des effets activateurs… Terme ambigu ?

M.Gaudin / Préparation au Capet / Immunologie
Coopération cellulaire – Fichier Coop_cellu_capet.doc
Version du 05/04/09
4
Classification proposée en CCL (Cys-Cys Ligand) et CXCL (Cys X
Cys Ligand) selon la structure
o en réalité donc : pas toujours très rigoureux.
- Nombreux types cellulaires donc aucun consensus.
2) Autres types de messagers solubles :
On retrouve des médiateurs plus généraux impliqués aussi dans la modulation
de la RI :
- dérivés de l'acide arachidonique : prostaglandines, leucotriènes – souvent
sécrétés par des cellules non immunitaires (sécrétion plaquettaire par
exemple),
- des amines vasoactives : histamine produite par les mastocytes
- des peptides neuronaux : substance P, neuropeptide, cholécystokinine,
pour lesquels il existe des récepteurs sur les lymphocytes.
- les corticoïdes : cortisol
Jusqu'où pousser cette notion de signal ? exemple du cas particulier des anticorps
qui peuvent être reconnus par des cellules de l'immunité dont ils modulent l'activité…
3) Récepteurs aux cytokines :
On l'a vu, pas de cytokine sans récepteur ! Logiquement, puisque les cytokines
sont de nature assez diverse (bien que toutes peptidiques ! mais pas de motif
structural commun), il n'existe pas de récepteur "typique".
- en général :
o affinité très forte (Kd = 10-10 à 10-12 mol.L-1) nécessaire car
concentration très faible (nmol.L-1 à pmol.L-1 !!)
o transmembranaire (extra/mb/intra)
o multimérique (plusieurs ss-U) – souvent trimériques
- un exemple : R-IL2
o dimère d'affinité moyenne
IL2-Rβ, dédié à la transduction du signal
IL2-Rγ, commun à d'autres cytokines (4, 7, 9, 15, 21)
o + IL2-Rα trimère de haute affinité
o les déficits chaine γ se traduisent d'absence totale de réponse
immune spécifique et une réponse non spécifique gravement
atténuée : phénotype SCID (syndrome sévère combiné
d'immunodéficience, "enfants bulles") ; premier essai durablement
efficace de thérapie génique (Alain Fischer, 99) mais leucémies
induites par le vecteur rétroviral…
4) Voies de transduction :
Là encore, pas de récepteur typique donc pas de transduction typique. Quatre
voies de transduction au moins :
- NFκB
- MAP-kinases
- JAK-STAT
- Protéines G

M.Gaudin / Préparation au Capet / Immunologie
Coopération cellulaire – Fichier Coop_cellu_capet.doc
Version du 05/04/09
5
5) Action coordonnée des médiateurs chimiques :
Anomalies IL2 ou IL2-R : génération de pathoprofils très variés, allant de
l'immunodéficience légère au SCID ; ceci suggère qu'il existe d'autres voies
parallèles ou complémentaires à l'activation par l'IL-2, et/ou effet-dose.
D'une manière générale, les messages chimiques délivrés et reçus sont
multiples, les modulateurs possibles du relais intracellulaire nombreux (facteurs de
transcription…) : avec un nombre limité de messages, on peut exercer une
communication fine et variée.
C - Signaux de contact :
1) Les molécules d'adhésion intercellulaire :
Qui dit délivrance de signal par contact dit support du contact, et maintien de
celui-ci le temps nécessaire à la transduction du signal. Les protéines d'adhésion
intercellulaires jouent un rôle fondamental, autorisant ou non des interactions entre
cellules (si pas d'adhésion pas d'échange !). Ces protéines jouent aussi un rôle
fondamental dans la (re)localisation des cellules immunitaires.
Ces molécules font partie des ICAM (molécules d'adhésion intercellulaires) ; on
y retrouve intégrines (reconnaissant des séquences peptidiques, notamment des
fibres de la MEC : fibronectine…), sélectines (reconnaissant des séquences
polyosidiques), des protéines de la superfamille des immunoglobulines (nb : rien
à voir avec l'anticorps !)…
Exemple : extravasation par diapédèse GN dans la réponse inflammatoire :
- les GN interagissent faiblement par leur radical Sialyl-Lewis avec la E-
sélectine exprimée par les cellules endothéliales des capillaires ; cette
interaction permet au GN de ralentir et de sortir du flux central, rapide ; en
quelque sorte les GN roulent à la surface de la paroi vasculaire ;
- lorsque le territoire sous-jacent est inflammé, les cellules endothéliales
expriment des ICAM supplémentaires (ICAM-1) qui reconnues par des
protéines du GN (LFA-1 = antigène de fonction leucocytaire n°1, formé par
l'assemblage de CD11:a et CD18) permettent une forte interaction du GN à
la paroi vasculaire ; celui-ci est "stoppé" de manière prolongée ;
- des protéines exprimées par les cellules endothéliales (CD31) permettent au
lymphocyte de se glisser entre celles-ci (diapédèse) et de sortir de la
lumière vasculaire (extravasation).
La coopération cellulaire dans la RI met donc en jeu des cellules immunitaires mais
aussi beaucoup d'autres cellules, dont les cellules endothéliales ou les cellules de la
matrice extracellulaire qui concourent à offrir un support aux cellules immunitaires.
2) Molécules de signalisation :
Les échanges intercellulaires nécessitent une communication souvent riche et
complexe ; on distingue conceptuellement :
- des signaux principaux (impliquant le plus l'antigène lors des étapes de
réponse spécifique) : exemple TCH-Ag-CMH
- des signaux complémentaires : cosignaux, aux effets variés.
Ce qui implique des transductions multiples et complexes dans la cellule.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%