L`ischémie critique chronique - Service Central d`Authentification

- 1
1
UNIVERSITE DE NANTES
FACULTE DE MEDECINE
Année 2006 N° 51
THESE
pour le
DIPLOME D’ETAT DE DOCTEUR EN MEDECINE
Médecine Générale
Par
Laure Anne CAPITAINE
Née le 6 avril 1976 à Saint-Nazaire
Thèse présidée par Monsieur le Professeur PLANCHON
et dirigée par Monsieur le Docteur PISTORIUS
Présentée et soutenue publiquement le mercredi 13 décembre 2006
VALEUR PRONOSTIQUE D’UN GRADIENT DISTAL
D’OXYMETRIE TRANSCUTANEE DANS LA PRISE EN
CHARGE DES PATIENTS EN ISCHEMIE CRITIQUE NON
REVASCULARISABLE.
Jury :
Monsieur le Professeur PLANCHON Bernard / Monsieur le Professeur PATRA Philippe
Monsieur le Professeur HAMIDOU Mohamed / Monsieur le Professeur SENAND Rémy
Monsieur le Docteur PISTORIUS Marc-Antoine / Monsieur le Docteur EVENO Dominique
Monsieur LE LAMER Serge
1

- 2
2
TABLE DES MATIÈRES
I. INTRODUCTION...................................................................................................................4
II. RAPPELS : ARTERIOPATHIE CHRONIQUE OBLITERANTE DES MEMBRES
INFERIEURS (ACOMI) ............................................................................................................6
II.1 Introduction.....................................................................................................................6
II.1.1 Définition..................................................................................................................6
II.1.2 Etiologies..................................................................................................................6
II.1.3 Athérosclérose.........................................................................................................6
II.1.4 Cas particulier du diabète ........................................................................................7
II.1.5 Classification de l’artériopathie oblitérante de membres inférieurs..........................8
II.2 Patient asymptomatique...............................................................................................10
II.2.1 Epidémiologie, signification....................................................................................10
II.2.2 Dépistage de l’ACOMI............................................................................................11
II.2.3 Bilan d’extension vasculaire...................................................................................11
II.2.4 Prise en charge des facteurs de risque cardio-vasculaire .....................................11
II.3 Claudication intermittente des membres inférieurs.......................................................13
II.3.1 Définition- signification...........................................................................................13
II.3.2 Epidémiologie- pronostic........................................................................................14
II.3.3 Examen physique...................................................................................................14
II.3.4 Explorations non invasives.....................................................................................14
II.3.5 Explorations invasives............................................................................................17
II.3.6 Prise en charge thérapeutique...............................................................................18
II.4 Ischémie critique chronique des membres inférieurs (ICMI) ........................................21
II.4.1 Définition................................................................................................................21
II.4.2 Incidence et prévalence.........................................................................................21
II.4.3 Pronostic................................................................................................................22
II.4.4 Physiopathologie....................................................................................................23
II.4.5 Diagnostic ..............................................................................................................25
II.4.6 Traitement..............................................................................................................30
III. MATERIEL ET METHODE................................................................................................53
III.1 Méthode.......................................................................................................................54
III.1.1 Critères d’inclusion................................................................................................54
III.1.2 Critères d’exclusion...............................................................................................54
III.1.3 Fin du suivi du patient pour l’étude .......................................................................55
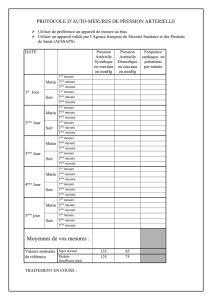
III.1.4 Protocole d’évaluation (annexe 1).........................................................................55
III.2 Matériel........................................................................................................................61
IV. ANALYSE DES RESULTATS...........................................................................................62
IV.1 Caractéristiques de la population étudiée...................................................................63
IV.1.1 Caractéristiques démographiques........................................................................63
IV.1.2 Lésions étudiées...................................................................................................63
IV.1.3 Facteurs de risque cardio-vasculaire....................................................................64
IV.1.4 Antécédents cardio-vasculaires............................................................................66
IV.1.5 Traitements...........................................................................................................68
IV.1.6 Biologie.................................................................................................................73
IV.1.7 Pression systolique à la cheville...........................................................................75
IV.1.8 Oxymétrie statique................................................................................................75
IV.1.9 Motifs de non revascularisation............................................................................78
IV.2 Evolution......................................................................................................................79
IV.2.1 Evolution générale................................................................................................79
IV.2.2 Evolution des signes fonctionnels.........................................................................81
IV.2.3 Evolution des plaies..............................................................................................84
2

- 3
3
IV.2.4 Evolution du traitement antalgique .......................................................................84
IV.2.5 Evolution selon l’âge et le sexe ............................................................................87
IV.2.6 Evolution selon la durée d’oxygénation nasale.....................................................89
IV.2.7 Evolution selon les données oxymétriques - TcPO2.............................................90
V. DISCUSSION...................................................................................................................105
V.1 Méthodologie..............................................................................................................106
V.2 Pronostic de l’ICMI.....................................................................................................109
V.3 Intérêt de l’oxymétrie statique distale dans l’ICMI......................................................114
CONCLUSION .....................................................................................................................121
BIBLIOGRAPHIE..................................................................................................................123
Annexes ...............................................................................................................................136
Annexe 1 : formulaire d’inclusion et de suivi.....................................................................136
Annexe 2 : évolution des plaies........................................................................................141
RESUME..............................................................................................................................164
MOTS-CLES ........................................................................................................................164
3

- 4
4
LES PHOTOS SONT VISIBLES SEULEMENT SUR L’EXEMPLAIRE PAPIER DE LA THÈSE
I. INTRODUCTION
Les patients en ischémie critique chronique des membres inférieurs non revascularisable, en
l’absence de neuropathie distale sévère, souffrent de douleurs souvent rebelles aux
morphiniques et leur pronostic vital peut être engagé par l’ulcère et ses conséquences,
notamment infectieuses. Ceci peut s’amender grâce à une amputation : comme dans le cas
de la chirurgie de revascularisation, une amputation de première intention peut être
préférable chez certains patients à un traitement médical de première intention prolongé
ayant peu de chances de réussir 1.
Néanmoins, le pronostic d’un patient en ICMI s’assombrit encore plus après une telle
intervention 2, 1, notamment en raison du caractère diffus de l’athérosclérose et de ses
conséquences cardiaques et cérébrales 3, 4
Si les douleurs sont convenablement jugulées et que le pronostic vital n’est pas mis en jeu
par l’ulcère, il importe donc de ne pas amputer d’emblée ces patients.
Mais comment distinguer le patient qui peut potentiellement guérir avec un traitement
médical optimal de celui qui n’échappera pas à l’amputation? En cas d’orientation vers un
traitement médical, en quoi consiste ce dernier ?
L’insuffisance de transport d’oxygène au niveau microcirculatoire entraîne la mort tissulaire
et génère des troubles trophiques ; les tissus hypoxiques, particulièrement vulnérables à
l’infection, ont des possibilités limitées de cicatrisation et malheureusement ces tissus
infectés majorent leur consommation locale d’oxygène, aggravant ainsi l’hypoxie tissulaire.
D’un autre côté, la mesure de la pression transcutanée d’oxygène est un outil permettant
l’évaluation du degré d’ischémie tissulaire et semble bien corrélée au pronostic du membre
ischémié.
De nombreuses études portent sur ces problématiques, dont l’étude de Eveno et al. 5 à
propos de l’oxymétrie transcutanée comme examen à visée d’orientation thérapeutique et de
l’inhalation d’oxygène comme acteur du traitement médical optimal. Chomard et al.6,
notamment, ont exploré la valeur de l’oxymétrie transcutanée distale, sans et avec
manoeuvres de sensibilisation, dans l’aide à la décision thérapeutique. Enfin, de
nombreuses études comme celle de Depairon et al.7 ont constaté que la seule valeur distale
d’oxymétrie transcutanée, si elle pouvait au-delà d’un certain seuil pronostiquer une
évolution favorable, ne permettait pas de distinguer, sous ce seuil, les patients à évolution
favorable de ceux à évolution défavorable.
Cette thèse s’inscrit ainsi dans la continuité de ces travaux en cherchant à déterminer, dans
le cadre de l’ischémie critique non revascularisable, un critère oxymétrique prédictif de
l’évolution sous traitement médical optimal avec inhalation d’oxygène sur une période
déterminée. Plusieurs pistes sont explorées : valeur absolue distale de pression trans-
cutanée d’oxygène (TcPO2) avant et après sensibilisation, valeur du gain oxymétrique distal
obtenu avec les manœuvres de sensibilisation (dTcPO2), indice du gain oxymétrique distal
pour passer de la TcPO2 distale avant sensibilisation à la TcPO2 distale après sensibilisation
(facteur de multiplication de la TcPO2). Dans ce travail, la TcPO2 distale rapportée à la
TcPO2 précordiale (rapport d’oxygénation tissulaire ROT) n’est pas étudiée.
4

- 5
5
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
 93
93
 94
94
 95
95
 96
96
 97
97
 98
98
 99
99
 100
100
 101
101
 102
102
 103
103
 104
104
 105
105
 106
106
 107
107
 108
108
 109
109
 110
110
 111
111
 112
112
 113
113
 114
114
 115
115
 116
116
 117
117
 118
118
 119
119
 120
120
 121
121
 122
122
 123
123
 124
124
 125
125
 126
126
 127
127
 128
128
 129
129
 130
130
 131
131
 132
132
 133
133
 134
134
 135
135
 136
136
 137
137
 138
138
 139
139
 140
140
 141
141
 142
142
 143
143
 144
144
 145
145
 146
146
 147
147
 148
148
 149
149
 150
150
 151
151
 152
152
 153
153
 154
154
 155
155
 156
156
 157
157
 158
158
 159
159
 160
160
 161
161
 162
162
 163
163
 164
164
1
/
164
100%