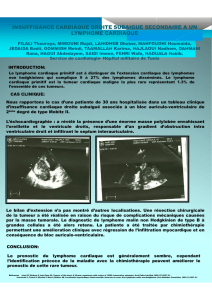
Classification pratique des lymphomes primitifs du tube digestif D

74
La Lettre de l’Hépato-Gastroentérologue - no2 - vol. III - avril 2000
DOSSIER THÉMATIQUE
dental”, c’est-à-dire focal ou pluri-focal, ou, plus rarement sous
nos climats, d’un lymphome dit “méditerranéen” ou IPSID
“Immunoproliferative Small Intestinal Disease”, c’est-à-dire
d’une atteinte diffuse d’un segment digestif, en règle de l’intes-
tin grêle (2).
La classification que nous expliciterons est celle d’Isaacson de 1999
(3), établie dès 1984, et depuis régulièrement réactualisée. Elle est
fondée sur le concept de l’existence d’un tissu lymphoïde spécifi-
quement associé aux muqueuses : MALT (Mucosa Associated Lym-
phoid Tissue), à l’origine des LPTD (se reporter à l’article de P.G.
Isaacson). En théorie “tout” LPTD provient du MALT. En pratique,
on utilise le terme de lymphome “de type MALT” pour certains
lymphomes B localisés, surtout celui de l’estomac.
La classification du lymphome digestif se fait habituellement sur
des biopsies réalisées au cours d’une exploration endoscopique.
Avant d’étudier les différentes entités de la classification d’Isaac-
son, nous préciserons quelques détails pratiques concernant les
biopsies.
LES BIOPSIES
Pour pouvoir classer un lymphome du tube digestif, le clinicien
et le pathologiste doivent se soumettre à quelques règles précises.
En effet, il est à l’heure actuelle indispensable de disposer de
biopsies suffisamment nombreuses, prélevées et conservées ou
fixées dans des conditions appropriées à l’application des tech-
niques d’immunohistochimie (IHC), de biologie moléculaire,
voire de cytogénétique. Des prélèvements fixés dans le formol à
10 % permettant éventuellement des études de biologie molécu-
laire, en particulier les techniques d’amplification (le liquide de
Bouin meilleure qualité de la morphologie), ainsi que des prélè-
vements congelés dans l’azote liquide, à sec pour la biologie
moléculaire ou dans du “Tissue Tek”, sorte de colle de préser-
vation (pour IHC), doivent ainsi être réalisés.
Classification pratique des lymphomes primitifs
du tube digestif
●
A. Lavergne-Slove*, N. Brousse**
Services d’anatomie et de cytologie pathologiques.
* Hôpital Lariboisière, Paris.
** Hôpital Necker-Enfants malades, Paris.
POINTS FORTS
POINTS FORTS
■ Diagnostic d’un lymphome digestif
➝
Biopsies suffisamment nombreuses ;
➝
Fixation des biopsies dans un milieu permettant l’immu-
nohistochimie et la biologie moléculaire (congélation ou
formol) ;
➝
Plus grande fréquence des lymphomes de phénotype B
➝
Lymphome B de l’estomac de type MALT, souvent asso-
cié à Helicobacter pylori ;
➝
Lymphome B à grandes cellules : le différencier du
carcinome ;
➝
Lymphome T digestif : peut révéler une maladie cœliaque.
L
es lymphomes digestifs comportent deux types de lym-
phomes : les lymphomes primitifs du tube digestif
(LPTD) révélés par une symptomatologie digestive,
sans localisation ganglionnaire superficielle antérieurement
connue, localisés au tube digestif ou aux ganglions mésentériques,
et les localisations digestives secondaires des lymphomes d’autres
localisations, plus rares et de même forme histologique que la
localisation primitive ; ils ne seront pas abordés ici.
Les LPTD sont les plus fréquents des lymphomes extra-gan-
glionnaires. Les localisations préférentielles sont l’estomac
(50 %), l’intestin grêle (30 %), le rectum et le côlon (20 %), et
enfin l’œsophage. Les localisations multiples sont évaluées entre
10 et 20 % (1).
Comme pour les lymphomes ganglionnaires, la classification
repose sur la distinction entre lymphome B (LB) et lymphome T
(LT), et entre lymphome de faible degré de malignité ou de grande
malignité. Tous les types de lymphomes ganglionnaires ou
presque peuvent être observés, mais certains sont plus fréquents
et regroupés dans une classification pratique où rentrent en ligne
de compte des entités anatomo-cliniques. Ils sont le plus souvent
de phénotype B (95 % des cas). Une particularité de la classifi-
cation des LPTD est de préciser s’il s’agit d’un LB de type“occi-
Abréviations
•HFL : hyperplasie lymphoïde folliculaire
•IHC : immunohistochimie
•LLE : lésions lymphoépithéliales
•MALT : mucosa associated lymphoid tissue
•MCa: maladie des chaînes alpha
3/71. THEMATIQUE 26/08/02 14:43 Page 74

Les prélèvements doivent être nombreux et concerner la tumeur,
mais aussi la muqueuse digestive “normale” à distance. Une
exploration endoscopique complète du tube digestif doit être réa-
lisée systématiquement avec biopsies étagées, même en zone
endoscopiquement normale.
Il est, par exemple, indispensable, en cas de lymphome diges-
tif T, d’étudier le duodénum par des biopsies systématiques,
afin de rechercher une éventuelle maladie cœliaque patente
ou latente. Des localisations multiples étagées dans le tube
digestif peuvent être observées dans les lymphomes de type
MALT et, a fortiori, font partie du diagnostic de polypose
lymphomateuse.
LYMPHOMES B
Les lymphomes B sont les plus fréquents des lymphomes diges-
tifs. Ils sont constitués d’une prolifération de petites ou de grandes
cellules. Les problèmes diagnostiques sont alors différents : les
proliférations à petites cellules posent plus souvent un problème
de classification, voire de confirmation de malignité ; celles à
grandes cellules peuvent poser le problème du diagnostic diffé-
rentiel entre lymphome et carcinome.
Lymphomes B à petites cellules
Les lymphomes B à petites cellules doivent être distingués des
hyperplasies lymphoïdes folliculaires (HFL) localisées. Dans
l’estomac, l’HFL est associée à d’autres lésions, ulcère gas-
trique, gastrite chronique à Helicobacter pylori (H. pylori) ou
réalise une gastrite folliculaire (4, 5). Dans l’intestin grêle,
l’HFL localisée est rare ; et sur prélèvement biopsique, il
convient de la différencier des plaques de Peyer. Dans le rec-
tum, une HFL localisée s’observe chez l’enfant – où elle réa-
lise un aspect de polype lymphoïde constitué de follicules lym-
phoïdes avec centres germinatifs – et chez l’adulte, dans les
rectites ulcéreuses, les rectites lymphoïdes folliculaires et les
rectums “exclus”. Dans toutes ces lésions lymphoïdes hyper-
plasiques, les follicules lymphoïdes ont un centre germinatif
polytypique n’exprimant pas bcl-2.
• Lymphome gastrique de type MALT, de faible malignité
(figures 1a et b) : Ce sont les plus fréquents des lymphomes
digestifs. Ce sont eux que l’on désigne couramment par
“lymphome du MALT”. Ils sont presque toujours associés à
une infection par H. pylori, et c’est l’efficacité du traitement
par éradication du germe dans plus de 50 % des cas qui a
récemment relancé tout l’intérêt de leur étude (6).
Leurs caractères histologiques sont stéréotypés, associant une
infiltration du chorion par des cellules lymphoïdes de petite taille,
des lésions lympho-épithéliales constantes et une hyperplasie
lymphoïde folliculaire : la muqueuse contient une population cel-
lulaire dense faite d’éléments lymphoïdes de petite ou moyenne
taille, les plus caractéristiques étant dits “centrocyte-like” ; elle
est parfois monocytoïde ou d’aspect lymphocytaire. Les plas-
mocytes, souvent présents dans la zone superficielle du chorion,
sont réactionnels, polytypiques dans deux tiers des cas. Dans le
dernier tiers, ces plasmocytes sont monotypiques, exprimant la
même chaîne légère d’immunoglobulines que la prolifération
lymphoïde à petites cellules, traduisant dans ce cas une diffé-
renciation plasmocytaire de la prolifération cellulaire.
La caractéristique de ce lymphome est la présence constante de
lésions lympho-épithéliales (LLE). Elles sont définies par une
infiltration et une destruction de l’épithélium des glandes et/ou
des cryptes par les cellules centrocyte-like associées à des ano-
malies épithéliales, avec un épithélium dégénératif, éosinophile,
en partie détruit. Elles reproduisent l’interaction existant entre le
lymphocyte B et l’épithélium en regard des plaques de Peyer, à
l’état normal.
L’hyperplasie folliculaire lymphoïde (HFL), sous la prolifération
lymphoïde centrocyte-like, est constante ; les follicules lym-
phoïdes peuvent être faciles à reconnaître, avec de volumineux
centres germinatifs ; dans d’autres cas, progressivement infiltrés,
colonisés et détruits par les cellules lymphoïdes tumorales, ils
sont plus difficiles à individualiser, et un reste de centre germi-
natif ne signifie pas nécessairement un contingent lymphoma-
teux de grandes cellules.
Les études immunohistochimiques montrent le phénotype B (20+,
CD79a+) de la population tumorale, permettent de préciser la
nature tumorale (monotypique, Kappa ou Lambda) ou réaction-
nelle de la population plasmocytaire, de montrer l’absence
75
La Lettre de l’Hépato-Gastroentérologue - no2 - vol. III - avril 2000
Figure 1.
Lymphome B
de l’estomac de type
MALT, à petites
cellules.
a. Aspect au faible
grossissement :
présence
d’une hyperplasie
lymphoïde folliculaire
et d’un infiltrat dense
de la muqueuse.
b. Aspect au fort
grossissement :
présence de lésions
lymphoépithéliales,
infiltration
de l’épithélium
glandulaire
par des cellules
lymphoïdes
de petite taille.
1a
1b
3/71. THEMATIQUE 26/08/02 14:43 Page 75

76
La Lettre de l’Hépato-Gastroentérologue - no2 - vol. III - avril 2000
DOSSIER THÉMATIQUE
d’expression de certains anticorps utiles au diagnostic différen-
tiel avec d’autres lymphomes B à petites cellules (IgD, CD5,
CD10, CD23), et surtout de mieux mettre en évidence les lésions
lympho-épithéliales par l’étude des marqueurs épithéliaux, (anti-
corps anticytokératine).
L’immunohistochimie est rarement nécessaire dans les cas
typiques ; elle est utile pour mettre en évidence les lésions lym-
pho-épithéliales. La recherche d’une monotypie est également
utile dans les cas à différenciation plasmocytaire.
Les techniques de biologie moléculaire avec amplification
génique (PCR) peuvent permettre la mise en évidence rapide d’un
réarrangement clonal des gènes des immunoglobulines, ce qui
peut être un élément décisif du diagnostic sur des biopsies. Les
anomalies cytogénétiques les plus fréquemment retrouvées dans
les lymphomes de type MALT sont la trisomie 3 (50 à 60 %) et
une translocation t (11, 18).
Les lymphomes de faible malignité de type MALT évoluent
lentement et restent longtemps confinés à la localisation ini-
tiale. Il n’y a pas d’urgence à traiter ce lymphome de façon
agressive et, en cas de doute diagnostique sur une biopsie, il
faut prendre le temps de réaliser d’autres biopsies, de complé-
ter l’étude histologique par la recherche d’une population lym-
phoïde montrant un même réarrangement clonal de la chaîne
lourde des Ig. L’éradication de H. pylori doit être la première
étape thérapeutique, même si son efficacité est parfois longue
à apparaître (plusieurs mois) et nécessite une surveillance endo-
scopique et biopsique prolongée. Si ce traitement s’avère insuf-
fisant, il est alors nécessaire de proposer une chimiothérapie
ou une gastrectomie totale, car les lésions sont habituellement
multicentriques.
L’évolution enfin peut aboutir au développement d’un lym-
phome B à grandes cellules, de haute malignité.
• Lymphome de type MALT de faible malignité : autres
localisations : elles peuvent survenir dans n’importe quel
segment digestif mais sont plus fréquentes dans l’intestin grêle
que dans le côlon ou le rectum, où elles sont exceptionnelles.
Leur aspect est identique à celui des localisations gastriques,
mais les lésions lympho-épithéliales, quoique présentes,
apparaissent plus rares. Leur transformation en lymphome de
grande malignité est plus fréquente que dans l’estomac, et leur
pronostic moins bon, avec un taux de survie à 5 ans inférieur
à50%.
• Lymphome de type MALT de faible malignité : IPSID :
les IPSID, exceptionnellement rencontrés sous nos climats,
sont représentés essentiellement par la maladie des chaînes
lourdes alpha (MCa), qui constitue un lymphome diffus de
type MALT se développant habituellement dans l’intestin
grêle. Ils représentent le premier exemple de l’efficacité d’un
traitement antibiotique dans la rémission d’un lymphome, bien
avant que le succès de l’éradication de H. pylori ait été reconnu
dans les lymphomes localisés de l’estomac.
La MCa, décrite en 1968, est une infiltration lymphoïde maligne
de l’intestin grêle, diffuse, sans intervalle de muqueuse saine,
caractérisée par la sécrétion d’une chaîne lourde alpha anormale,
dépourvue de chaîne légère. L’IPSID sera ultérieurement défini
par l’OMS (1976) comme une infiltration lymphoïde diffuse
de l’intestin grêle d’aspect similaire à celui observé dans la
maladie des chaînes alpha, mais sans préjuger de la nature de
l’immunoglobuline sécrétée ni du caractère bénin ou malin de
la prolifération.
Un des caractères histopathologiques essentiel de la MCa
est l’atteinte de toute la longueur de l’intestin grêle, sans laisser
d’intervalle de muqueuse saine. On décrit trois stades, de mali-
gnité croissante. Au stade A, l’infiltrat cellulaire est limité à la
muqueuse et constitué de plasmocytes “matures”, plus rarement
de lymphocytes. Dans la moitié des cas environ, des lésions simi-
laires à celles décrites dans les formes localisées de lymphome
de type MALT sont associées : foyers de prolifération de petites
cellules centrocyte-like avec LLE et follicules lymphoïdes hyper-
plasiques. Le stade C est un lymphome de grande malignité,
immunoblastique avec différenciation plasmocytaire, responsable
de tumeur(s) ulcérée(s). Le stade B est intermédiaire : l’infiltrat
atteint au moins la sous-muqueuse, les cellules plasmocytaires
présentent d’importantes anomalies cytonucléaires et des immu-
noblastes peuvent être présents (7).
Les lésions peuvent progresser ; les trois stades peuvent se suc-
céder dans le temps et/ou s’observer simultanément dans le même
segment digestif ou dans différents segments.
Les ganglions mésentériques sont habituellement (mais pas tou-
jours au stade A) atteints par la prolifération lymphoïde. L’IHC
permet d’évoquer le diagnostic de MCasur la présence dans les
plasmocytes d’une chaîne lourde alpha, sans chaîne légère asso-
ciée. Elles sont particulièrement intéressantes en cas de forme
non sécrétante ou pour le suivi lorsque la chaîne lourde alpha
n’est plus détectée dans le sang ou le liquide duodénal, alors que
des cellules malignes résiduelles peuvent être retrouvées sur les
prélèvements biopsiques (8).
Lymphomes B à grandes cellules
On distingue un peu artificiellement des lymphomes de haut grade
de type MALT et “les autres”. On peut dire d’un lymphome de
grande malignité qu’il possède les caractéristiques d’un lym-
phome de type MALT lorsqu’il existe un contingent lympho-
mateux de faible degré de malignité de type MALT, avec des
LLE caractéristiques, ou bien un tropisme particulier des élé-
ments tumoraux de grande taille pour les structures épithéliales,
mimant des LLE à grandes cellules. Quoi qu’il en soit, la dis-
tinction entre ces deux formes ne semble présenter aucun intérêt
pour le patient, et il est possible que certains lymphomes à grandes
cellules soient simplement liés à la disparition du contingent de
faible grade.
Les lymphomes B à grandes cellules (centroblastiques et immu-
noblastiques) sont les plus fréquents des lymphomes primitifs
digestifs.
Leur diagnostic est le plus souvent facile, même sur prélèvements
biopsiques : il s’agit d’une prolifération tumorale maligne détrui-
sant la muqueuse, souvent largement ulcérée et constituée par un
infiltrat lymphoïde dense, diffus, fait de cellules de grande taille,
de type centroblastique ou immunoblastique avec de nombreuses
mitoses (figures 2a et b).
3/71. THEMATIQUE 26/08/02 14:43 Page 76

Lorsque le diagnostic posé est celui d’une tumeur maligne indif-
férenciée, l’immunohistochimie le confirme facilement grâce à
l’utilisation de l’anticorps dirigé contre l’antigène commun leu-
cocytaire (CD45 RA), exprimé à la surface des cellules lym-
phoïdes, alors que les anticorps anticytokératine (KL1) marquent
les cellules épithéliales tumorales des carcinomes. Les lym-
phomes de haut grade ont par ailleurs les mêmes caractères IHC
que ceux de bas grade ; on y met plus souvent en évidence des
immunoglobulines cytoplasmiques.
Il arrive fréquemment que des grandes cellules soient obser-
vées au sein d’une prolifération B à petites cellules, et la fron-
tière entre lymphome de faible degré de malignité et de haut
grade de malignité est quelquefois difficile à établir. Il n’y a pas
à l’heure actuelle de véritable consensus sur le nombre et la
répartition des grandes cellules. De Jong et coll. proposent un
grading des lymphomes gastriques du MALT en fonction du
nombre et de l’agencement des grandes cellules lymphoïdes
activées. Ils montrent que les lymphomes de bas grade conte-
nant 1 à 10 % de cellules activées, souvent agencées en amas
n’excédant pas 20 cellules, sont significativement de plus mau-
vais pronostic que les lymphomes contenant moins de 1 % de
cellules activées dispersées ou formant des agrégats de moins
de 5 cellules (9).
Lymphomes à cellules du manteau,
polypose lymphomateuse
Les lymphomes à cellules du manteau de localisation digestive
réalisent l’aspect caractéristique d’une polypose lymphomateuse.
Ils représentent moins de 10 % des LPTD. Deux entités peuvent
être distinguées, la polypose lymphomateuse primitive vraie et
la localisation digestive d’un lymphome du manteau ganglion-
naire. L’aspect endoscopique est celui d’une polypose digestive,
avec polypes multiples, disséminés dans un ou, typiquement, plu-
sieurs segments du tube digestif. L’atteinte de l’intestin grêle et
des ganglions mésentériques est quasi constante. La maladie est
souvent découverte au stade IV, avec une atteinte médullaire dans
les deux tiers des cas environ.
L’aspect histologique est stéréotypé : les cellules tumorales sont
de petite taille, avec un noyau clivé, un cytoplasme peu abon-
dant ; elles sont parfois groupées en nodules, classiquement sans
lésion lympho-épithéliale. L’IHC montre un phénotype caracté-
ristique: les cellules lymphomateuses expriment les marqueurs
des cellules B (CD20), une immunoglobuline de surface de type
IgM, et IgD, l’antigène CD5 (marqueur habituel des cellules T),
et la cycline D1. Elles n’expriment ni CD10 (CALLA) ni CD23.
L’antigène CD5 peut être mis en évidence sur un prélèvement
fixé et inclus en paraffine (2).
Les études de biologie moléculaire ont montré les mêmes ano-
malies que celles observées dans les lymphomes du manteau,
c’est-à-dire une translocation 11;14 (JH/bcl-1), soulignant le lien
biologique entre polypose lymphomateuse et lymphome du man-
teau et un réarrangement fréquent du gène Bcl-1.
L’évolution habituelle se fait vers la dissémination du lymphome
à petites cellules, et exceptionnellement vers la survenue d’une
prolifération à grandes cellules.
Un aspect endoscopique de polypose lymphomateuse ne corres-
pond pas toujours à un lymphome du manteau, et ce diagnostic
ne peut être retenu qu’après l’étude histologique et immunohis-
tochimique. Il peut en effet correspondre à une hyperplasie lym-
phoïde folliculaire, à la localisation d’une leucémie lymphoïde
chronique, exceptionnellement à un lymphome de type MALT ;
et, récemment, ont été décrites des observations de lymphome
folliculaire à petites cellules, avec une atteinte multiple alors
exclusive de l’intestin grêle.
Lymphomes de Burkitt et de type Burkitt
Les lymphomes de Burkitt, endémiques ou sporadiques, peuvent
être observés. Ils surviennent typiquement dans la région iléo-
cæcale, chez l’enfant ou l’adulte jeune. Leurs caractères histolo-
giques et immunohistochimiques sont identiques à ceux des lym-
phomes de même type de localisation ganglionnaire.
Autres lymphomes : les autres types de lymphomes ganglion-
naires peuvent être observés dans le tube digestif, à titre tout à
fait exceptionnel, et posent d’autant plus la question du dia-
gnostic différentiel avec la localisation secondaire d’un lym-
phome ganglionnaire. Nous citerons pour exemple les lym-
phomes folliculaires.
77
La Lettre de l’Hépato-Gastroentérologue - no2 - vol. III - avril 2000
Figure 2. Lymphome B de l’estomac à grandes cellules.
a. aspect au faible grossissement : infiltration tumorale détruisant en
partie la muqueuse.
b. aspect au fort grossissement : l’infiltration tumorale est faite de
cellules lymphoïdes de grande taille.
2a
2b
3/71. THEMATIQUE 26/08/02 14:43 Page 77

78
La Lettre de l’Hépato-Gastroentérologue - no2 - vol. III - avril 2000
DOSSIER THÉMATIQUE
LYMPHOMES DIGESTIFS T
Ils sont très rares et représentent moins de 5 % des LPTD. Ils siè-
gent presque tous au niveau de l’intestin grêle, mais des localisa-
tions gastriques et plus rarement coliques ont été décrites (10, 11).
Lymphome T associé à une maladie cœliaque
Ce sont les plus fréquents des lymphomes T digestifs ; ils se déve-
loppent dans l’intestin grêle où ils sont associés à une maladie
cœliaque. Ils sont dénommés communément EATCL (enteropa-
thy associated T-cell lymphoma).
Leur particularité est d’infiltrer l’épithélium des villosités et des
glandes intestinales et d’avoir un phénotype particulier, ce qui a
suggéré une origine possible des cellules tumorales à partir de la
population des lymphocytes intestinaux intra-épithéliaux CD7+,
CD3+, CD5–, CD4–, CD8–, TiA1+(granules cytotoxiques) et sur-
tout HML1+(CD103, anticorps reconnaissant les différentes sous-
populations des lymphocytes intra-épithéliaux intestinaux). Ils
seraient développés à partir de cellules T activées cytotoxiques,
cellules qui ont été décrites dans l’épithélium des patients atteints
de maladie cœliaque.
Il s’agit d’un lymphome de haut degré de malignité, le plus sou-
vent pléomorphe à grandes cellules, parfois à cellules moyennes
ou immunoblastiques.
De rares cas pourraient correspondre à un lymphome de faible
degré histologique de malignité, leur seule lésion correspondant
à une lymphocytose intra-épithéliale majeure, de phénotype anor-
mal et présentant un réarrangement clonal T, ainsi que des ano-
malies cytogénétiques. Certains de ces cas correspondent à une
entité décrite récemment, la sprue réfractaire.
La signification de l’atrophie villositaire est imprécise. Si la mala-
die cœliaque est souvent associée à ce type de lymphome, elle
précède rarement le lymphome : dans la plupart des cas décrits,
le lymphome révèle la maladie intestinale. “Secondaire”, elle
pourrait être liée à l’action des cellules T malignes. De rares cas
de lymphomes T intestinaux sont révélés par un tableau de jéju-
nite ulcéreuse.
La présence de l’EBV a été démontrée, dans une seule étude,
dans 13 % de lymphomes T gastro-intestinaux (même pourcen-
tage que celui observé dans les lymphomes T ganglionnaires et
pulmonaires).
Autres types de lymphomes T sans maladie cœliaque
Un deuxième type de lymphome T intestinal, plus rare encore,
comporte une association à une réaction éosinophilique importante.
Les tumeurs prédominent également au niveau de l’intestin grêle,
peuvent être multiples, parfois ulcérées, nécrosées, voire se révé-
ler par une perforation. Les cellules tumorales sont souvent rares
et le diagnostic peut être difficile. La cytologie est polymorphe
avec des cellules de grande taille, parfois multinucléées.
D’autres types plus rares de lymphomes T intestinaux, sous forme
de cas isolés, ont été également décrits : lymphome intestinal immu-
noblastique T CD8 avec grains azurophiles intra-cytoplasmiques,
lymphome T intestinal à petites cellules de phénotype CD4+,
CD103–, sans maladie cœliaque associée et avec une atteinte dif-
fuse essentiellement intra-muqueuse de l’intestin grêle. ■
Mots clés. Lymphome du MALT - IPSID - Lymphome T.
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Isaacson P.G., Wright D.H. Extranodal malignant lymphoma arising from
mucosa associated lymphoid tissue. Cancer 1984 ; 53 : 2515-24.
2. Solal Céligny P., Brousse N., Fermé C. et coll. Les lymphomes. Frison
Roche Éd, 3
e
éd, 1997.
3. Isaacson P.G. Gastrointestinal lymphomas of T- and B-cell types. Mod
Pathol 1999 ; 12 : 151-8.
4. Genta R.M., Hammer H.W., Graham D.Y. Gastric lymphoid follicles in
Helicobacter pylori infection : frequency, distribution and response to triple
therapy. Hum Pathol 1993 ; 24 : 577-83.
5. De Mascarel A., Dubus P., Belleannée G. et coll. Low incidence of mono-
clonal B-cells in Helicobacter pylori gastritis patients with duodenal ulcer.
Hum Pathol 1998 ; 29 : 784-90.
6. Wotherspoon A.C., Doglioni C., Diss T.C. et coll. Regression of primary
low-grade B-cell gastric lymphoma of mucosa-associated lymphoid tissue type
after eradication of Helicobacter pylori. Lancet 1993 ; 342 : 575-7.
7. Galian A., Lecestre M.J., Scotto J. et coll. Pathological study of alpha-chain
disease with special emphasis on evolution. Cancer 1977 ; 39 : 2081-101.
8. Price S.K. Immunoproliferative small intestinal disease : a study of 13 cases
with alpha heavy-chain disease. Histopathology 1990 ; 17 : 7-17.
9. De Jong D., Boot H., Van Heerde P. et coll. Histological grading in gastric
lymphoma : pretreatment criteria and clinical relevance. Gastroenterology
1997 ; 112 : 1466-74.
10. Chott A., Dragosics B., Radaszkiewicz T. et coll. Peripheral T-cell lym-
phomas of the intestine. Am J Pathol 1992 ; 141 : 1361-71
11. Schmitt-Graff A., Hummel M., Zemlin M. et coll. Intestinal T-cell lym-
phoma : a reassessment of cytomorphological and phenotypic features in rela-
tion to patterns of small bowel remodelling. Virchows Arch 1996 ; 429 : 27-36.
12. De Bruin P.C., Jiwa N.M., Oudejans J.J. et coll. Epstein-Barr virus in pri-
mary gastrointestinal T-cell lymphomas. Association with gluten-sensitive
enteropathy, pathological features and immunophenotype. Am J Pathol 1995 ;
146 : 861-7.
LYMPHOMES B
➪De type MALT
Localisés
•Faible degré de malignité
•Grande malignité, avec ou sans contingent de faible
malignité
IPSID
•Faible degré de malignité
•Grande malignité, avec ou sans contingent de faible
malignité
➪À cellules du manteau (polypose lymphomateuse)
➪De Burkitt et de type Burkitt
➪Autres, équivalents des lymphomes ganglionnaires
•Lymphome folliculaire
•Lymphome lymphocytique
•Lymphome B à grandes cellules
➪Lymphomes associés à un déficit immunitaire
•Post-transplantation
•Acquis
•Congénital
LYMPHOMES T
•Lymphome T associé à une entéropathie (EATCL)
•Autres types, sans entéropathie
Types rares
(incluant les lésions pouvant simuler un lymphome)
Tableau. Classification des lymphomes primitifs du tube digestif.
3/71. THEMATIQUE 26/08/02 14:43 Page 78
1
/
5
100%