Lire l'article complet

234 | La Lettre de l’Infectiologue • Tome XXVIII - no 6 - novembre-décembre 2013
Actualités dans
LE TRAITEMENT DE L’HÉPATITE C
Interactions
entre les médicaments
contre l’hépatite C,
les antirétroviraux
et les immunosuppresseurs
Interactions between HCV drugs, antiretrovirals and
immunosuppressive drugs
B. Chauvin*, S. Drouot*, P. Eloy*, A. Barrail-Tran*, **, A.M. Taburet*
Sur les 33 millions de personnes infectées par
le VIH dans le monde, 4 à 5 millions seraient
également infectées par le VHC (1). La prise en
charge de cette co-infection a connu une nouvelle
avancée thérapeutique avec la mise à disposition
récente de 2 inhibiteurs de protéase (IP) du VHC, le
bocéprévir et le télaprévir. Ces traitements exposent
à un risque élevé d’interactions médicamenteuses,
que ce soit avec les antirétroviraux lors du traite-
ment des patients co-infectés par le VIH et le VHC,
ou avec les immunosuppresseurs chez les patients
transplantés, qu’ils soient infectés par un seul de
ces virus ou par les 2.
L’objectif de cet article est de faire le point sur les
interactions médicamenteuses décrites entre anti-
rétroviraux, immunosuppresseurs et traitements
de l’hépatite C.
Résumé des caractéristiques
pharmacocinétiques
de ces médicaments
Les principales caractéristiques pharmacocinétiques
des médicaments contre l’hépatite C et le VIH et
des immunosuppresseurs sont résumées dans le
tableau, p. 236.
Médicaments de l’hépatite C
Les 2 traitements majeurs de l’hépatite C, la riba-
virine et l’interféron, présentent peu d’interactions
d’ordre pharmacocinétique, c’est-à-dire infl uen-
çant les concentrations des médicaments associés.
L’interféron (pégylé ou non) est principalement
éliminé dans les urines sous forme inchangée. La
ribavirine n’infl uence pas l’activité des cytochromes
P 450 (CYP450). Son élimination passe par 2 voies
métaboliques : une phosphorylation intracellulaire
réversible et une voie impliquant une déribosylation
et une hydrolyse de la liaison amide. L’élimination
est essentiellement urinaire (2).
Les 2 IP du VHC actuellement commercialisés, le
bocéprévir et le télaprévir, présentent un méta-
bolisme complexe, associant la voie classique par
les CYP3A et par d’autres voies métaboliques plus
ou moins bien identifi ées, notamment les aldoké-
toréductases pour le bocéprévir. De plus, ils sont
inhibiteurs du CYP3A4 et des transporteurs, que ce
soit la P-glycoprotéine (P-gp), transporteur d’effl ux
facilitant la sortie du substrat de la cellule, ou les
OATP (Organic Anion-Transporting Polypeptide) 1B1
et 1B3, transporteurs d’infl ux facilitant l’entrée du
substrat dans la cellule. L’élimination sous forme
inchangée et sous forme de métabolites est essen-
tiellement fécale. La demi-vie est plus longue pour
* Service de pharmacie, hôpital
Bicêtre, Le Kremlin-Bicêtre.
** Département de pharmacie
clinique et de pharmacocinétique,
université Paris-Sud, EA4123,
Châtenay-Malabry.
B. Chauvin

La Lettre de l’Infectiologue • Tome XXVIII - no 6 - novembre-décembre 2013 | 235
Points forts
le télaprévir (9 à 11 heures) que pour le bocéprévir
(3 à 4 heures) [3, 4].
Antirétroviraux
Le profi l pharmacocinétique des inhibiteurs nucléo-
sidiques et nucléotidiques (ténofovir) de la trans-
criptase inverse limite leur implication dans des
interactions d’ordre pharmacocinétique. C’est leur
forme intracellulaire triphosphorylée qui est active,
et ces composés sont principalement éliminés par
voie urinaire sous forme inchangée (ténofovir, emtri-
citabine et lamivudine), même si certains sont méta-
bolisés au niveau hépatique sans implication des
CYP450 (l’abacavir et la zidovudine sont éliminés
par glucuronoconjugaison par les UDP-glucuronosyl-
transférases, et la moitié de la dose de didanosine
est éliminée par la voie des xanthines) [5].
Les inhibiteurs non nucléosidiques de la transcriptase
inverse (INNTI) [névirapine, éfavirenz, étravirine
et rilpivirine] ont une demi-vie longue permet-
tant théoriquement une administration en 1 prise
quotidienne (5), et un métabolisme hépatique par
les CYP : CYP2B6 pour la névirapine et l’éfavirenz,
CYP2C pour l’étravirine, et CYP3A pour la rilpivirine.
La névirapine, l’étravirine et l’éfavirenz présentent
un effet inducteur enzymatique modéré (5).
Les IP du VIH actuellement prescrits (lopinavir et,
surtout, atazanavir et darunavir associés au ritonavir)
sont tous métabolisés par le CYP3A4, dont ils sont
également inhibiteurs – en particulier le ritonavir,
inhibiteur très puissant –, particularité qui a conduit à
associer cette molécule à un autre IP afi n d’améliorer
ses propriétés pharmacocinétiques (5).
Parmi les inhibiteurs d’entrée, le maraviroc, antago-
niste du récepteur CCR5, est substrat du CYP3A4,
mais n’a pas d’effet inhibiteur ou inducteur
notable (5). La nature peptidique de l’enfuvirtide
explique que son métabolisme se fasse essentiel-
lement par hydrolyse, limitant ses interactions
potentielles. Parmi les inhibiteurs de l’intégrase, le
raltégravir et le dolutégravir (commercialisé prochai-
nement) sont principalement éliminés par glucu-
ronoconjugaison par l’UGT1A1 ; peu d’interactions
médicamenteuses sont donc attendues et ont été
décrites, si ce n’est une inhibition par l’atazanavir et
une induction par la rifampicine (6, 7). L’elvitégravir
vient d’obtenir l’AMM européenne associé à un inhi-
biteur puissant du CYP3A, le cobicistat ; le potentiel
d’interaction avec les substrats du CYP3A est donc
important, comme pour les IP associés au ritonavir.
Immunosuppresseurs
Les immunosuppresseurs prescrits en prévention du
rejet du greffon présentent un index thérapeutique
étroit. Les inhibiteurs de la calcineurine (tacrolimus
et ciclosporine), les inhibiteurs de la mTOR (sirolimus
et évérolimus) et la prednisone sont substrats à la
fois de la P-gp et des CYP3A. En outre, la ciclosporine
a une activité inhibitrice sur la P-gp et l’OATP1B1.
Les autres immunosuppresseurs, acide mycophéno-
lique (MPA, forme active du mycophénolate mofétil
ou du mycophénolate sodique) et azathioprine, sont
métabolisés par des voies métaboliques autres que
les CYP. Le MPA est glucuronoconjugué par les UGT
hépatiques. L’azathioprine est une prodrogue méta-
bolisée en 6-mercaptopurine active par réaction non
enzymatique. L’élimination est rapide, essentielle-
ment par voie rénale.
Interactions
entre les médicaments
de l’hépatite C
et les antirétroviraux
Coadministrée avec certains inhibiteurs nucléosi-
diques de la transcriptase inverse (INTI) [didanosine
et zidovudine], la ribavirine augmente le risque de
toxicité mitochondriale et donc de pancréatite et
d’acidose lactique (8). Une augmentation du risque
d’anémie a été décrite en cas de coadministration de
ribavirine et de zidovudine, risque accru en présence
d’IP du VHC (9). L’association est donc déconseillée.
En revanche, la coadministration avec l’abacavir,
l’emtricitabine, la lamivudine et le ténofovir est
possible (10).
Les interactions du bocéprévir ou du télaprévir avec
les principaux médicaments antirétroviraux sont
résumées dans la fi gure 1, p. 237. Les concentrations
»
Le télaprévir et le bocéprévir ont un métabolisme complexe et sont substrats et inhibiteurs du cyto-
chrome P450-3A (CYP3A), ce qui entraîne de nombreuses interactions médicamenteuses.
»
L’association avec la majorité des inhibiteurs de la protéase du VIH n’est pas recommandée. Mais l’asso-
ciation est possible avec l’atazanavir, renforcée par le ritonavir, ou avec le raltégravir, dont l’élimination
ne dépend pas des CYP, ce qui permet le traitement des patients co-infectés.
»
L’administration du télaprévir et du bocéprévir après une transplantation est possible, sous réserve
d’une diminution souvent importante de posologie des immunosuppresseurs métabolisés par le CYP3A
(ciclo sporine, tacrolimus, évérolimus et sirolimus) et sous réserve d’un suivi thérapeutique quotidien, du
début du traitement jusqu’à l’équilibre des concentrations sanguines.
Mots-clés
Immunosuppresseurs
Antirétroviraux
Médicaments
del’hépatiteC
Cytochrome
Interaction
médicamenteuse
Highlights
»
Direct Acting Antivi-
rals (DAA), telaprevir and
boceprevir have complex
metabolic pathways. They are
substrate and inhibitors of
CYP3A and a number of drug-
drug interactions have been
reported.
»
Treatment of HIV and HCV
coinfected patients is possible,
however antiretrovirals should
be selected cautiously. Coad-
ministration with ritonavir-
boosted atazanavir and
raltegravir is possible without
dose adjustment. A decrease
in concentrations of other
ritonavir-boosted HIV-protease
inhibitors has been reported
when combined with telaprevir
or boceprevir.
»
An important increase in
concentrations of calcineu-
rine inhibitors (tacrolimus and
ciclosporine) or mTOR inhibi-
tors (sirolimus and everolimus)
which are CYP3A substrates,
has been reported in healthy
volunteers when coadmin-
istered with telaprevir or
boceprevir. Treatment of HCV-
infected transplant recipients is
feasible, but daily therapeutic
drug monitoring of immuno-
suppressive therapy must be
performed to optimize dosing
regimen and avoid high
concentrations of immunosup-
pressive drugs.
Keywords
Immunosuppressive drugs
Antiretrovirals
Hepatitis C drugs
Cytochrome
Drug-drug interaction

236 | La Lettre de l’Infectiologue • Tome XXVIII - no 6 - novembre-décembre 2013
Interactions entrelesmédicaments contrel’hépatiteC,
lesantirétroviraux etlesimmunosuppresseurs
Actualités dans
LE TRAITEMENT DE L’HÉPATITE C
Tableau. Principales caractéristiques pharmacocinétiques des antiviraux (VHC et VIH) et immunosuppresseurs.
Molécule Biodisponibilité
(%) Métabolisme Élimination
rénale sous forme
inchangée (%)
Demi-vie Commentaires Réf.
Médicaments de l’hépatite C
Autres Interféron α> 60 s.c. Protéolyse tubulaire Négligeable 160 h (pégylé)
4 h sinon
Ribavirine 45-65 Phosphorylation/déribosylation puis
hydrolyse de la fonction amide 30 300 h Activation par phosphorylation
(2)
IP Bocéprévir – Aldokétoréductase
CYP3A4, 3A5 Négligeable 3,4 h Inhibiteur CYP3A4/5
Inhibiteur P-gp
Inhibiteur OATP1B1/3
(3)
Télaprévir – CYP3A4, 3A5 Négligeable 9 à 11 h Inhibiteur CYP3A4/5
Inhibiteur P-gp
Inhibiteur OATP1B1/3
(3)
Antirétroviraux
INTI Abacavir 75 – Négligeable 0,8 à 1,5 h Activation par phosphorylation
(5)
Didanosine 40 – 50 1 à 2 h Activation par phosphorylation
(5)
Emtricitabine 90 – 80 9 h Activation par phosphorylation
(5)
Lamivudine 80 – 80 2 à 3 h Activation par phosphorylation
(5)
Ténofovir 40 – 80 14 h Activation par phosphorylation
(5)
Zidovudine 60 Glucuronoconjugaison 20 1 à 1,5 h Activation par phosphorylation
(5)
INNTI Névirapine 90 CYP2B6 et autres CYP minoritaires < 15 25 à 30 h Inducteur CYP3A4, 2B6
(5)
Éfavirenz 50 CYP2B6 et autres CYP minoritaires Négligeable 50 h Inducteur CYP3A4
Inhibiteur CYP2C9, 2C19
(5)
Étravirine – CYP3A4, 3A5, 2C9, 2C19 Négligeable 30 à 40 h Inducteur CYP3A4 (modéré)
Inhibiteur CYP2C9, 2C19
(modéré)
(5)
Rilpivirine – CYP3A4 et autres CYP minoritaires – 35 à 50 h Inhibiteur P-gp
(12)
IP Atazanavir/ritonavir – CYP3A Négligeable 8 à 9 h Inhibiteur puissant du CYP3A
(5)
Darunavir/ritonavir – CYP3A Négligeable 15 h Inhibiteur puissant du CYP3A
(5)
Fosamprénavir/
ritonavir – CYP3A Négligeable 12 à 15 h Inhibiteur puissant du CYP3A
Lopinavir/ritonavir – CYP3A Négligeable 5 à 6 h Inhibiteur puissant du CYP3A
(5)
Inhibiteur
d’entrée Maraviroc 25-35 CYP3A Négligeable 17 h Substrat P-gp
(5)
Enfuvirtide 70 Peptidases, protéinases Négligeable 3 à 8 h –
(5)
Inhibiteur
del’intégrase Raltégravir – Glucuronoconjugaison – 9 h –
Dolutégravir – UGT – 12 h –
(7)
Elvitégravir – CYP3A4 – Associé au cobicistat
(inhibiteur puissant du CYP 3A)
Immunosuppresseurs
Inhibiteurs
delacalcineu-
rine
Tacrolimus 25 CYP3A4, 3A5 Négligeable 10 à 12 h Substrat P-gp
Ciclosporine 30 CYP3A4, 3A5 Négligeable 10 à 12 h Inhibiteur OATP1B1
Substrat P-gp
Inhibiteurs
delamTOR Sirolimus CYP3A4, 3A5 Négligeable 60 h Substrat P-gp
Évérolimus CYP3A4, 3A5 Négligeable 25 h Substrat P-gp
Autres MPA1Prodrogue 94 UGT Négligeable 17 h –
6-mercaptopurine2Prodrogue 83 Xanthine oxydase Négligeable 2 h –
1 Administré sous forme de mycophénolate mofétil ou de mycophénolate sodique. 2 Administré sous forme d’azathioprine.
IP: inhibiteurs de protéase; CYP: cytochrome; P-gp: glycoprotéine; OATP:
Organic Anion-Transporting Polypeptide
.

Figure 1. Interactions entre les IP du VHC et les antirétroviraux.
0,25
0,75
1,25
VHC
Télaprévir Bocéprévir
+ EFV
EFV : éfavirenz ; LPV : lopinavir ; DRV : darunavir ; ATV : atorvastatine ; TDF : ténofovir ; RGV : raltégravir.
+ EFV+ LPV+ LPV+ DRV+ DRV+ ATV + ATV+ TDF+ TDF+ RGV + RGV
VIH
0,5
1
1,5
AUC association/AUC seuil
0
La Lettre de l’Infectiologue • Tome XXVIII - no 6 - novembre-décembre 2013 | 237
Actualités dans
LE TRAITEMENT DE L’HÉPATITE C
du télaprévir et du bocéprévir sont diminuées par
l’éfavirenz : lors de la coadministration de bocéprévir
et d’éfavirenz, la diminution de l’aire sous la courbe
(ASC) du bocéprévir s’accompagne d’une augmen-
tation de l’ASC de l’éfavirenz ; cette association n’est
donc pas recommandée. La coadministration de
télaprévir et d’éfavirenz se traduit par une baisse
de l’exposition aux 2 molécules. Un essai clinique a
montré la possibilité de compenser la diminution de
l’exposition au télaprévir en présence d’éfavirenz par
une augmentation de posologie (passage de 800 mg
à 1 125 mg toutes les 8 heures) [9].
Les interactions lors de la coadministration avec les
IP du VIH sont complexes, diffi cilement prévisibles
et bidirectionnelles, affectant les concentrations des
IP du VIH et du VHC, comme le montre le rapport
des ASC de chaque médicament associé, par rapport
à chaque médicament administré seul (fi gure 1).
L’association au télaprévir entraîne une réduction
de l’exposition (quantifi ée par l’ASC) au darunavir,
alors que le lopinavir reste inchangé ; en revanche,
l’exposition à l’atazanavir est légèrement augmentée.
Le bocéprévir entraîne une réduction des concentra-
tions du darunavir, du lopinavir et de l’atazanavir.
Le ténofovir ne modifi e pas la pharmacocinétique
du bocéprévir ni du télaprévir. En revanche, le daru-
navir, le lopinavir et l’atazanavir réduisent signifi -
cativement les concentrations de télaprévir et de
bocéprévir : ces associations ne sont pas conseillées.
Par contre, l’interaction moins importante avec l’ata-
zanavir associé au ritonavir permet de privilégier, si
nécessaire, cette association.
Aucune interaction significative n’a été décrite
entre le bocéprévir ou le télaprévir et le raltégravir ;
cette association doit donc être privilégiée chez les
patients co-infectés par le VIH et le VHC lorsque le
génotype du VIH le permet (3, 11). Les IP du VHC
augmentent l’exposition au ténofovir. Cette augmen-
tation modérée requiert une vigilance accrue concer-
nant la toxicité rénale du ténofovir (4).
Le maraviroc et la rilpivirine étant métabolisés par le
CYP3A, mais n’étant ni inhibiteurs ni inducteurs, une
augmentation de leur concentration est attendue
lors de la coadministration avec le bocéprévir et le
télaprévir. La surveillance de la tolérance (en parti-
culier pour la rilpivirine) sera renforcée (12).
Ces études d’interactions, nécessaires pour les dossiers
d’enregistrement, permettent d’identifi er les interac-
tions à risque, mais elles sont réalisées chez des volon-
taires sains, avec des objectifs pharmacocinétiques et
de tolérance. L’effi cacité de telle ou telle association
devra être vérifi ée par des essais cliniques incluant les
malades auxquels ces médicaments sont destinés.
Interactions
entre antirétroviraux
et immunosuppresseurs
L’effet inducteur enzymatique des INNTI est suscep-
tible de diminuer l’exposition aux inhibiteurs de la
mTOR et de la calcineurine. Cette interaction est
cependant minime dans la majorité des cas et se
gère facilement par un suivi thérapeutique régulier
de ces immunosuppresseurs. Cela a notamment été
mis en évidence lorsque l’éfavirenz est associé à la
ciclosporine ou au tacrolimus (13, 14).
L’effet inhibiteur enzymatique des IP (CYP3A4,
CYP3A5 et P-gp notamment) conduit à une augmen-
tation très importante des concentrations de certains
immunosuppresseurs. Les posologies d’immunosup-
presseurs doivent être drastiquement réduites, avec
un suivi très régulier, voire quotidien, de leurs concen-
trations sanguines, notamment si l’IP est boosté
par le ritonavir. Ainsi, la posologie de tacrolimus est
réduite de 99 % chez le patient transplanté traité par
l’association lopinavir-ritonavir. Pour obtenir de telles
réductions de posologies, la diminution de la dose par
prise doit s’accompagner d’un espacement des doses :
des intervalles de 7 à 25 jours ont été décrits dans la
littérature (14). Un intervalle de 1 semaine entre les
prises a également été appliqué avec succès pour le
sirolimus lors de la coadministration avec le fosam-
prénavir boosté par le ritonavir. Dans cette optique,
la mise à disposition de formes faiblement dosées
(Modigraf
®
0,2 mg pour le tacrolimus et Néoral
®

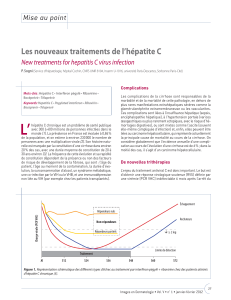
Figure 2. Ratio des ASC des inhibiteurs de la calcineurine avec ou sans inhibiteurs de
protéase du VHC.
10
30
50
Bocéprévir
Ciclosporine Tacrolimus
Télaprévir
20
40
60
70
AUC association/AUC seuil
0
238 | La Lettre de l’Infectiologue • Tome XXVIII - no 6 - novembre-décembre 2013
Interactions entrelesmédicaments contrel’hépatiteC,
lesantirétroviraux etlesimmunosuppresseurs
Actualités dans
LE TRAITEMENT DE L’HÉPATITE C
25 mg pour la ciclosporine) simplifi e l’adaptation
des doses d’immunosuppresseur.
Les corticoïdes étant également métabolisés par le
CYP3A, il est probable que les interactions seront
similaires à celles décrites ci-dessus, avec notamment
une augmentation des concentrations en présence
d’IP/r. La plus petite dose de corticoïdes sera privi-
légiée et le suivi clinique sera renforcé.
L’intérêt du raltégravir chez le patient transplanté
hépatique a été démontré dans l’essai clinique ANRS
148 Liveral. En effet, en plus d’un bon profi l d’effi ca-
cité et de tolérance, cette molécule n’est pas méta-
bolisée par le CYP 3A et sa pharmacocinétique n’est
pas affectée par l’altération de la fonction hépatique
due à l’hépatite C.
Interactions entre
médicaments de l’hépatite C
et immunosuppresseurs
Le bocéprévir et le télaprévir augmentent de façon
importante les concentrations de tacrolimus et,
dans une moindre mesure, celles de la ciclosporine,
comme le montre la fi gure 2 (4). Ainsi, l’ASC de
la ciclosporine est multiplié en moyenne par 3 en
présence de bocéprévir (15) et par 4 en présence de
télaprévir chez les volontaires sains (9). L’ampleur de
ces interactions est encore plus grande pour le tacro-
limus, avec une multiplication de l’ASC de l’immuno-
suppresseur par 17 en présence de bocéprévir (15) et
par 70 en présence de télaprévir (9). Ces interactions
doivent être gérées par des équipes pluridiscipli-
naires associant des pharmaco logues et des clini-
ciens experts. Les adaptations de posologie suivront
les mêmes règles que celles proposées avec les IP
du VIH renforcés par le ritonavir, telles que résu-
mées précédemment. Des expériences ponctuelles
montrent la faisabilité de la coadministration du
bocéprévir, voire du télaprévir avec la ciclosporine
ou le tacrolimus (16, 17).
Compte tenu de ces interactions importantes, la
prise en charge après une transplantation de patients
co-infectés par le VIH et le VHC est complexe. Dans
ce contexte, un traitement antirétroviral à base de
raltégravir évitera les interactions avec les immuno-
suppresseurs et le télaprévir ou le bocéprévir.
De même, les taux d’hémoglobine doivent être
contrôlés très régulièrement dans le but de rechercher
une éventuelle anémie, toxicité la plus fréquemment
observée (17). Outre ces interactions médicamen-
teuses pharmacocinétiques, qui peuvent être gérées
par des équipes expérimentées, il faut considérer
également certaines interactions d’ordre pharmaco-
dynamique. Ainsi, la coadministration d’azathioprine
et de ribavirine, myélotoxiques, doit être évitée (18).
Conclusion
Les interactions entre les médicaments contre
l’hépa tite C, les antirétroviraux et les immuno-
suppresseurs sont donc nombreuses. L’effet des
traitements anti-infectieux sur les inhibiteurs de la
calcineurine et sur les inhibiteurs de la mTOR est
aujourd’hui bien connu. Des précautions simples
lors de la mise en place du traitement immunosup-
presseur (doses faibles en cas de coadministration
de ritonavir notamment) et un suivi régulier des
concentrations sanguines doivent en assurer l’effi -
cacité et l’absence de toxicité. La ribavirine doit être
utilisée avec précaution, que ce soit avec certains
INTI ou avec l’azathioprine. Mais le problème le plus
complexe à gérer réside dans les interactions des
IP du VHC avec les IP du VIH et les INNTI dans le
cadre de la prise en charge des patients co-infectés
par le VIH et le VHC. À cet égard, par son métabo-
lisme particulier qui réduit le risque d’interactions,
le raltégravir constitue une alternative prometteuse
dans la prise en charge du patient co-infecté par le
VIH et le VHC. De nombreux médicaments actifs sur
le VHC sont en cours de développement ; espérons
que leur profi l pharmacocinétique limitera les inter-
actions et facilitera la prise en charge des patients
co-infectés par le VIH et le VHC ou la prise en charge
complexe des patients transplantés pour éviter la
récidive virale C. ■
Les auteurs déclarent
nepasavoir deliens d’intérêts.
 6
6
1
/
6
100%