Facteur tissulaire et cancer Tissue factor and cancer »
publicité

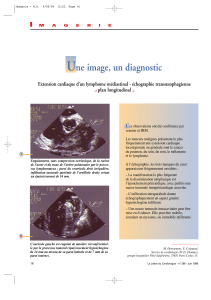
Thromboses et hémopathies malignes dossier Facteur tissulaire et cancer Tissue factor and cancer P. Nguyen* également douée de propriétés pléiomorphes impliquées dans le développement des cancers. L’expression du FT par les monocytes et les polynucléaires lui confère un rôle dans l’immunité innée. Son expression par les cellules endothéliales activées pourrait intervenir, avec d’autres facteurs procoagulants, dans la constitution des niches favorisant l’éveil tumoral. Cette glycoprotéine, qui est un récepteur du facteur VII, existe sous une forme entière et sous une isoforme tronquée soluble qui joue un rôle déterminant dans la biologie du cancer. L’implication du FT dans la migration et l’invasion tumorale est par ailleurs sous le contrôle de mi-RNA, ce qui laisse entrevoir des possibilités thérapeutiques de modulation de son expression. Le dosage du FT soluble, qui pourrait rejoindre la panoplie des biomarqueurs prédictifs du risque thrombotique chez les patients atteints de cancer, nécessite toutefois encore d’être validé. Mots-clés : Facteur tissulaire – Angiogenèse – Cancer. L e facteur tissulaire (FT) joue un rôle déterminant et tient une place à part dans la biologie du cancer. En effet, cette glycoprotéine d’expression tissulaire, très ubiquitaire, est à la fois le facteur déclenchant de la coagulation plasmatique et un authentique récepteur cellulaire, capable d’activer de multiples voies de signalisation. Différents modèles ont établi le rôle du FT dans des processus de migration cellulaire, d’angiogenèse, de prolifération et de dissémination tumorale ainsi que dans la thrombogénicité associée au cancer (1, 2). Enjeux en biologie du cancer L’intérêt majeur qu’a suscité le FT est probablement en lien direct avec la fonction procoagulante de cette molécule. L’apparition et le développement d’une tumeur sont associés à un risque thrombotique élevé, plus veineux qu’artériel, mais toujours caractérisé par Correspondances en Onco-Hématologie - Vol. IX - n° 2 - mars-avril 2014 Summary RÉSUMÉ » Le facteur tissulaire (FT ) est une molécule procoagulante, Tissue factor ( TF) is a pro-coagulant molecule with pleiomorphic features involved in the development of cancer. TF expression by monocytes and polymorphonuclears provides it with an implication in innate immunity. Also expressed by activated endothelial cells, it could take part, with other procoagulant agents, in the formation of niches favoring tumor emergence. This glycoprotein acts as a receptor for factor VII and exists as a transmembrane full molecule or as a truncated soluble isoform. The latter is determinant in the biology of cancer. The involvement of TF in tumor cells migration and invasiveness is moreover controlled by miRNA, which suggests possible therapeutic modulation of its expression. Soluble TF assays, which could join the array of biomarkers predictive of thrombosis risk in cancer patients, still however require validation. Keywords: Tissue factor – Angiogenesis – Cancer. la sévérité de la thrombose (propension aux récidives, y compris sous antivitamines K [AVK]) et par le caractère insolite de certaines localisations. La thrombogénicité observée au cours du cancer n’est pas univoque. S’agit-il de la conséquence directe de l’expression du FT par la tumeur elle-même ? Cela impliquerait un processus d’extravasation tumorale. Est-ce la manifestation délétère d’une réponse innée face à la tumeur ? Dans ce cas, quelles seraient les cellules impliquées ? Le FT “soluble”, libre ou véhiculé par des microparticules, joue-t-il un rôle déterminant ? Ce FT soluble pourrait-il constituer un biomarqueur prédictif du risque thrombotique ? Pourquoi la thrombose associée au cancer résiste-t-elle aux AVK ? Comment, à l’inverse, interpréter l’efficacité des héparines de bas poids moléculaire (HBPM) ? Quelle pourrait être la place de nouveaux antithrombotiques dans un tel contexte ? En parallèle se pose la question du rôle du FT dans le développement de la tumeur elle-même. En effet, des modèles expérimentaux indiquent clairement le rôle * Service d’hématologie, pôle de biologie, CHU de Reims, et EA3801-HERVI faculté de Reims, université Reims-ChampagneArdenne. 69 Thromboses et hémopathies malignes dossier du FT dans l’angiogenèse tumorale, mais également dans la prolifération tumorale et le processus métastatique. Carte d’identité d’une protéine peu connue Bien connu des biologistes en tant que réactif de laboratoire sous le nom de “thromboplastine”, le FT est encore assez peu familier pour le clinicien, dans la mesure où cette molécule n’est pas explorée par des analyses médicales (figure). Il s’agit d’une glycoprotéine transmembranaire (masse moléculaire de 47 kDa), constituée d’un domaine extracellulaire et de 2 courts domaines intramembranaire et cytoplasmique (3). Ce récepteur appartient à la famille des cytokines de classe 2. Il est doté d’une très forte affinité pour le facteur VII, qu’il lie sous sa forme native ou activée (FVIIa). Ainsi, le complexe FT-FVIIa favorise l’auto-activation du FVII et l’activation des facteurs IX et X. Les FVII, FX et FIX sont des Gla-protéines (dépendant de la vitamine K) et des zymogènes de sérine-protéases, capables de se fixer par des ponts calciques aux phospholipides anioniques. Il existe une forme “intégrale” de FT (full length Tissue Factor [flTF]) et une isoforme, tronquée (30 kDa), résultant d’un épissage alternatif (4). Cette isoforme (alternatively spliced Tissue Factor [asTF]) est soluble puisque les domaines transmembranaire et cytoplasmique y ont été remplacés par un domaine unique C-terminal (40 acides aminés). Cette forme soluble serait dotée d’une activité procoagulante faible. L’asTF joue un rôle déterminant dans la biologie du cancer. TFPI K1 K2 FVIIa FXa K3 C FT Membrane TFPI : Tissue Factor Pathway Inhibitor. Figure. Relations entre le facteur tissulaire et les autres facteurs de la coagulation. 70 Dans sa forme intégrale, le FT existe sous une forme cryptique, non procoagulante. L’activité procoagulante sous-entend donc un ou plusieurs mécanismes de “dé-encryptation”. Parmi ces derniers, l’exposition des phospholipides anioniques (phosphatidylsérine, principalement) est mise en avant. Par ailleurs, certains travaux suggèrent l’existence d’une dé-encryptation “allostérique” du FT, mettant en jeu une protéine disulfide isomérase (PDI), qui régule la conformation du FT au niveau des cystéines 186 et 209 (5). Ainsi, l’oxydation ou l’isomérisation du FT convertit (switch) une forme peu procoagulante en une molécule fortement procoagulante. L’activité procoagulante du FT est régulée par le TFPI (Tissue Factor Pathway Inhibitor) [6]. Il s’agit d’une protéine de 34 kDa, synthétisée par les mégacaryocytes et l’endothélium. La structure du TFPI est caractérisée par 3 boucles de Künitz, qui interagissent avec les facteurs VIIa (K1) et Xa (K2). Le complexe quadrimoléculaire ainsi formé n’est pas procoagulant. Ce mécanisme d’inhibition est original dans la mesure où le FXa joue un rôle pivot dans la régulation de la génération de thrombine, en participant à l’inhibition de la phase d’initiation. Expression du FT dans les tissus et les cellules d’origine hématopoïétique Le FT est très largement exprimé, de façon constitutive, dans les tissus. Certains organes − le poumon, le cerveau, le placenta − sont très riches en FT. À l’inverse, des organes comme le thymus, la rate et le foie en contiennent peu. Le FT est exprimé par les cellules d’origine hématopoïétique. L’expression du FT par les monocytes est inductible, notamment en réponse à des lipopolysaccharides (LPS) d’origine bactérienne. Cette induction est médiée par le récepteur CD14 associé à TLR-4 et s’intègre dans les réponses immunitaires innées. Les voies de signalisation en cause impliquent p38-MAPK. La région régulatrice du gène FT présente des sites de fixation pour différents facteurs de transcription (AP1, SP1, NF-κB). Ainsi, l’expression du FT apparaît en réponse au stress et lors de l’apoptose. Le FT est exprimé par les cellules dendritiques d’origine monocytaire et par les macrophages, mais également par les cellules endothéliales et des progéniteurs endothéliaux issus de cellules souches hématopoïétiques, exprimant CD34 (7). Le FT est présent (ARNm et protéine) dans les polynucléaires neutrophiles (PNN). Cette notion, longtemps Correspondances en Onco-Hématologie - Vol. IX - n° 2 - mars-avril 2014 Facteur tissulaire et cancer controversée, semble aujourd’hui établie. Récemment, M. Demers et al. (8) ont mis en lumière l’expression du FT par les PNN activés, lors du phénomène de NETose (correspondant à la formation de Neutrophil Extracellular Trap). Là encore, cela témoigne d’un lien entre l’expression du FT et les mécanismes de défense innée de l’organisme (9). La présence de FT a été mise en évidence au niveau des plaquettes, mais ces données sont sujettes à caution. Un article récent de l’équipe de K.G. Mann (10), utilisant une méthodologie robuste, réfute la présence de FT. Les plaquettes pourraient néanmoins jouer un rôle lors de la dé-encryptation du FT, soit par l’apport de phospholipides, soit par le biais de la PDI. tion inverse entre l’expression de FT et celle de miR-19, observée aux stades I et II du cancer colique mais pas au-delà. L’ensemble de ces données obtenues ex vivo suggère un rôle du FT dans l’invasion tumorale et ouvre de nouvelles perspectives dans le cancer colique. Le miR-19a intervient également dans l’expression du FT par les cellules tumorales mammaires. D’autres mi-RNA (miR-19b, miR-20a, miR-93, miR-106b, miR-126) interviennent dans la régulation de l’expression du FT par les cellules du microenvironnement tumoral (monocytes, cellules endothéliales et musculaires lisses), mais également par les cellules tumorales notamment les léiomyosarcomes (14). La modulation d’expression du FT par les si-RNA est prometteuse dans la mesure où elle permet de réduire la néovascularisation (15). Expression du FT par les tumeurs Une récente étude a évalué le niveau d’expression du gène du FT dans différentes tumeurs solides et hémopathies. Ce travail a montré que les tumeurs solides, dans leur grande majorité, expriment le FT. Cette expression est hétérogène, quel que soit l’organe impliqué, mais elle peut être forte, particulièrement dans les cancers digestifs et pancréatiques, réputés fortement thrombogènes (11). Au contraire, le FT n’est pas exprimé par les hémopathies lymphoïdes, qu’elles soient d’origine B ou T. Cette observation est en lien avec la très faible, voire l’absence de capacité d’expression du FT par la lignée lymphocytaire non pathologique (12). FT, mi-RNA et invasion tumorale Le FT joue un rôle dans la migration et l’invasion tumorales. Dans un modèle utilisant des lignées de cancer colique, il a été démontré que ces cellules exprimaient fortement le FT. Cette expression est régulée négativement par des micro-RNA (mi-RNA-19a, miR-19) avec, pour conséquence, un ralentissement de la migration cellulaire et une diminution de l’invasion tumorale (13). Cette inhibition de la migration cellulaire passe par la régulation de la métalloprotéinase matricielle MMP-9. À partir de l’analyse directe de tumeurs coliques, ce travail a montré que l’expression de FT est plus importante dans le tissu tumoral qu’au niveau du tissu sain, à partir du stade II de la maladie. L’expression du FT augmente ensuite avec les stades d’extension. De façon intéressante, le niveau d’expression de miR-19a s’élève de façon significative comparativement au tissu sain, mais cette surexpression n’est pas corrélée avec le stade évolutif du cancer. Les auteurs rapportent une corréla- Correspondances en Onco-Hématologie - Vol. IX - n° 2 - mars-avril 2014 FT et éveil tumoral Il existe aujourd’hui des arguments expérimentaux montrant que le FT joue un rôle dans l’éveil tumoral. En effet, une cellule gliale n’exprimant pas le FT est viable mais latente (tumor dormancy). En revanche, l’expression du FT favorise la transition tumorale. Dans un modèle glial, la croissance tumorale s’accompagne d’une modification permanente du microenvironnement, avec le recrutement de cellules vasculaires et myéloïdes (16). Ces modifications microenvironnementales modifient le phénotype tumoral mais également l’expression génique et la méthylation de l’ADN. Ainsi, le FT et les systèmes procoagulants pourraient participer à la constitution d’une niche favorable à l’éveil et à la progression d’une tumeur à partir de cellules quiescentes. FT et métastases Le FT joue un rôle dans le phénomène métastatique. Différentes données expérimentales ont pu montrer le rôle du FT dans l’angiogenèse et la croissance tumorales médiées par les signalisations induites par le FT lui-même et impliquant le récepteur PAR-2 et la liaison aux β-intégrines. L’intravasation des cellules tumorales est la première étape de la dissémination tumorale et le FT y joue un rôle facilitant. En utilisant un modèle de souris présentant un phénotype “hyperthrombotique” secondaire à un déficit fonctionnel de la thrombomoduline, l’équipe de N. Mackman et W. Ruf (17) vient d’apporter de nouveaux arguments démontrant le rôle du FT dans les métastases pulmonaires des cancers du sein. Ce modèle leur permet de mettre en évidence 71 Thromboses et hémopathies malignes dossier le rôle majeur de la thrombine, qui favorise le processus métastatique en activant les plaquettes et les récepteurs PAR-1 exprimés par la tumeur et les cellules de l’hôte. asTF, croissance tumorale et angiogenèse tumorale Deux publications très récentes des équipes de H.H. Versteeg, V.Y. Bogdanov et W. Ruf (18), établissent le rôle de l’isoforme asTF dans la croissance et l’angiogenèse tumorales. À partir d’une tumorothèque provenant de 574 patientes atteintes d’un cancer du sein, les auteurs montrent que l’asTF est exprimé par ces tumeurs et que cette expression est corrélée au grade et au stade de la tumeur. En utilisant une construction cellulaire établie dans une lignée MCF-7, ils montrent que l’asTF favorise la prolifération des cellules cancéreuses et l’expression de gènes pro-oncogéniques. L’effet sur la prolifération est dépendant de la liaison de l’asTF avec les β1-intégrines. Le blocage de l’asTF réduit la croissance tumorale, ce qui ouvre des perspectives thérapeutiques. Dans des modèles expérimentaux in vivo et in vitro, ces mêmes équipes ont montré que l’asTF favorise l’angiogenèse, indépendamment de l’expression de PAR-2 (19). Cette observation suggère que le FVIIa de la coagulation n’intervient pas dans cet effet proangiogénique. L’asTF favorise la migration endothéliale et le bourgeonnement vasculaire en se liant aux β1- et β3-intégrines exprimées par l’endothélium, dont ils activent certaines voies de signalisation. Ces effets ne sont pas observés avec le FT dans sa forme transmembranaire intégrale. L’ensemble de ces données est cohérent. Elles identifient l’asTF, dans son interaction avec les β-intégrines, comme cible potentielle d’une thérapeutique antitumorale et antiangiogénique. Le FT cryptique L’expression du FT par une cellule tumorale peut sembler impressionnante, lorsqu’on la compare à celle de monocytes ou de cellules endothéliales perturbées par des activateurs pourtant puissants (LPS ou cocktails cytokiniques). Dans une publication à la méthodologie expérimentale très rigoureuse, l’équipe de L.V. Rao (20) montre que l’expression du FT par une lignée de carcinome mammaire (MDA-231) est comparable à celle de cellules endothéliales (HUVEC), monocytaires (THP-1) ou fibroblastiques (WI-1) sous la forme de monomères de FT de 48 kDA, avec une quasi-absence de formes 72 dimériques. Les auteurs pointent la difficulté de définir l’état cryptique ou décrypté du FT et proposent des méthodes très fines, permettant de définir son état fonctionnel, en mesurant l’activité spécifique du complexe FT-VIIa et l’activité prothrombinase du FT de la surface cellulaire. L’évaluation du FT actif est de l’ordre de 21 % au niveau de la lignée cancéreuse alors qu’il est de 14 % au niveau de la lignée monocytaire mais atteint 64 % au niveau de l’endothélium activé par les cytokines. En cohérence avec ces données comparatives, l’activité spécifique du complexe FT-FVIIa et l’activité prothrombinase du FT membranaire sont moindres, comparativement aux activités spécifiques et prothrombinase des cellules endothéliales et des monocytes. Les auteurs rappellent que la concentration plasmatique de FVII (10 nM) serait suffisante pour se fixer au FT à la surface des cellules, que ce dernier soit ou non sous forme cryptique. Contrairement à l’idée communément admise, le FT exprimé par la tumeur ne serait donc pas constitutivement procoagulant. FT, le nouveau biomarqueur du cancer ? La mesure du FT plasmatique n’est pas réalisée en pratique courante (absence de marquage CE, analyse ne figurant pas dans la nomenclature française des examens de biologie). L’interprétation d’une élévation du FT est par ailleurs délicate et dépendante de la méthodologie utilisée. S’agit-il d’une forme soluble, issue de l’épissage alternatif ou d’une forme soluble et clivée de la forme intégrale ? Le FT exprimé par des microparticules est-il mesuré par ces techniques ? En réponse à un article montrant une association entre le FT porté par des microparticules et la mortalité (mais pas thrombogénicité) chez des patients atteints d’un cancer (21), l’équipe de N. Mackman (22) remet en cause les conclusions de cette étude, en indiquant les difficultés méthodologiques de l’exploration du FT. Il est en effet nécessaire d’utiliser des techniques strictement standardisées de quantification des microparticules ; les méthodes de dosage (ELISA, méthodes fonctionnelles) et les trousses commerciales actuellement disponibles sont de qualité et de spécificité parfois médiocres ou peu spécifiques. La plupart des équipes multidisciplinaires évaluent le risque de thrombose lié à la chimiothérapie en calculant le score prédictif proposé par A.A. Khorana et al. (23). Ce score a été validé de façon indépendante par 6 études cliniques, dont 3 études prospectives. Le calcul du score repose sur des paramètres simples et disponibles : site du cancer, indice de masse corporelle, Correspondances en Onco-Hématologie - Vol. IX - n° 2 - mars-avril 2014 Facteur tissulaire et cancer paramètres de l’hémogramme avant chimiothérapie (plaquettes, leucocytes, hémoglobine) ou utilisation d’érythropoïétine. Différents biomarqueurs pourraient permettre d’affiner ce score : D-dimères, P-sélectine, fragment 1.2 de la prothrombine, FVIII, mesure de la génération de thrombine (24). Le FT soluble est cité parmi ces biomarqueurs mais, compte tenu des réserves émises, il n’est pas encore utilisé comme marqueur prédictif du risque thrombotique chez les patients atteints d’un cancer. Conclusion Le FT joue un rôle déterminant dans la biologie du cancer et dans sa thrombogénicité. Le rôle de l’asTF dans le développement du cancer lui-même est établi par des données expérimentales solides et convaincantes. À côté de son rôle direct dans la biologie du cancer, le FT favorise l’activation des voies de coagulation mettant en jeu des récepteurs PAR spécifiques des différentes sérines protéases de la coagulation. Grâce aux études de signalisation (kinome profiling), les conséquences sur le métabolisme tumoral, l’inflammation, le cycle cellulaire et l’apoptose sont de mieux en mieux connues. L’activation des plaquettes par la thrombine et le dépôt de fibrine favorisent le thrombus et modifient le microenvironnement tumoral. L’occlusion thrombotique du vaisseau, en créant l’hypoxie, déclenche des voies de signalisation pro-angiogéniques, modifiant en permanence le microenvironnement au profit de la prolifération et de l’invasion tumorale. Dans les phénomènes de thrombose liés au cancer, les AVK pourraient s’avérer inefficaces dans la mesure où de faibles concentrations de FVIIa suffisent à saturer le FT exprimé à la surface cellulaire et que des processus indépendants de la voie extrinsèque sont mis en œuvre notamment par le phénomène de NETose. Devant cette complexité d’interactions biologiques, il y a fort à parier que les nouveaux médicaments anticoagulants, ciblant soit le FXa, soit la thrombine, auront des effets très différents, à court terme, sur la coagulation plasmatique et la thrombogénicité, mais également à plus long terme, sur le développement tumoral lui-même. ■ P. Nguyen déclare ne pas avoir de liens d’intérêts. Références 1. Gil-Bernabé AM, Lucotti S, Muschel RJ. Coagulation and 9. Schulz C, Engelmann B, Massberg S. Crossroads of coagu- 17. Yokota N, Zarpellon A, Chakrabarty S et al. Contributions metastasis: what does the experimental literature tell us? Br J Haematol 2013;162(4):433-41. lation and innate immunity: the case of deep vein thrombosis. J Thromb Haemost 2013;11(Supp 1):233-41. of thrombin targets to tissue factor-dependent metastasis in hyperthrombotic mice. J Thromb Haemost 2014;12(1):71-81. 2. Kasthuri RS, Taubman MB, Mackman N. Role of tissue factor 10. Bouchard BA, Gissel MT, Whelihan MF et al. Platelets do not 18. Kocatürk B, Van den Berg YW, Tieken C et al. Alternatively in cancer. J Clin Oncol 2009;27(29):4834-8. express the oxidized or reduced forms of tissue factor. Biochim Biophys Acta 2014;1840(3):1188-93. 3. Morrissey JH, Fakhrai H, Edgington TS. Molecular cloning of the cDNA for tissue factor, the cellular receptor for the initiation of the coagulation protease cascade. Cell 1987;50(1):129-35. 4. Bogdanov VY, Balasubramanian V, Hathcock J et al. Alternatively spliced human tissue factor: a circulating, soluble, thrombogenic protein. Nat Med 2003;9(4):458-62. 5. Versteeg HH, Ruf W. Tissue factor coagulant function is enhanced by protein-disulfide isomerase independent of oxidoreductase activity. J Biol Chem 2007;282(35):25416-24. 6. Lindhout T, Salemink I, Valentin S et al. Tissue factor pathway inhibitor: regulation of its inhibitory activity by phospholipid surfaces. Haemostasis 1996;26(Suppl 4):89-97. 7. Cuccuini W, Poitevin S, Poitevin G et al. Tissue factor upregulation in proinflammatory conditions confers thrombin generation capacity to endothelial colony-forming cells without influencing non coagulant properties in vitro. J Thromb Haemost 2010;8(9):2042-52. 11. Cesarman-Maus G, Braggio E, Lome-Maldonado C et al. Absence of tissue factor is characteristic of lymphoid malignancies of both T- and B-cell origin. Thromb Res 2014;133(4):606-9. 12. Mechiche H, Cornillet-Lefebvre P, Nguyen P. A subpopu- spliced tissue factor promotes breast cancer growth in a β 1 integrin-dependent manner. Proc Natl Acad Sci USA 2013;110(28):11517-22. 19. Van den Berg YW, Van den Hengel LG, Myers HR et al. Alternatively spliced tissue factor induces angiogenesis through integrin ligation. Proc Natl Acad Sci USA 2009;106(46):19497502. lation of human B lymphocytes can express a functional tissue factor in response to phorbol myristate acetate. Thromb Haemost 2005;94(1):146-54. 20. Kothari H, Pendurthi UR, Rao LV. Analysis of tissue factor 13. Yu G, Li H, Wang X et al. MicroRNA-19a targets tissue factor 21. to inhibit colon cancer cells migration and invasion. Mol Cell Biochem 2013;380(1-2):239-47. 14. Eisenreich A, Leppert U. The impact of microRNAs on the regulation of tissue factor biology. Trends Cardiovasc Med 2014;24(3):128-32. 15. Peng W, Yu Y, Li T et al. The effects of small interfering RNA-targeting tissue factor on an in vitro model of neovascularization. Mol Vis 2013;19:1296-303. 8. Demers M, Wagner DD. NETosis: a new factor in tumor 16. Magnus N, Garnier D, Meehan B et al. Tissue factor expres- progression and cancer-associated thrombosis. Semin Thromb Hemost 2014;40(3):277-83. sion provokes escape from tumor dormancy and leads to genomic alterations. Proc Natl Acad Sci USA 2014;111(9):3544-9. Correspondances en Onco-Hématologie - Vol. IX - n° 2 - mars-avril 2014 expression in various cell model systems: cryptic vs. active. J Thromb Haemost 2013;11(7):1353-63. Hernandez C, Orbe J, Roncal C et al. Tissue factor expressed by microparticles is associated with mortality but not with thrombosis in cancer patients. Thromb Haemost 2013;110(3):598-608. 22. Geddings JE, Mackman N. Comment on “tissue factor expressed by microparticles is associated with mortality but not with thrombosis in cancer patients”. Thromb Haemost 2014;111(1):180-1. 23. Khorana AA, Kuderer NM, Culakova E et al. Development and validation of a predictive model for chemotherapy-associated thrombosis. Blood 2008;111(10):4902-07. 24. Pabinger I, Thaler J, Ay C. Biomarkers for prediction of venous thromboembolism in cancer. Blood 2013;122(12):2011-8. 73