1S CH20 TP PILES ET OXYDOREDUCTION bis.pub

PARTIE AGIR CH20 PILES ET OXYDORÉDUCTION
Objectifs : Pratiquer une démarche expérimentale pour réaliser une pile et modéliser son fonctionnement.
Relier la polarité de la pile aux réactions mises en jeu aux électrodes.
Notions : Polarité aux électrodes, réactions aux électrodes. Oxydant réducteur, couple oxydant réducteur, réaction d’oxydo-réduction.
Modèle par transfert d’électrons.
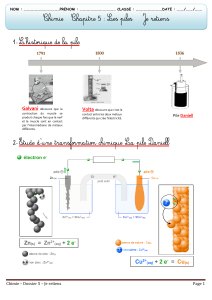
I / PILE DE DANIELL Cuivre-Zinc
Réaliser le montage suivant : dans un bécher A, introduire
50 mL d’une solution de Zinc, (Zn
2+
+SO
4 2-
), de concentration
C=0.10 mol.L
-1
et une plaque de zinc décapée munie d’une pince
crocodile.
Dans un bécher B, introduire 50 mL d’une solution de
Cuivre II, (Cu
2+
+SO
4 2-
), de concentration C=0.10 mol.L
-1
et une pla-
que de cuivre décapée munie d’une pince crocodile.
Plonger un papier filtre imbibée de solution de chlorure de
sodium (pont salin), « à cheval » entre les deux béchers.
Placer un voltmètre entre les deux pinces crocodiles.
1°) Noter la valeur de la tension indiquée par les voltmètre. On la nomme « f.e.m », force électromotrice de
la pile. Ce système est-il un générateur ? Identifier les bornes positives et négatives de la pile.
2°) Remplacer le voltmètre par une résistance branchée en série avec un ampèremètre. Mesurer l’intensité
du courant; que se passe-t-il si vous supprimez le pont salin ? Quel est son rôle ?
3°) Quel est le sens du courant électrique dans l’ampèremètre ? Quels sont les porteurs de charge en mou-
vement dans le circuit extérieur de la pile ? Dans quel sens se déplacent-ils ?
4°) Le sens du courant à l’intérieur de la pile ? Quels sont les porteurs de charge en mouvement dans le cir-
cuit intérieur de la pile ? Dans quel sens se déplacent-ils ?
5°) Considérer le déplacement des électrons dans les parties métalliques de la pile. Que se passe-t-il au ni-
veau de la plaque de Zinc ? Que se passe-t-il au niveau de la plaque de Cuivre ? Proposer une explication.
6°) Relier la polarité de cette pile aux réactions qui se produisent aux électrodes.
7°) Recopier le schéma en indiquant tous les porteurs de charge et leurs sens de déplacement.
II/COUPLE OXYDANT RÉDUCTEUR
On a placé au bureau plusieurs béchers :
l’un contenant une plaque de Fer dans une solution de sulfate de cuivre,
l’autre une plaque de Cuivre dans une solution de sulfate de fer.
Un dernier contenant une plaque de Zinc dans une solution de nitrate d’argent
Observer ce qu’il se passe.
Dans chaque cas écrire les couples oxydant / réducteur mis en jeu
Écrire les demi-équations intervenant entre une espèce et sont « conjugué »
Écrire les équations bilans équilibrées se déroulant dans chaque becher
TP PILES ET OXYDORÉDUCTION
Un couple oxydant-réducteur est formé des deux espèces susceptibles d’échanger des électrons entre elles.
• L’oxydant est l’espèce susceptible de capter un ou plusieurs électrons.
• Le réducteur est l’espèce susceptible de céder des électrons.
• L’oxydant est réduit, le réducteur est oxydé.
• Une réaction d’oxydation correspond à une perte d’électron, une réaction de réduction à un gain d’électrons
• On peut écrire deux demi-équation sous la forme
Ox
1
+ n
1
e
-
= Red
1
Red
2
=Ox
2
+n
2
e
-
Les deux espèces oxydant et réducteurs sont dites « conjuguées » et forment un couple Oxydant/Réducteur
On écrit une équation bilan (en éliminant les électrons)
n
2
Ox
1
+ n
1
Red
2
= n
2
Red
1
+n
1
Ox
2

Matériel :
Par poste :
Solution sulfate de cuivre 0.1 mol.L
-1
Solution sulfate de zinc 0.1 mol.L
-1
Plaque zinc décapée
Plaque de cuivre décapée
Papier filtre imbibée de solution salée de chlorure de sodium
Deux becher
Pinces croccodiles
Multimètre
Résistance 10 Ohms
Au bureau
3 bécher
Plaque cuivre, zinc, fer
Solution nitrate d’argent
Solution sulfate de fer
Solution sulfate de cuivre.
1
/
2
100%