2de DEVOIR DE SCIENCES PHYSIQUES N°3 12 décembre 2008

2de4 CORRECTION DEVOIR DE SCIENCES PHYSIQUES N°3
4 décembre 2009
NOM :
EXERCICE 1 : REFRACTION DE LA LUMIERE (7,5 POINTS, 15 MIN, A/B)
1. a. On appelle la grandeur notée λ longueur d’onde, elle caractérise la couleur de la lumière/radiation
considérée. (A, 1 point)
b. Cocher les bonnes réponses, ou compléter : (A, 2,5 points)
Le rayon laser est : violet vert X rouge
Le laser émet une lumière : X monochromatique polychromatique
La lumière du laser peut être décomposée par un système dispersif : VRAI X FAUX
Donner le nom de deux systèmes dispersifs : un réseau, un prisme, un prisme à vision directe…
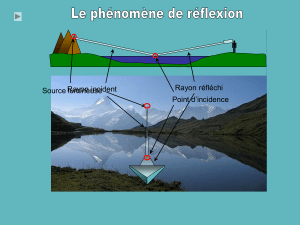
Un rayon laser (λ = 656 nm) se propageant dans l'air rencontre la surface
plane et horizontale d'un bloc de verre dont l'indice de réfraction est n =
1,779 pour cette lumière colorée. L'angle d'incidence est i = 38.0°.
2. Schématiser la situation en utilisant les notations du texte.
(B, 1point)
Il fallait au moins représenter (à la règle) les rayons incidents et réfractés
(sans légende), la normale (sans légende), les angles i et r et le dioptre avec
le nom des deux milieux
(+ l’indice du verre).
3. a. Enoncé de la 1ère loi de la réfraction (ou première loi de Snell-Descartes) : le rayon incident, le rayon
réfracté et la normale au dioptre au point d’incidence sont dans le même plan : le plan d’incidence.. (A, 0,5
point)
b. Relation littérale donnée par la seconde loi de la réfraction dans le cas d’une réfraction air-verre (utiliser
les notations de l’énoncé) : sini = n.sinr (B, 1 point)
Un rayon incident se propage dans l’air et arrive avec un angle i sur le dioptre, alors le rayon réfracté qui se
propage dans le verre est réfracté avec un angle r vérifiant la relation précédente.
4. Calcul de l'angle r que fait le rayon laser dans le verre avec la normale au point d'incidence :
(B, 1,5 points) (Attention, la calculatrice doit être réglée en mode degré, méthodologie)
sinr = sini/n
r = arcsin(sini/n) (remarque : arcsin(x) = sin-1(x) )
A.N. : r = arcsin (sin38,0/1,779)
r = 20,2° (3 chiffres significatifs, comme la donnée qui en comporte le moins)
L’angle de réfraction vaut 20,2°.
EXERCICE 2 : COMPOSITION D’ENTITES CHIMIQUES (7 POINTS, 10/15 MIN, B)
A Je connais
la leçon et ses
définitions
B Je sais
appliquer mon
cours
C Je sais appliquer
et utiliser mes
connaissances
/5
/12,5
/2,5
Exercice 1
Ex. 2
Exercice 3
Exercice 4
1.a
A
1.b
A
2
B
3.a
A
3.b
B
4
B
B
1
A
2
B
3
B
4
C
1
B
2
C
/1
/2.5
/1
/0.5
/1
/1.5
/7
/1
/0.5
/1
/1
/0.5
/1.5

Compléter le tableau sur cette feuille :
Nom de l’entité
Atome d'azote
Ion sodium
Atome de
Brome
Ion
chlorure
Formule chimique
N
Na+
Br
Cl-
Symbole du noyau
N
14
7
Na
........
11
7935Br
.......
35
17
Nombre de protons
7
11
35
17
Nombre de neutrons
7
12
44
18
Nombre de nucléons
14
23
79
35
Nombre d’électrons
7
11 – 1 = 10 (a
perdu un électron
...)
35
17 + 1 = 18 (a
gagné un électron)
Charge électrique
totale
0 Coulomb
+e
0 C
-e
Anion (cocher si c’est
le cas)
x
Cation (cocher si c’est
le cas)
x
EXERCICE 3 : ELEMENT CHIMIQUE (3,5 POINTS, 10 MIN, A/B/C)
1. Par quoi est caractérisé un élément chimique (2 réponses à donner) ? (A, 1 point)
Un élément chimique est caractérisé par son numéro atomique et son symbole.
Les premiers flashs photographiques utilisaient la combustion entre le magnésium Mg et le dioxygène O2 de
l’air. Cette transformation chimique s’accompagne d’une lumière blanche très intense. Il se forme un composé
ionique formé d’ions magnésium II et d’ions oxyde.
2. Quels sont les éléments chimiques présents avant la transformation chimique ?
(B, 0,5 point)
Les éléments chimiques présents avant la transformation chimique sont le magnésium et l’oxygène.
3. Quels sont les éléments chimiques présents après la transformation chimique ? Justifier.
(B, 1 point)
Après la transformation chimique, on retrouve les éléments magnésium et oxygène car il y a conservation
des éléments chimiques lors d’une transformation chimique.
4. Quelles sont les formules des ions formés ? (C, 1 point)
La formule de l’ion magnésium II est Mg2+ et celle de l’ion oxyde est O2- .
EXERCICE 4 : ISOTOPES (2 POINTS, 10 MIN, B/C)
Parmi les atomes suivants :
Li
7
3
C
12
6
Ni
60
28
N
14
7
C
14
6
1. Lesquels sont des isotopes? (B, 0,5 point)
Une expérience a permis de déterminer la masse de l’un de ces atomes, soit 2,0 . 10-26 kg.
2. Quel est cet atome ? Donner votre démarche et le nommer. (C, 1,5 point)
Donnée : m nucléon= 1,67 . 10-27 kg
1.
C
12
6
et
C
14
6
sont des isotopes car les isotopes sont des entités qui ont le même numéro atomique Z mais des
nombres de nucléons différents A.
2. La masse d’un atome est approximativement m = A.mnucléon
Connaissant m et mnucléon, on peut retrouver le nombre de nucléons de l’atome considéré par A = m/ mnucléon
A.N. : A = 2,0 . 10-26/ 1,67 . 10-27 soit A = 12
L’atome considéré est donc le carbone 12.
1
/
2
100%