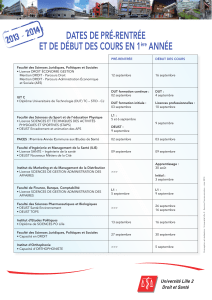
Composition de la Matière

Ch. Bochu
DU
2012
Composition de la
Matière
Ch. Bochu
DEUST SE
2016

Ch. Bochu
DU
2007
Ch. Bochu
DEUST SE
2016
2
Composition de la matière
Solide
Liquide
Gaz

Ch. Bochu
DU
2007
Ch. Bochu
DEUST SE
2016
3
Composition de la matière
Cristal
Electriquement neutre Atome
Electriquement neutre Noyau et
Z Electrons
Z charges négatives
Z charges positives
Nucléons
N Neutrons
Z charges positives
Electriquement neutres
Z Protons
A= Z + N

Ch. Bochu
DU
2007
Ch. Bochu
DEUST SE
2016
4
Composition de l’Univers
Hydrogène
73,97%
Hélium
24,02%
Oxygène
1,04%
Carbone
0,46%
Néon
0,13%
Fer
0,11%
Azote
0,10%
Silicium
0,07%
Magnésium
0,06%
Soufre
0,04%
Le soleil représente 99,86 % de la
masse du système solaire

Ch. Bochu
DU
2007
Ch. Bochu
DEUST SE
2016
5
Composition de la planète Terre
FER
32,1%
Oxygène
30,1%
Silicium
15,1%
Magnésium
13,9%
Soufre 2,9%
Nickel 1,8%
Calcium 1,5%
Aluminium 1,4%
Carbone
traces
Azote
traces
Hydrogène
73,97%
Hélium
24,02%
Oxygène
1,04%
Carbone
0,46%
Néon
0,13%
Fer
0,11%
Azote
0,10%
Silicium
0,07%
Magnésium
0,06%
Soufre
0,04%
118 éléments chimiques
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%