Copie de diaporama mollusques
publicité
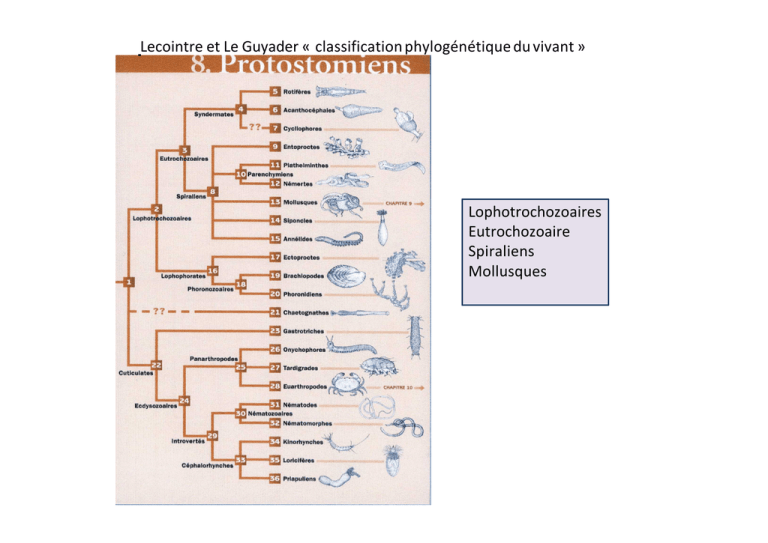
Lecointre et Le Guyader « classification phylogénétique du vivant » Lophotrochozoaires Eutrochozoaire Spiraliens Mollusques Plan d’organisation des Mollusques Tête Radula Manteau = Pallium Repli du tégument Développée chez certains absente chez d’autres Toujours présente à l’exception des bivalves La face externe sécrète la coquille la face interne limite la cavité palléale Fonction de la cavité palléale Organes de la respiration Déboucher des conduits Spicules - Coquille Des plaques : polyplcophores une seule pièce : monoplacophores Gastéropodes Scaphopodes Pied Reptation-enfouissement perforation Fixation aux rochers 1 Mollusques 2 Solénogastres 3 Caudofovéates 4 Eumollusques : coquille /plaques 5 Polyplacophores 8 plaques = chitons 6 Conchifères coquille véritable 7 Monoplacophores, 8 Ganglioneures 10 Gastéropodes & 11Céphalopodes. 12 Diasomes : acéphales 13 Bivalves &14 Scaphopodes, Le principal problème de la phylogénie des mollusques tient à la position de la racine de l’arbre et à l’interprétation de l’anatomie des Solénogastres et caudofoféates, autrefois appelés aplacophores (= absence de coquille). Le phylum est homogène en ce qui concerne l’organisation interne, mais les organes et appareils peuvent être si variés qu’il est impossible de prendre un animal déterminé comme type. Répartition, Ecologie, Ethologie De vastes régions comportant de nombreuses sous-régions ont été définies (Woodward 1856 ; Wallace 1876 ; Fischer 1887) et ces divisions rendent compte de la différenciation des formes terrestres. Artique Atlantico-boérale Aléoutienne Panaméenne Californienne Japonaise Péruvienne Magellanique Patagoninne Caraïbe Atlanto-africaine Atlanto-méditerranéenne Indienne Pacifique Sud-africaine Australienne Transatlantique Exemple de peuplement malacologique en milieu marin – Zone intertidale ou de balancement des marées = Estran rocheux Etage médiolittoral supérieur Les chitons se dissimulent par homochromie avec les rochers mais aussi grâce aux bords inégaux de la coquille couverte d’ épines. De nuit, ils quittent leur abri et vont à la recherche de plantes incrustées sur les rochers. Ils laissent derrière eux une traînée de mucus et utilisent leur odorat pour retrouver leur chemin qui les ramène à leur site préféré. La coquille de chiton composée de huit plaques lui permet de se rouler en boule lorsqu’il est détaché du rocher et part à la dérive. Cela lui permet de supporter les chocs qu’il est amené à subir. Le chiton relève les bords du manteau pour laisser entrer l’eau dans la cavité palléale circulaire où se trouvent jusqu’à 25 branchies. Vu par en dessous, le pied musculaire est entouré d’ une jupe également musculaire formée par le manteau et qui lui permet d’adhérer au rocher Les patelles Prosobranches, Archéogastéropodes. Ce sont des mollusques brouteurs qui raclent le substrat. Les roches convenant pour le repos sont recherchées aussi les patelles forment des colonies abondantes. Dès qu’elle est recouverte par la marée, elle va chercher à manger. Au cours de ses pérégrinations elle s’éloigne parfois d’un mètre de son point d’attache préféré mais elle y retourne dès que la mer commence à se retirer. La patelle n’a pas une durée de vie très longue mais elle a le temps d’éroder la roche sur laquelle elle choisit de rester. La patelle est mature à l’âge de deux ans. Elle est d’abord mâle puis se féminise vers 4 ans. Reproduction fin été début de l’hiver. Troques et gibbules - Prosobrances Archéogastéropodes Gibulla umbilicalis se rencontre sur les rochers des parties hautes et médiane du littoral. Gibulla cineraria (cendré) se trouve à l’étage inférieur du littoral Les archéogastéropodes à coquille spiralée montrent un enroulement régulier. Des spires. Les bords du péristome sont en demi-cercle et la nacre est très apparente. Monodonta lineata est extrêmement abondant dans les parties hautes de l’estran. Le calliostome Calliostoma zyzyphinum vit sur les substrats rocheux, dans parties les plus basses d e l’estran jusqu’à 300 de profondeur. Il se nourrit d’algues. Helcion (patellidae )= archéogastéropodes ) est une petite patelle qui vit uniquement sur les stipes de laminaires à l’étage infralittoral jusqu’à 30 m de profondeur car il craint la dessiccation. Sa coquille translucide est parcourue de raies bleues discontinues. Au cours de sa croissance, elle migre de la fronde vers la tige de laminaire, où elle creuse une empreinte profonde. Littorines, gastéropodes prosobranches, mésogastéropdes Chaque espèce de littorine peuple une zone marégraphique précise. Chacune adopte la stratégie de reproduction la mieux adaptée à son niveau d’exposition selon l’étage de la zone intertidale qu’elle occupe. Elles s’alimentent en raclant les surfaces dures, en sortant la radula pour brouter les microorganismes. Les aliments favoris sont les algues unicellulaires et les bactéries mais aussi les débris organiques et les détritus qui se trouvent sur les fonds marins. Elles exploitent différentes ressources alimentaires et ont adopté divers modes de reproduction. A telle enseigne qu’elles ne sont pas en concurrence directe. Les littorines se déplacent comme les autres gastéropodes au moyen d’un pied musculeux glissant sur une traînée de mucus. L’animal n’est pas emporté par les vagues car son pied exerce une forte adhérence sur l’algue. Littorina saxatilis peut montrer d’étonnantes variations de couleurs au même endroit.. Pour des animaux qui semblent sédentaires, ils peuvent parcourir quotidiennement des distances considérables. La littorine obtuse Littorina obtusata montre un polymorphisme chromatique, les plus communes étant jaunes et brun orangé. Le bigorneau, Littorina littorea peut mesurer jusqu’à 2cm. Son opercule est bordé de blanc Les coquilles de littorines, très robustes sans nacre apparente. L’enroulement est irrégulier , le dernier tour de spire étant très grand et globuleux. Les grains de café appartiennent à la famille des porcelaines. Ce sont des Mésogastéropodes (1 cm) qui se rencontrent parmi les algues sur les côtes rocheuses, à partir des niveaux les plus bas (infralittoral). Le péristome est en forme de fente . Deux espèces vivent sur nos côtes, Trivia artica à la coquille toute blanche, et Trivia monaca dont la coquille est ornée de trois petites taches sombres. Le grain de café est considéré comme un brouteur mais ce sont les ascidies qui constituent l’essentiel de son alimentation. Il les perfore et en aspire le contenu. . Etage médiolittoral moyen et inférieur Le pourpre Nucella lapilus (Thais l.) ou bigorneau perceur néogastéropode Il est abondant en étage médiolittoral moyen à inférieur, là où se trouve la moulière. Sa coquille est variable avec un siphon court et droit . Le rocher ou cormaillot Ocenabra erinacea vit aux étages infralittoral et circalittoral. Le buccin, Buccinum undatum peut mesurer jusqu’à 8 cm. Sa coquille est fotement cannelée. Il est commun sur les fonds marins plutôt vaseux ou sablonneux au large. Les prosobranches néogastéropodes ont une coquille siphonostome. Ils sont prédateurs ou nécrophages. Prédateurs, les pourpres et les cormaillots se nourrissent principalement de moules et de balanes dont ils forent la coquille grâce à une sécrétion acide d’une glande buccale. La coquille fragilisée de la proie est ensuite percée par la radula. Gastéropodes Opisthobranches (branchies en arrière du cœur) Strictement marins, ces gastéropodes sont en général dépourvus de coquille ou bien cette dernière est présente sous forme résiduelle. Ils ont deux paire de tentacules : dorsaux, ce sont les rhinophores olfactifs et les tentacules situés près de la bouche sont tactiles. Ils sont hermaphrodites. La majorité des opisthobranches mange des polypes, des bryozoaires. Cette sous-classe comporte plusieurs ordres, selon la présence ou non d’une coquille sous le manteau, la présence ou non de cavité palléale et de branchies. Limaces de mer : ce terme est un nom vernaculaire désignant des mollusques sans coquille, ni cavité palléale, appartenant aux Nudibranches. Les doris et les éolis sont assez fréquents sur la côte. Le lièvre de mer, l’aplysie Aplysia punctata, est un opisthobranche ayant une coquille réduite recouverte par le manteau et des branchies Aplysie : vue dorsale rhinophore Orifice génital Couronne de branchies anus Coquille transparente 2 lobes parapodiaux anus pied Doris éolis Papilles dorsales = cérates Bivalves Ostreides et Pectinides : Filibranche Ptériomorphia à charnière dysodonte Seul persiste le muscle adducteur postérieur = monomyaire qui est très puissant Les ostreidés ont une coquille irrégulière, à valve gauche bombée, fixée sur les rochers. Les huîtres sont hermaphrodites successivement mâles puis femelles. Les larves ciliées éclosent dans la cavité palléale. Chez l’huître plate, Ostrea edulis ou Belon, le sexe peut changer au cours d’un même été alors que chez l’huître creuse Crassostrea gigas, (japonnaise) le sexe change d’une année sur l’autre. Pétoncle et clamys 2 valves bombées Peigne operculé Aequipecten opercularis Clamys varia Les pétoncles ont un byssus et vivent fixés tout en pouvant rompre chimiquement leur attache Une valve plate, une valve bombée Genre Pecten coquille ST Jacques Les Pectinidae ont une charnière dysodonte, munie d’excroissances ou auricules et une coquille pourvue de stries rayonnantes. Les pecten sont posés sur le fond par la valve droite, très bombée. Ils se propulsent vers l’arrière en rabattant la valve gauche aplatie et en expulsant de l’eau de la cavité palléale. En relation avec leur vie libre, de nombreux tentacules sensoriels bordent le manteau ouvert, dont certains sont photosensibles (yeux). Surplomb rocheux en milieu marin 1 Littorina neritoides 2 Patella sp 3 Ormeau, Haliotis tuberculata 4 fissurelle 5 polyplacophores 6 Monodonta lineata 7 Pisania sp 8 Myoidae pholade 9 Lithophage Lithophaga 10 Ostrea 11 Polyplacophore 12 Nudibranche 13 Muricidae Cormaillot 14 Cerithium Espèce pélagique Espèces foreuses Plaques calcaires sur la charnière Muscle adducteur antérieur Janthina avec son flotteur et ses coques ovigères Plaques calcaires Un lamellibranche perforant le taret Teredo navalis creuse le bois immergé à l’aide des bords tranchants de la coquille. La plus grande partie du corps est formée par les siphons enfermés dans un tube calcaire qui tapisse la cavité creusée par le bivalve. Coquille 20 mm , siphons 600 mm. Cuilleron ligamentaire siphons Muscle adducteur antérieur Tube calcaire Sinus palléal Valve de la coquille Pied Masse viscérale Coquille de pholade : vue dorsale et vue interne de la valve gauche La pholade peuple les fonds rocheux. C’est une espèce perforante qui creuse une galerie dans divers matériaux, surtout des roches calcaires. Elle vit dans un trou qu’elle ne quitte jamais et ce sont ses siphons qui assurent la relation avec l’extérieur. Le pied semble être l’organe essentiel de l’érosion, mais les valves travaillent aussi par un mouvement rotatif . Elle avance de (qq mm /mois). Adaptations à l’anoxie = manque d’oxygène marée basse = phase de résistance nécessitant des mécanismes biochimiques pour survivre en anaérobiose. Les différentes espèces manifestent un étagement bathimétrique précis qui dépend de leurs possibilités de survivre à marée basse pendant un temps plus ou moins long. La plupart d’entre eux cessent toute activité en s’isolant dans leur coquille hermétiquement close - fermeture des valves chez les bivalves -ajustement des bords de la coquille aux irrégularités du substrat chez les Patellidés - présence d’un opercule chez les gastéropodes prosobranches : tous disposent d’un opercule corné ou calcifié fixé sur la partie postérieure du pied et grâce auquel l’animal peut clore sa cavité palléale durant l’exondation et y maintenir une petite quantité d’eau. In Turquier : les animaux dans leur milieu Répartition bathymétrique des Littorinidés et des Trochidés dans la zone intertidal des côtes de la Manche . BM & PM : niveaux de la basse mer et de la pleine mer ; VE & ME : marées de vive-eau ou de morte-eau, moyennes (moy) ou exceptionnelles (exc) Littorina neritoides Littorina saxatilis Littorina littoralis Monodonta lineata Gibbula penenti Littorina litorea Gibbula umbilicalis Gibbula cineraria Gibbula magus (substrat meuble) Adaptations à l’anoxie = manque d’oxygène Etagement bathimétrique des trochidés, littorinidés, et néritidés Mécanismes biochimiques Une exception a été remarquée à propos des littorines qui conservent partiellement leur activité à marée basse et dont la consommation d’oxygène, même au repos, est plus grande pendant l’exondation que pendant la phase aquatique. Pour couvrir leur dépense énergétique en anaérobiose, les mollusques stockent une quantité importante de substrats fermentescibles dans leurs tissus, principalement dans les muscles : glycogène, acide aspartique, etc. L’accumulation d’acide lactique devient rapidement un facteur limitant de la survie. Ces invertébrés marins présentent une grande résistance à l’anoxie car ils n’accumulent pas d’acide lactique et disposent de mécanismes enzymatiques qui court-circuitent le cycle de Krebs. La caractéristique étonnante de tous les animaux intertidaux est leur récupération métabolique dès le retour de la mer. Mais même si l’animal dispose d’une eau bien oxygénée, il récupère conjointement par un mécanisme aérobie et anaérobie pendant au moins trois heures. Exemple de peuplement malacologique en milieu marin – Zone de balancement des marées = Estran - Substrat meuble 1 Nassarius reticulata 2 Dentalium (Scaphopode) 3 Cerastoderma edula 4 Solen 5 Macoma balthica 6 Mya arenaria 7 Turritelle comunis 8 Acteon tornatilis 9 Telline 10 Alvania cimex 11 Apporrhais pespelicanis 12 Arca noae 13 Capulus hungaricus 14 gourmya vulgata Milieu meuble La nasse Nassa reticulata Prosobranche Néogastéropode. C’est un animal nécrophage qui se tient à l’affut dans le sédiment ou entre les rochers de l’infralittoral . Grâce à un siphon la nasse est en contact avec l’extérieur ; elle repère les cadavres car elle a un sens olfactif très développé. Les pontes sont souvent alignées sur les tiges de phanérogame marine Zostera marina La crépidule Crepidula fornicata (Prosobranche Mésogastéropode). Originaire d’ Amérique du nord, de la côte atlantique, elle a été introduite en Angleterre avec un naissain d’huîtres (1880) et elle est bien établies sur nos côtes . Elle a une coquille qui évoque un chausson (crepidula en latin), la cloison ventrale étant le septum ; fornix = voute évoquant le forme bombée de la coquille. Elles vivent en petites chaînes sous forme d’arche, les plus anciennes supportant jusqu’à douze congénères entassées l’une sur l’autre. Comme elles sont microphages et extraient leur nourriture de l’eau, elle n’ont pas besoin de se déplacer. C’est une espèce hermaphrodite protandre, chaque individu étant d’abord mâle avant de devenir femelle pour le reste de sa vie. Comme elles vivent empilées, les individus âgés femelle sont en bas de la colonie et les mâles en haut. L’individu qui sert de support devient femelle alors que le suivant restera mâle aussi longtemps qu’aucun nouveau venu ne se place sur sa coquille. Prosobranche Archéogastéropode La troque mage Gibbula magus et la natice Polinices catenus sont de grandes espèces (30 mm) avec un ombilic très marqué. Les natices sont des prédateurs qui dévorent les bivalves dans le sable. Stries concentriques saillantes et protubérances verruqueuses caractéristique de la praire Siphon inhalant Siphon exhalant Dentale Scaphopode Pied fouisseur Les palourdes Venerupis Eulamellibranches, hétérodontes, (sinupalliées) vivent dans des sédiments fins où elles peuvent s’enfouir jusqu’à 10 cm, laissant les siphons affleurer en surface (coquille sinupalliée). La praire Venus verrucosa, appartenant comme les palourdes aux Vénéridés vit dans des sables grossiers. Cerastoderma edule est comestible . Elle vit dans les sédiments sablo-vaseux du médiolittoral et affectionne les estrans découverts à marée basse. Plusieurs espèces de bucardes colonisent l’estran supportant des sables grossiers (gravier) et tolérant des niveaux de salinité variables : la bucarde à papilles A. echinata, la bucarde tuberculée A tuberculata, la bucarde épineuse A. aculeata. Les coquilles des coques sont robustes, cannelées et quasi sphériques. La charnière est de type hétérodonte (eulamellibranches), mais les coques étant des endogés superficiels, les siphons courts qui ferment le manteau postérieurement ne laissent pas une empreinte du sinus = coquille intégripalliée. Substrat meuble Enfouissement du couteau Le couteau s’encre ferment dans le sol à l’aide de son pied Le pied pousse vers le bas Lorsqu’il est arrivé à une assez grande profondeur, le pied s’élargit en adhérant au sable Ce processus est répété jusqu’à ce que le couteau soit tout entier à l’abri dans le sable Les couteaux ont tous en commun des valves étroites, fines et coupantes (razor shell). Les courts siphons affleurent en surface , l’extrémité antérieure étant enfoncée dans le sable. Le pied est particulièrement développé et puissant. Les siphons très longs et contractiles de la mie des sables Mya arenaria (Myoïdea) , sont enveloppés d’une tunique. La coquille est bâillante . La charnière dite desmodonte est très particulière : le ligament a migré à l’intérieur sur un cuilleron porté par la valve gauche et qui est perpendiculaire à la valve droite. Les lutraires (Mactridae), de plus grande taille (10 cm) et à la coquille plus épaisse, ont le même type de charnière mais les cuillerons sont portés par les deux valves et leur sont parallèles. Ce sont des fouisseurs profonds, s’enfonçant jusqu’à 40 cm. Vers et bivalves fouisseurs ont des prédateurs. Les échassiers ont développé des becs différents qui leur permettent de se partager les mêmes sites sans pour autant dépendre de la même nourriture. Les échassiers fouillent le sable . Les huitriers presque inféodés au domaine littoral, fracassent les bivalves et écarte les valves. Les oiseaux débusquent les mollusques et les vers en utilisant leur bec comme un levier. Courlis barge huitrier pie chevalier Coque gambette bécasseau Coque et spissule palourde Les plages de sable ne gèlent pas et surtout en hiver, les échassiers nordiques visitent l’estran . Les oiseaux attendent la marée basse pour fouiller le sable et chercher les proies enfouies arénicole gravelot Exemple de peuplement malacologique en milieu terrestre en eau douce 1 Oxychilus draparnaudi 2 Clausilia 3 Cepaea nemoralis & Cepaea hortensis 4 Helicigona lapicida 5 Pomatias elegans (Prosobranche) 6 Caecilioides 7 Paladilia helvetica 8 Pisidium sp 9 Pupilla 10 Cochlostoma (Prosobranche) 11Fructicicola 12 Bythinia hydrobiidae 13 Valvata piscinalis 14 Succinea 15 Physe 16 Radix auricularia 17 Stagnicola palustris 18 Planorbe 19 Viviparus sp paludine 20 Anodonte 21 Unio sp Le poumon des gastéropodes terrestres L’affranchissement définitif du milieu aquatique en tant que milieu de vie a été réalisé efficacement par les gastéropodes Pulmonés. Les gastéropodes sont de tous les mollusques, les seuls qui aient acquis la respiration aérienne leur donnant accès à l’habitat terricole : Pulmonés Stylommatophores. Mais ils ont des représentants inféodés au milieu aquatique, les Pulmonés Basommatophores. Les structures respiratoires de ces animaux peuvent être considérés comme des innovations évolutives (néoformation) ayant permis d’utiliser l’oxygène atmosphérique tout en limitant les pertes d’eau au niveau des échangeurs respiratoires. Classiquement, le poumons des gastéropodes terrestres est considéré comme l’homologue d’une cavité palléale transformée pour capter l’oxygène atmosphérique. C’est effectivement le cas chez les rares Prosobranches continentaux (Cyclostomidés). Chez les Pulmonés en revanche, le poumon se forme par invagination de l’épiderme, indépendamment de la cavité palléale qui régresse au cours de la vie embryonnaire. Le poumon communique avec l’extérieur par un pneumostome. Sa paroi dorsale est richement vascularisée. La circulation sanguine n’est pas modifiée au niveau du poumon : le sang oxygéné gagne directement le cœur. Une ventilation simple existe chez les pulmonés Stylommatophores. Le poumon des gastéropodes terrestres retournés à l’eau Ils ont les problèmes respiratoires liés au « retour à l’eau ». Leur besoin majeur est celui de la couverture de leurs besoins au cours de la plongée. La plupart des Basommatophores conservent une respiration pulmonaire et viennent régulièrement en surface pour remplir leur poumon : limnées planorbes, physes. La persistance chez les Basommatophores, d’organe de la respiration aérienne pratiquement identiques à ceux des espèces continentales (poumons) amène à considérer leur vie aquatique comme un phénomène secondaire évolutivement parlant. Les ajustement de l’appareil respiratoire ne remettent pas en cause la structure fondamentale ni les mécanismes qui assurent son fonctionnement. Cette interprétation est concrétisée par l’expression « retour à l’eau » utilisée pour ces animaux. Les Basommatophores ont conservé une respiration tégumentaire qui constitue sans doute un apport important à la respiration : les capacités d’apnée des limnées sont importantes car elles peuvent rester 2 à 3 jours immergées dans des eaux oxygénées. « Les poumons d’eau » Quelques espèces disposent de structures d’appoint de la respiration pulmonaires : papilles dorsales des lobes palléaux. Chez quelques familles, le retour à l’eau est plus poussé dans ce sens que les animaux sont capables de vivre uniquement en consommant l’O2 dissout. Le poumon est alors reconverti en organe de la respiration aquatique sans modification de l’épithélium. Pour augmenter la surface d’échanges en raison de la faible concentration de l’O2 dans l’eau, il y a des diverticules tégumentaires autour du pneumostome. Ce sont des branchies extrapalléales observées chez les Bullinus par exemple. Des branchies néoformées se développent à l’intérieure de la cavité pulmonaire chez les Ancylidés Domaine terrestre Les milieux terrestres abritant des mollusques sont ceux qui possèdent une bonne stabilité climatique incluant un minimum d’humidité. Bois, forêts, fourrés, haies, anfractuosités, rochers, grottes, sont de bons sites. Divers groupes restent très liés à des milieux extrêmement humides et semblent finalement apparaître comme des amphibies : ce sont les genres Zonitoides, Monacha, Vertigo. Les collines et les dunes littorales offrent par leur végétation des abris aux Helicella et Theba et un abri dans leurs racines aux Pomatia elegans. Les genres Helix et Arianta sont caractéristiques des milieux assez humides, qu’ils soient naturels ou cultivés, qu’il s’agissent de forêt de champs ou de potagers, de jardins. Les Acanthinula, Hygromia sont absolument ennemis de tels milieux ou de tous autres milieux humanisés. Les lieux rudéraux hébergent Pupilla qui se rencontre sur des ruines, des pierres. Il existe des escargots anthropophiles qui se sont parfaitement adaptés à l’activité agricole de l’homme et qui ont entrepris le tour du monde à sa suite : Cornu (Helix) aspersum, Oxychilus draparnaudi et Hygromia striolata Domaine aquatique terrestre Les gastéropodes sont des pulmonés qui continuent d’utiliser l’oxygène atmosphérique et doivent se réapprovisionner régulièrement en surface. Ils ont les problèmes respiratoires liés au « retour à l’eau ». Leur besoin majeur est celui de la couverture de leurs besoins au cours de la plongée. Le milieu idéal pour les mollusques d’eau douce est réalisé par les eaux calcaires, à vitesse d’écoulement modérée, riches en végétation et sans nuisance due à une quelconque activité humaine. C’est la teneur en calcium qui est déterminante : eau dure ou eau douce au sens strict. Les eaux « douces » se rencontrent en montagne où l’on trouve Pisidia et Lymnaea peregra. Les eaux calcaires possèdent de façon générale des représentants des limnées (L. palustris, L. truncatula, L. stagnalis), des planorbes et des Sphaerium. Les espèces les plus volumineuses se trouvent dans les grandes étendues d’eau stable tandis que les petites étendues sujettes à assèchement contiennent des petites espèces. Les canaux sont préférés par les physes, Bythinella et Vivipares et Dreissena (moule) Les eaux lacustres, fluviales ou stagnantes abritent des anodontes et des unios (bivalves). Régulation hydrique. hiver en hibernation - été en estivation, C’est-à-dire en léthargie, dans le sol, la vase, les anfractuosités. C’est principalement par leur comportement que les gastéropodes terrestres régulent leur bilan hydrique ce qui leur permet d’être présents absolument partout. Orifice génital oeil tentacule oeufs Ponte de l’escargot pneumostome Pulmonés Stylommatophores Terrestres 2 paires de tentacules yeux au bout des tentacules dorsaux Basommatophores aquatiques 1 paire de tentacules yeux à la base des tentacules Limnée Pulmonés basommatophores planorbe physe Milieux caractéristiques - Dunes littorales En étroite interaction avec la plage, les avant-dunes sont les premières formations terrestres. Les pelouses à chiendent qui résistent bien au sel marin, les oyats et tout le cortège de plantes psammophiles, sont colonisés par des escargots L’escargot des dunes englobe plusieurs espèces dont la plus fréquente Theba pisana vit sur le littoral Atlantique. Il est de couleur généralement blanche. Afin de résister aux températures élevées régnant dans ces milieux arides, il a développé des stratégies d’adaptation. Dès les premières chaleurs, il grimpe sur différents supports pour fuir le sol brûlant. Il forme alors des grappes de centaines d’individus. Une fois en place, il sécrètent un épiphragme formé de mucus séché afin de conserver un peu d’humidité. Il se nourrit de plantes. Theba pisana Comme l’espèce précédent, Cochlicella acuta se rencontre au sommet des tiges de plantes dans les lieux secs et ensoleillés. Succès invasif de l’escargot petit gris Cornu aspersum L’escargotpetit gris Cornu aspersum est représenté par plusieurs races génétiquement déterminée. Seule la lignée orientale est considéreé comme invasive en Amérique, Austarlie, Océanie où elle a été introduite vers le 16 eme siècle. En Californie où elle a été introduite en 1850, elle a été reconnue en 1931 comme une espèce ravageuse (a pest). Son aptitude à coloniser toujours de nouvelles aires géographiques tient à la variation phénotypique de ses traits de vie : trade-offs poids & nombre d’oeufs pondus ; sa résiatnce aux ennemis naturels. Les multiples introductions simultanées ont entraîné une rapide expansion à travers le monde. California (1856) Hawai Utah Maine (1839) Massachussets (Irland) Texas New Orleans (Spain) (1952) Haiti Spanish colonization (16th BC) ¡ Chile légende 1 population ¡ 2 populations Spanish colonization (16th BC) Uruguay South Africa (1650 ? 1850) Reunion Indian Company (17th BC) Australia (1879) New Caledonia (1879) New Zealand 3 populations Distribution area of the landsnail Cornu aspersum. In green: origin center of the species and primary introduction areas (Tertiary and Quaternary periods). In pink: spatial localization of sampling populations of secondary introduction areas (last millennium) analysed for phylogeohraphic and population genetics purposes. Blue arrows indicate the suspected origin of some alien populations. Added information on putative date of first introduction are also reported into brackets (Reichling, 1950; Madec, 1989; Guiller et al., 1994; Sherley, 2000; Guiller and Madec, 2009) (Guiller). Cornu aspersum Population introduite Californie Population native des îles Baléares dans son aire d’origine, l’escargot n’est pas un fléau A B Comparison between introduced (A) and native (B) populations of the land mollusc Cornu aspersum. The trunk of citrus trees are full of snails in Californian orchards only (http://edis.ifas.ufl.edu), where the species is a regulated pest. By contrast, the species is not invasive in its native range (citrus trees in Balearic islands, photo by L. Madec). Biological control: the predation of one C. aspersum snail by several Rumina decollata individuals (http://www.goodsnails.com/index.htm). Arion lusitanicus : menace pour la biodiversité indigène Arion rufus limace rouge La limace tueuse, dont le nom scientifique est Arion lusitanicus, est originaire de la péninsule ibérique. La limace tueuse a commencé à se répandre en Europe il y a environ 30 ans, par le biais d’œufs présents dans la terre de plantes en pots. Cette voie de propagation demeure d’ailleurs une source d’infestation majeure à l’heure actuelle. Elle est une menace pour la biodiversité indigène. Elle colonie toute l’Europe, résiste aux mesures d’éradication ; elle tue et mange les autres espèces de limaces manteau pied Anus pneumostome orifice génital L’escargot de Quimper, Elona quimperiana : une espèce protégée Sauvegarde de la biodiversité Elle est protégée depuis 1979 par la France et depuis 1992 par la Directive habitats de l’Union européenne. L’escargot de Quimper (Elona quimperiana) a une aire de répartition large mais fragmentée : une partie ouest de la Bretagne et une partie du pays basque pour la France, puis en Galice, au Pays basque espagnol, et dans les Monts Cantabriques pour l’Espagne. Aplatissement de la coquille avec un ombilic très ouvert ; le rebord de la coquille est clair. L’escargot de Quimper a une préférence pour les milieux boisés, humides et ombragés. Il mange de tout : il est à la fois carnivore, coprophage (excréments), détritivore et nécrophage (cadavres d’animaux). Ses prédateurs : le hérisson, la grive musicienne, le crapaud commun, les carabes.