Le savon : sa fabrication (= saponification) et son mode d`action

p. 1
SITIENS MENS
"Esprit désireux de comprendre"
LE SAVON : SA FABRICATION (= SAPONIFICATION) ET SON MODE
D'ACTION.
"Terre
Marie-Christine & Jean-François Misonne
Lyrique"
gelura@proximus.be
www.gelura.com
Table des matières
1. Rappel mnémotechnique!
2. Rappel de nomenclature chimique!
2.1. Alcanes (uniquement atomes C et H)!
2.2. Alcool (substitution H par OH)!
2.3. Acide gras (substitution H par COOH)!
2.4. Estérification (Substitution ("estérification") -OH par -O-CO-R =
acide gras)!
3. Principe de saponification!
4. Savon dur ou savon mou ?!
5. D'où viennent le sodium ou le potassium dans les
cendres ?!
5.1. Sodium : cendres de plantes maritimes!
5.2. Potassium : cendres de bois de cheminée p.ex.!
6. Mode d'action du savon!
7. Bibliographie!
* * *
Abréviations & lexique
°ANGL. Étymologie anglaise (anglais "traduction").
°AR. Étymologie arabe (!"#"#$%# 'prononciation'
"traduction").
°ÉG. Étymologie égyptienne (égyptine "traduction").
°ENGL. = °Angl.
°GR. Étymologie grecque (προνον 'prononciation' "traduction")
°IT. Étymologie italienne (italien "traduction").
°LAT. Étymologie latine (latin "traduction").
⋲ "issu de…"
18ES. 18ième siècle.
1AMAF Amaranthaceae (famille botanique).
1CAFO Caryophyllales (ordre botanique).
1ZYGF Zygophyllaceae (famille botanique).
1ZYGO Zygophyllales (ordre botanique).
ALKALI (°Lat. alkali < °Ar. &'('% 'āl-qily' "la cendre" (sous-
entendu : cendre de plante à soude)). Al °Ar. '% 'al' "la". Kali
°Ar. &'( 'qili' "cendre"
AMPHILYOPHILE (AMPHIPHILE, AMPHIPATHIQUE, AMPHIPOLAIRE) Espèce
chimique (molécule ou ion) possédant à la fois un groupe
hydrophile et un groupe hydrophobe.
BPSADM : Biotique Plante Spermatophyte Angiosperme
Dicotylée (vraies) Moyenne.
ESTER n.m. Groupement chimique formé d'un atome lié
simultanément à un atome d'oxygène et à un groupement
alkoxy (R-O-) du type R-COO-R'. Quand cet atome est un
atome de carbone, on parle d'esters carboxyliques.
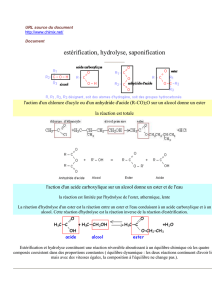
ESTÉRIFICATION n.f. Réaction chimique au cours de laquelle un
groupe fonctionnel ester -COOR est obtenu par condensation
d'un groupe acide carboxylique (-COOH) et d'un groupe alcool
(-OH).
GLYCÉRIDE (= acylglycérol = glycérolipide). Ester d'acide gras et
de glycérol. Majoritairement présent dans le tissu adipeux (90
%) et faisant partie des lipides. Ex. CH3-CH2-CH2-O-COR.
GLYCÉROL (= glycérine). Composé chimique de formule CH2OH–
CHOH–CH2OH. Dérivé du propane CH3-CH2-CH3 où trois
hydrogènes ont été remplacés par trois hydroxyles,
correspondant à trois fonctions alcool.
HALOGÈNE adj. et n.m. (°Gr. αλος 'halos' "sel" + γενναω 'gennao'
"engendrer"). Élément "qui engendre du sel", figurant dans la
colonne VII A du tableau périodique de Mendeleïev : fluor,
chlore, brome, iode et astate.
HALOPHYTE ou HALOPHILE adj. et n.f. (°Gr. αλος 'halos' "sel" +
φυτον 'phyton' "plante" ou φιλος 'philos' "ami"). Plante vivant
dans des eaux ou sur des sols salés.
HYDROLYSE n.f. (°Gr υδρο 'hydro' "eau" + λυειν 'luein' "briser").
Réaction chimique dans laquelle une liaison covalente est
rompue par action d'une molécule d'eau. Ex. de hydrolyse
d'un ester : Ester + Eau ! Alcool + Acide carboxylique (R1-
COO-R2 + H2O ! R2-OH + R1-COOH. La réaction inverse est
l'estérification.
KALIUM (°Ar. &'( 'qili' "cendre"). Nom néerlandais et anglais de
la potasse.
LIAISON COVALENTE n.f. Liaison chimique dans laquelle deux
atomes partagent deux électrons d'une de leurs couches
externes afin de former un doublet d'électrons liant les deux
atomes. Ex. NaCl.
LIXIVIATION n.f. Précipitation des particules solides non solubles.
MACÉRATION n.m. Procédé consistant à laisser séjourner un
solide dans un liquide froid pour en extraire les composés
solubles.
MICELLE n.f. (°Lat. mica "parcelle'). Agrégat sphéroïdal de
molécules possédant une tête polaire hydrophile dirigée vers
le solvant et une chaîne hydrophobe dirigée vers l'intérieur.
Une micelle mesure entre 0,001 et 0,3 µ.
NATRIUM (°Ég. Wadi El Natroun = Vallée du Natron dans le
désert de Nitrie en Égypte où il existait des lacs d'où les
Égyptiens tiraient, après purification ou asséchement, le
natron = carbonate de soude Na2CO3). Nom néerlandais et
anglais du sodium.
POTASSE CAUSTIQUE n.f. KOH.
SAUMÂTRE. Dont le goût est celui de l'eau de mer mêlée d'eau
douce.
SODIUM n.m. (°Angl. soda "soude" + suffixe d'élément métallique
"ium").
SOUDE CAUSTIQUE n.f. NaOH
SOUDE [Version1] n.f. (°Angl. soda "soude" ⋲°It. soda ⋲°Ar. !"ّﻮﺳ
'suwayd' ou 'suwwad' ⋲ mot de la racine s-w-d "noir" (des
cendres) = "salicorne", plante dont les cendres sont riches en
soude et qui étaient utilisées pour combattre la migraine.
SOUDE [Version2] n.f. (°Angl. soda "soude" ⋲°Ar. suda 'mal de tête')
Parce que le carbonate de sodium, produit à partir des
cendres de la plante appelée 'suwwad' en arabe, à savoir la
saloicorne, servait de remède traditionnel aux maux de tête.
TRIGLYCÉRIDE (= triacylglycérol = triacylglycéride = TAG).
Glycéride dans lequel les trois groupes hydroxyle du glycérol
sont estérifiés par des acides gras. Constituant principal des
graisses animales et de l'huile végétale. CH2-O-COR-CH-O-
COR-CH2-O-COR.
µ micromètre = 0,001 mm.
* * *
1.Rappel mnémotechnique
Acide + Base ! Sel + Eau
(ex. HCl + NaOH ! NaCl + H2O)
Acide gras + Base ! Savon + Alcool/Eau
(ex. CH3-(CH2)n-COOH + NaOH ! CH3-(CH2)n-COONa
+ H2O).
2.Rappel de nomenclature chimique
2.1.Alcanes (uniquement atomes C et H)

p. 2
CH4 Méthane, CH3-CH3 Éthane, CH3-CH2-CH3
Propane, CH3-(CH2)2-CH3 Butane.
2.2.Alcool (substitution H par OH)
CH3OH Méthanol, CH3-CH2OH Éthanol,
CH3-CH2-CH2OH Propanol* = propane-1-ol,
CH3-(CH2)2-CH2OH Butanol.
*Cas particulier :
Propane-1,2,3-triol = Glycérol = Glycérine :
CH2OH
⎢
CHOH
⎢
CH2OH
Liquide incolore visqueux et inodore au goût sucré.
Il constitue l'articulation centrale de tous les lipides
de la classe des triglycérides.
2.3.Acide gras (substitution H par COOH)
CH3COOH Acide méthanecarboxylique (= acide
acétique = acide éthanoïque), CH3-CH2COOH Acide
éthanecarboxylique (= acide propanoïque),
CH3-CH2-CH2COOH Acide propanecarboxylique,
CH3-(CH2)2-CH2COOH Acide butanecarboxylique.
2.4.Estérification (Substitution ("estérification") -OH
par -O-CO-R = acide gras)
Ester = Monoglycéride :
CH2OH
⎢
CHOH
⎢
CH2-O-CO-R
Ester = Triglycéride (R peut être R1, R2, R3) :
CH2-O-CO-R
⎢
CHO-O-CO-R
⎢
CH2-O-CO-R
Triglycéride = glycéride dans lequel les trois groupes
OH du glycérol sont estérifiés par des acides gras.
Ils sont le constituant principal des graisses animales
et de l'huile végétale.
3.Principe de saponification
Au 18eS., les ménagères faisaient leurs lessives en
"générant" du savon – sans le savoir - en mélangeant
des graisses avec du sel de potasse obtenu par
macération et lixiviation de cendres végétales par
l'eau.
Quant à la solution alcaline, elle pouvait être
chauffée afin d'obtenir un produit sec, dénommé
"alcali" (cendre), constitué principalement de K2CO3
(carbonate de potassium) qui, en réaction1 avec du
Ca(OH)2 (lait de chaux) donne du KOH (potasse
caustique, alcali fort =base forte) et du CaCO3.
En mélange avec un triglycéride, cette base forte
produit le savon.
1 Réaction dite de "caustication" ou "caustification".
Saponification = Hydrolyse d'un triglycéride (graisse
ou huile animale ou végétale) en milieu basique par
NaOH ou KOH (t°80-100 °C pour accélérer la
réaction). Produit = glycérol + carboxylates
(= savon).
Exemple 1 : ester
R-CO-O-R + KOH ! R-CO-O-K + R-OH
Ester + base ! savon (ion carboxylate) + Alcool
Deuxième exemple : triglycéride
CH2-O-CO-R
⎢
CHO-O-CO-R + 3 KOH ! 3 K-O-CO-R +
⎢
CH2-O-CO-R
CH2OH
⎢
CHOH
⎢
CH2OH
Acide gras + Base
!
Savon + alcool
(triglycéride, (potasse (Ion (glycérol
huile…) caustique) carboxylate) =glycérine)
4.Savon dur ou savon mou ?
Si la base forte est du sodium (NaOH) on obtient un
savon dur.
Si la base forte est du potassium (KOH) on obtient
un savon mou.
Le savon à la potasse est d’une grande douceur, son
ph est souvent de 7, celui du savon à la soude
descend rarement sous 8.
5.D'où viennent le sodium ou le potassium
dans les cendres ?
5.1.Sodium : cendres de plantes maritimes
Ce qui est normal, vu la présence de sel marin
(NaCl) dans les sols en bord de mer.
1) la salicorne2 plante originaire des bords de mer
(plante halophyte).
1) La betterave3 plante originaire des bords de mer
(plante halophyte).
Zygophyllum fontanesii (Photo J.-Fr. Misonne, Lanzarote 16.10.2016)
2) La fabagelle de Desfontaines4 est également une
plante halophyte, au goût très saumâtre.
Les cendres de ces plantes sont donc plus riches en
2 BPSADM1CafO1AmaF Salsola soda, Soude vraie, SasSo.
3 BPSADM1CafO1AmaF Beta vulgaris ssp. maritima, Betterave maritime,
Strandbiet, BeaVm
4 BPSADM1ZygO1ZygF Zygophyllum fontanessi, Fabagelle de
Desfontaines, ZygFo

p. 3
sodium que celles d'autres plantes.
En brûlant ces plantes et en faisant macérer leurs
cendres, on obtient une solution alcaline riche en
NaOH comme signalé plus haut.
5.2.Potassium : cendres de bois de cheminée p.ex.
Ces cendres sont constituées de ¼-½ CaO (chaux),
±⅛ de potasse5 & soude et ±10% d'oxydes (Mg, Fe,
Mn…).
Mélange d'huile dans une solution où ont macéré des cendres de feu de
bois et dont on a gardé la solution riche en KOH. (Les cendres ont été
éliminées après lixiviation.)
6.Mode d'action du savon
Rappel : R-CO-O-R + KOH ! R-CO-O-K + R-OH
Ester + base ! savon (ion carboxylate) + Alcool/Eau
L'ion carboxylate (savon) est donc formé d'une
chaîne carbonée "R" et d'une tête carboxylate
"COO-". Il est représenté comme suit :
Représentation de l'ion carboxylate : Chaîne carbonée ("queue") "R"
hydrophobe (= hydrofuge) et tête hydrophile "COO-".
Le composé chimique R-CO-O-Na, appelé "savon" ou
"ion carboxylate" comprend deux groupements :
- le groupement "R" comprend une longue chaîne
hydrocarbonée hydrophobe ou lipophile (lipos
=graisse ; philos = ami) ; c’est la "queue" de la
molécule de savon.
- le groupement "–CO-O-Na" est hydrophile (qui a de
l’affinité pour l’eau) ; c’est la tête de la molécule
de savon.
L'ion carboxylate est un tensioactif, c.-à-d. qu'il
5 Pour étonnant que ce soit, en néerlandais, anglais et allemand, on
n'utilise pas le mot "potassium" mais "kalium"… alors que le mot
français en est dérivé ! Ce mot proveint en effet (pour le néerlandais)
de "potas", signifiant "cendre du pot".
modifie la tension superficielle des liquides dans
lesquels il se trouve.
Voici comment agissent les ions carboxylates (savon)
lors du nettoyage :
(http://toutsurlesbulles.free.fr/site/lesavon.html)
Action des carboxylates lors du nettoyage
Pour enlever une tache sur un tissu, il faut mettre
du savon dans l’eau car l’huile (p.ex.), étant
hydrophobe, ne se mélange pas à l’eau. Si on ajoute
du savon dans de l’eau, les chaînes carbonées
(queues) adhèrent à la tache, alors que les têtes
s'orientent vers l’eau.
Par frottement, la tache se sépare du tissu, formant
une "micelle" (sa surface étant hydrophile, elle ne
colle plus au tissu). Le rinçage emporte le savon &
la tache.
Micelle
7.Bibliographie
http://fr .wikipedia.org
http://toutsurlesbulles.free.fr/site/lesavon.html
http://translate.google.com
https://fr.wikipedia.org/wiki/micelle
https://gd.eppo.int
LODEN JOËL (2010). Plantes succulentes des Îles
Canarie. Guide d'identification facile. Espagne :
Turquesa. 368 p.
PERDOMO PERDOMO G.B. (2013). Lanzarote Cactus

p. 4
Garden. Las Palmas de Gran Canaria : Cabildo de
Lanzarote. 155 p.
REY ALAIN (1998). Le Robert Dictionnaire historique
de la langue française. Paris : Dictionnaires Le
Robert. 3 tomes.
SCERRI ERIC (2013). 3 Minutes pour comprendre les
50 éléme,ts les plus répandus en chimie. Paris : Le
Courrier du Livre. 160 p.
* * *
1
/
4
100%