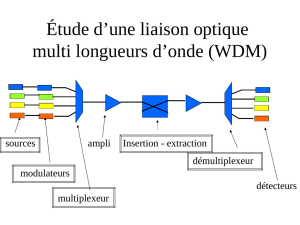
R 4

c
<Jf Par
spectrophotométrie,
on suit la
cinétique
de la
réaction
des ions iodure
I"(aq)
avec
les ions peroxodisulfate
S20s2"(aq)
qui conduit à la formation de diiode
(solution
jaune).
Cette
réaction
est totale. La
réaction
est
modélisée
par
l'équation
chimique
:
s2o82-(aq)
+
2
r
(aq)
—>
l2(aq)
+ 2
SO4
(aq)
Les
concentrations et volumes des
réactifs
introduits sont les suivants :
S2082"
: C, = 0,50
moLL'1,
V,
= 10
mL;
I'
: C2 = 0,020
moLL"1,
V2 = 10
mL,
On
a
mesuré
l'absorbance au cours du temps et obtenu la courbe ci-dessous :
A
2,0 '
'0
20 40 60 80
A.
Le
temps de
demi-réaction
vaut environ 10 min.
B.
L'ion
iodure est le
réactif
limitant
C.
La réaction étudiée étant
totale, la concentration finale doit
être
[LW
=
5
mmol.L'1.
D.
La
valeur du coefficient k pour la longueur
d'onde
choisie est
égale
à
400.102
L.mol"1.
E.
aucune des propositions
précédentes
n'est exacte
100
&J
On considère la réaction
Cr202"
+
14H+
+ 6F
—
2CrM +
3I2
+
7H20.
-jimi
ces affirmations concernant
cette
réaction,
lesquelles
:it
correctes ?
•
a.
d[Cr209"]/dt
=
1
/3d[I2]/dt.
•
b.
La
concentration en
Cr202~
diminue six
fois
plus
vite
que
celle
en
T.
• c.
Cr,+ se forme deux
fois
plus vite que
Cr:072~
ne
disparaît.
•
d.
tv(Cr202-)
=
^7(Cr,+).
j
•
e.
^(Cr20^)=2l7(Cr3+).
1
,
~<^H
- (ikfïtX
>
)
L'avancement
d'une
réaction
chimique totale varie avec le
temps suivant
féquation :
x(t) = t/(2t +
2).
f
en min
et x(t)
en mol.
Quelle
est la vitesse
initiale
de
cette
réaction
est en
mol.L_1.min_1
:
•
a.
0.4
•
b.
5
• c.
0,2
• d.
4
•
e. 0.5
Donnée :
volume
de
la
solution V =
10 dL.
^
On
réalise
une
série
de mesures d'absorbances A de solutions de violet
cristallisé,
à la longueur
d'onde
X
= 580 nm à l'aide d'un
spectrophotomètre
dont
la
cuve
a une
épaisseur
de 1,00 cm. On obtient les
résultats
suivants en fonction de la
concentration massique
t„,
des solutions : 0
tm
(gJL-1)
0,60.10J
1,50.10-J
2,40.10J
3,00.10J
4,50.10-J
6,00.10"j
A
0,150 0,500 0,840 1,030 1,550
2,080
Données
:
A.
L'inverse
de l'absorbance est la transmittance
été
choisie car
cette
radiation est bien
Formule
du violet
cristallisé
:
Q5H30CIN3
Masse
molaire de ce
composé
: M = 408
g.
mol"1.
Quelles
sont les affirmations exactes ?
A.
L'inverse
de l'absorbance est la trar—
B.
La longueur
d'onde
X = 580 nm a
transmise par la solution
C.
la loi de
Beer-Lambert
n'est pas valide pour
toutes
les concentrations
utilisées
dans
cette
expérience
D. Si
l'épaisseur
de la cuve
était divisée
par 2, on obtiendrait des valeurs
d'absorbance 2
fois
plus
élevées.
E.
Aucune des propositions
précédentes
n'est exacte
Vffc
Par hydratation du
3-méthylbut-l-ène,
on obtient un alcool A de
manière
majoritaire
et un alcool B de
manière
minoritaire.
L'oxydation
ménagée
par un
excès
d'oxydant de A conduit à la formation de A', celle de B conduit à la
formation
de
B'.
1) Les alcools A et B peuvent
décolorer
une solution de permanganate de
potassium
2) B' est
l'acide3-méthylbutanoïque
3)
L'oxydation
de
A'
est impossible
4)
La
réaction
de la
2,4-DNPH
sur B'
mène
à la formation d'un
précipité
jaune-
orangé
5) La
réaction
de la
2,4-DNPH
sur A'
mène
à la formation d'un
précipité
jaune-
orangé
6) La
réaction
de A* sur le
réactif
de
Tollens
mène
à la formation d'un miroir
d'argent
Quel
est le nombre
d'affïrmation(s)
exactes) ?
^
J A.0.
B.
I C.3 D.4 E.6 ^

A.
Ce
composé
peut
posséder
une
fonction
alcool
B. Ce composé
peut
posséder
une
fonction
cétone
C.
Ce
composé
peut
posséder
une
fonction
acide
carboxylique
D.
Ce
composé
peut
posséder
une
fonction
alcène
E.
Le composé précédent
peut
être
de la
1
-hydroxybutanone
(suite
du fl) Si le spectre
avait
été
obtenu en phase gazeuse
A.
le spectre obtenu aurait été identique
B.
le pic d'absorption large
situé
vers
3400
cm-1 serait
remplacé
par un pic fin à
a>3400
cm"1
C.
le pic d'absorption large
situé
vers
3400
cm"1 serait
remplacé
par un pic fin à
CT<3400 cm"'
D.
cette
différence
est due
aux
liaisons
hydrogène
en phase
condensée
E.
cette
différence
est due aux
interactions
de
Van
der
Waals
en phase
condensée
Le
spectre RMN d'un
composé
de formule
C3H9N présente
trois
signaux
différents
;
Signal
1 : un heptuplet, pour un
déplacement
chimique à
environ
3,1 ppm, pour
lequel
la courbe
d'intégration présente
un saut de h, = 0,7 cm
Signal
2
:
un singulet
vers
1,2 ppm pour
lequel
la courbe
d'intégration présente
un
saut
de
h2
= 1,4 cm
Signal
3 : un doublet
vers
1,1 ppm pour
lequel
la courbe
d'intégration présente
un
saut
de h3 = 4,2 cm
Quelles
sont les
affirmations
exactes ?
A.
Le composé
contient 2 groupes de protons
équivalents
B. Le composé
contient trois groupes de protons
équivalents
C.
Le
signal
3 correspond à un groupe de 6 protons
équivalents
D. Le
signal
1
correspond à un groupe comprenant
1
seul
proton
E.
Le
signal
2 correspond à un groupe de 2 protons
équivalents
(DM- (suite
du 1»)
» A. Il
existe
4
isomères
de formule brute
C3H9N.
B.
le
signal
3 montre que le groupe comprenant 6 protons est
voisin
du groupe
contenant
1
proton
C.
le
signal
1 montre que le groupe ne comprenant qu'un proton est
voisin
de 6
protons
équivalents
D.
le
composé étudié
est la
propylamine
E.
le
composé étudié
est la
2-méthyléthylamine
Un
composé
organique a pour formule
C5H|20
donne un spectre d'absorption
dans l'infrarouge qui
présente
une large bande d'absorption
vers
3300
cm ', et une
autre beaucoup plus
fine
à
3600
cm'.
Donnée
: tableau des bandes d'absorption en infrarouge du cours
Quelles
sont les propositions
exactes
?
A.
La
bande d'absorption à
3300
cm"'
est due à la
liaison
O-H
B. La
bande d'absorption à
3600
cm"'
est due à la
liaison
O-H
C.
La
différence
de nombre
d'onde
entre ces deux bandes montre que la
molécule
possède
deux groupements fonctionnels
différents
D. Le composé
peut
être
le
2-méthylpentan-2-ol
E.
Le composé
peut
être
le
2-méthylbutan-l-ol
'•jÊh
Un
composé
organique a pour formule
C5Hi0O.
Son spectre infrarouge
présente
une bande d'absorption à 1730
cm"1. 11
donne un
précipité
jaune
avec
la
2,4-DNPH
A.
Le composé étudié
est un ester
B. Le composé étudié
est un
composé carbonylé
C.
La
longueur
d'onde
à
laquelle
se situe le pic est de
1730
cm
D. La
longueur
d'onde
à
laquelle
se situe le pic est de 5,8
\xm
E.
Le composé
peut
être
du
2-méthylpropanal
(P Jj-
Un
extrait
du spectre infrarouge
d'une
molécule A,
obtenu en phase
condensée,
est
donné
ci-dessous.
Transmittance
(%)
Quelles
ont les
affirmations
exactes ?
1
/
2
100%