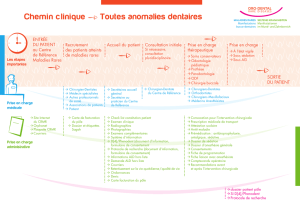
Gestes algogènes en dehors du bloc

GESTES ALGOGÈNES EN DEHORS DU BLOC :
ÉPIDÉMIOLOGIE, SÉDATION HORS BLOC PAR LES
NON-ANESTHÉSISTES, INDICATIONS
DE L’ANESTHÉSIE GÉNÉRALE
F. Dixmerias-Iskandar, F. Lakdja
Département d’Anesthésie-Réanimation-Analgésie, Institut Bergonié, Centre Régional
de Lutte Contre le Cancer, 229, cours de l’Argonne, 33076 Bordeaux Cedex
email : dixmerias @bergonie.org, [email protected]g.
INTRODUCTION
Les progrès réalisés ces dernières années dans les domaines du diagnostic et de la
thérapeutique des maladies ont été considérables. Les investigations et les soins sont plus
fréquents et plus prolongés. La prise en charge «globale» des patients est devenue une
nécessité sinon une obligation morale pour tout soignant. Le malade au centre de nos
préoccupations est la victime fréquente d’une «myriade de touche de douleur» comme
l’exprimait Philippe Brenot en 1992 [Les mots de la douleur, L'esprit du temps]. Cette
complexité algologique s’explique autant par les douleurs générées par les affections
que par les algies iatrogéniques. Dans ce contexte, les douleurs provoquées par les actes
médicaux sont légion. Elles pourraient se définir comme des douleurs aiguës, extempo-
ranément induites par des actes diagnostiques et/ou thérapeutiques. Nous exclurons donc
de notre propos les douleurs séquellaires.
Par ailleurs, la notion de «hors bloc» comprend des sites et des situations très diverses.
Il en est ainsi aussi bien du cabinet médical ou dentaire que des environnements extra-
hospitaliers, de la salle de de surveillance post-interventionelles. La question concernant
les actes d’imagerie mérite également un développement spécifique [1]. Quoi qu’il en
soit, la prise en charge de ces douleurs provoquées relève d’une obligation juridique.
L’article 40 du Code de Déontologie rapporte que le médecin doit s’interdire, dans
les investigations et interventions qu’il pratique comme dans les thérapeutiques qu’il
prescrit, de faire courir au patient un risque injustifié. Des investigations dites naguère
«sanglantes», aujourd’hui «invasives», comme des ponctions–biopsies ou relevant de
l’imagerie interventionnelle, peuvent entraîner des complications, qui seront considérées
avant que l’indication ne soit posée. Même des examens réputés plus anodins présentent
des inconvénients, proprement toxiques ou psychologiques, qu’on ne saurait sous-
estimer. On peut dire aussi que, comme des médicaments, ils ne se délivrent pas n’importe
comment, mais avec précautions, à certains moments, à certaines «doses».

MAPAR 2004
34
L’ article L II I0-5 du Code de Sa nté publique préci se : « … To u -
te personne a le droit de recevoir des soins visant à soulager sa douleur.
Celle–ci doit être en toute circonstance prévenue, évaluée, prise en compte et trai-
tée». La loi du 4 mars 2002 relative aux droits du malade, réaffirme l’obligation des
soignants et des établissements de santé à prendre en charge la douleur des patients. Ainsi,
la prise en charge de la douleur est un droit pour le patient et un devoir pour le médecin.
L’obligation de prise en charge est une obligation de moyens. Enfin, le programme de
lutte contre la douleur 2002-2005 est, entre autres, ciblé sur la douleur provoquée par les
soins et la chirurgie. Il rappelle l’importance de développer les protocoles définis dans la
circulaire 98/94 du 11 février 1999 relative à la mise en place des protocoles de prise en
charge de la douleur aiguë. Ces protocoles sont «indispensables à une prise en charge de
qualité. Ils sont considérés comme des prescriptions anticipées ou des conduites à tenir
lors de situations bien identifiées et décrites. Ils permettent notamment aux infirmiers
d’intervenir sans délai, de personnaliser la prescription et d’utiliser des procédures
reconnues pour leur efficacité».
Ainsi, tout médecin, eu égard à la loi et à la jurisprudence se doit de prodiguer des
soins consciencieux et conformes aux données actuelles de la science et reste tenu de se
former en conséquence.
1. ÉPIDÉMIOLOGIE
Les données publiées en la matière sont peu fréquentes ou peu exploitables. La plupart
des études ont concerné les enfants. Les enfants traités pour des cancers considèrent les
gestes diagnostiques ou thérapeutiques comme la partie de leur maladie la plus difficile
à supporter [2]. Murat apporte des réponses aux douleurs des gestes en se fondant sur
une revue d’études randomisées et contrôlées [3]. Pendant toute la durée des traitements,
aucune habitude du geste ni détente ne s’installe malgré leur répétition, ce qui peut com-
pliquer sérieusement la prise en charge thérapeutique [4].
Chez l’adulte, peu d’études de bonne méthodologie et relatives aux gestes
invasifs et à leurs conséquences ont été faites. On peut néanmoins noter un travail
récent : «Douleurs provoquées lors des actes diagnostiques, thérapeutiques et des
mobilisations en cancérologie chez l’adulte» dans les conditions d’une recherche
bibliographique effectuée sans limites sur l’antériorité de la recherche (Medline de
1966 à nos jours) et sur l’âge des patients (enfants et adultes). Les articles retenus ont
été sélectionnés sur la base du titre et du résumé ainsi que sur les critères de sélection
suivants (études contrôlées randomisées ou non, prise en charge de la douleur liée à
l’acte lui-même, ponctions lombaires, osseuses ou sanguines [veineuse ou artérielle],
patients adultes, critère principal correspondant à une diminution de la douleur mesurée
par des échelles validées [EVA…] [5]. Les résultats sont en cours de publication. Les
analyses des articles sont faites à partir d’une grille (Annexe). Salomon montre que 35 %
des patients hospitalisés un jour donné, déclaraient avoir eu mal lors d’un geste ou d’un
soin [6]. Une enquête en salle de surveillance postopérationnelle montre que, sur 70 %
des patients qui expriment une douleur, 38 % le font face à une douleur induite par le
soin [7]. Dans cette approche, huit actes douloureux ont été individualisés selon le critère
fréquence > 30% (sonde nasogastrique [présence, mobilisation, ablation], changement de
position du patient, premier lever, changement de lit, kinésithérapie respiratoire, réfection
de pansement, ablation de capteur artériel radial, présence d’une voie veineuse).

Douleur 35
2. GESTES ALGOGÈNES HORS BLOC
2.1. ACTES NOMBREUX ET VARIÉS
Dans ce cadre complexe, on peut néanmoins tenter de classifier les actes directement
et indirectement douloureux.
2.1.1. ACTES NON DOULOUREUX
On peut distinguer des actes non douloureux en eux–mêmes comme la réalisation
d’actes de radiologie, la radiothérapie... Ils nécessitent la mobilisation du patient (source
de douleur), de s’allonger sur une table d’examen froide et dure, aidé par un personnel
inconnu, générant un mal–être, une angoisse et indirectement des douleurs.
2.1.2. PROCÉDURES DOULOUREUSES
Les procédures douloureuses en elles-mêmes sont nombreuses tout le long de la
maladie : certaines le sont modérément (ponctions veineuses ou injections, certains
pansements, sondages urinaires, ponction lombaire…), mais par leur répétition du fait
de l’anxiété générée par cette fréquence, elles peuvent devenir très douloureuses voire
insupportables.
2.1.3. ACTES D’EMBLÉE DOULOUREUX
D’autres actes sont d’emblée douloureux (myélogramme, biopsie, ponction arté-
rielle…). Au cours de ces gestes douloureux, plusieurs types de douleurs sont décrits et
sont à considérer. Par exemple, pour le myélogramme, 3 douleurs sont distinguées : une
douleur aiguë lors de l’insertion de l’aiguille au niveau de la peau, une forte pression lors
du passage du périoste et une douleur intense et brève lors de l’aspiration de la moelle
[2, 8]. Ainsi, chaque étape douloureuse est à prendre en compte. L’anesthésie locale ne
sera efficace que lors de la ponction cutanée et non pour l’aspiration ; d’autres modes
d’analgésie seront donc à utiliser.
Enfin, certains gestes peuvent réveiller ou exacerber une douleur déjà présente.
Les gestes invasifs les plus fréquemment incriminés pour engendrer une expérience
désagréable peuvent être répertoriés comme suit :
• Ponctions et biopsies (ponction lombaire, pleurale, cutanée, prélèvement de moelle
osseuse, biopsie osseuse) ;
• Prélèvement veineux (pour bilan) ou artériel (pour analyse des gaz du sang) ;
•
Injections (IV, ponctions sous scanner ou sous échographie) pour examen d’imagerie ;
• Mise en place d’accès vasculaires divers (cathéters veineux et artériels, chambre à
cathéter implantables) ;
• Accès vasculaires, injections intraveineuses, sous-cutanées ;
• Injections intra-musculaires ;
• Exérèses de nodules sous-cutanés, biopsie cutanées…
Certains considèrent également les soins de plaies, les soins dentaires, l’extraction
de fécalomes… C’est dire la nécessité de lister tous ces actes, de les définir et de leur
opposer des attitudes antalgiques préventives et curatives.
Les patients présentant des affections chroniques subissent de nombreux actes «agres-
sifs» pour le diagnostic et les traitements (ponction lombaire, myélogramme, biopsie…).
Bien que les prélèvements veineux, la pose de perfusion, les injections intraveineuses ou
musculaires soient moins douloureuses, leur répétition au cours de la maladie génère une
angoisse très importante et il n’est pas improbable que le seuil de tolérance à la douleur
baisse proportionnellement à la durée de la maladie et à son évolution péjorative.
Lors de traitements intensifs, de nombreuses procédures invasives peuvent être néces-
saires chaque jour ou semaine. D’après Manne et al. [9], plus de 300 ponctions veineuses

MAPAR 2004
36
sont effectuées. Cet auteur rapporte une étude postérieure qui sera publiée quelques
semaines plus tard. 70 enfants (38 garçons et 32 filles âgés de 3 à 10 ans (moyenne 6,1
ans) présentant un cancer (sarcomes, lymphomes, leucoses, tumeurs solides, désordres
immunitaires).Les diagnostics ont été effectués en moyenne 32 mois auparavant (écarts :
2 à 83 mois) et les enfants ont subi en moyenne 93 ponctions veineuses (écarts : 2 à
300) pendant une durée moyenne de 80 jours (écarts 1 à 571 jours). Les ponctions ont
été effectuées pour prélèvements sanguins, chimiothérapie, anesthésie ou pour plusieurs
objectifs combinant les raisons précédentes. L’analyse des comportements parentaux lors
des procédures de ponction s’est faite auprès de 70 parents (55 mamans et 15 papas).
Trois facteurs interviennent pour expliquer la détresse : l’âge des enfants, les conditions
de l’accès veineux et les attentes et coopérations des parents (provoquant ou non une
distraction lors de l’acte). Ainsi, la détresse était supérieure chez les enfants les plus jeu-
nes qui subissaient quelques ponctions et qui avaient les accès veineux les plus pauvres
et chez lesquels les parents étaient les moins coopératifs. Il en ressort une expression
modérée de la douleur au cours des gestes invasifs répétitifs, mais pour certains patients
«chaque nouvelle piqûre est un pas vers la guérison » ou encore « la vie a un prix et il
faut le payer».
Dans tous les cas, la prise en charge de ces patients devrait être précédée par une re-
mise en question du praticien : pourquoi cet examen ou ce geste ? Dans quel but ? Est-ce
indispensable ? Sera-t-il répété ? Quel est le niveau de douleur prévisible et sa durée ?
Quelle est le niveau et la durée de l’anxiété à venir ? Comment le patient pense-t-il réagir ?
Le patient est-il suffisamment informé ?
La prise en charge de la douleur et du stress générés par les différentes actions inva-
sives, devrait comprendre le type de procédure, le niveau prévisible de douleur et des
facteurs individuels tels l’âge et le statut physique et psychique du patient.
3. MOYENS THÉRAPEUTIQUES PRÉVENTIFS ET CURATIFS
3.1. MOYENS NON-PHARMACOLOGIQUES
Chez l’enfant, des traitements non-pharmacologiques ont montré leur efficacité
lors de ponctions lombaires, de myélogramme ou de biopsies. Il s’agit des méthodes
simples de distraction, de concentration, des exercices de respiration ou des méthodes
plus spécialisées comme l’hypnose [4, 8, 10], les techniques de relaxation, de sophro-
logie de biofeedback, relation d’aide, de toucher relationnel… [11, 12]. Des techniques
physiques, telles que l’application de froid ou de chaud, le massage, peuvent être asso-
ciées. Dans une étude randomisée récente [13], l’attention structurée et l’auto-relaxation
hypnotique ont prouvé leur bénéfice pendant des actes invasifs médicaux. L’hypnose pos-
sède des effets positifs plus prononcés sur la douleur et l’anxiolyse ; elle permet également
une stabilité hémodynamique supérieure, comparaison faite avec le bras témoin.
3.2. MOYENS PHARMACOLOGIQUES
3.2.1. CRÈME EMLA [14]
La crème Emla (Eutectic Mixture of Local Anesthetics) est un mélange équimolaire
de deux anesthésiques locaux, la lidocaïne et la prilocaïne. L’effet analgésique est obtenu
grâce à une diffusion au travers de la peau pour bloquer la transmission neuronale des
nerfs cutanés. Son action dépend du temps de pose et de la quantité appliquée. L'Emla
permet de prévenir la douleur induite par les effractions cutanées nécessitées par les
soins. Son efficacité a été largement démontrée chez l’enfant [15]. Les études rapportées
dans la littérature et l’expérience de la pratique clinique montrent que l’efficacité de la
crème EMLA est nette surtout quand la ponction est réussie lors de la première tentative.

Douleur 37
Si la ponction est difficile, l’effet analgésique diminue car des plans plus profonds non-
anesthésiés sont stimulés. Elle peut être utilisée dans de nombreuses procédures mais
le temps de pose doit être respecté car la profondeur de l’analgésie obtenue varie avec
le temps : 60 mn d’application confèrent une analgésie d’une profondeur de 3 mm, la
profondeur maximale est de 5 mm après 120 mn d’application [16].
Ainsi, lors d’une ponction lombaire, elle est efficace pour la douleur superficielle,
mais elle n’empêche pas la douleur plus profonde créée par la ponction du ligament jaune
et d’autres moyens analgésiques doivent être associés.
Site Durée d’application conseillée
Ponction veineuse
Ponction artérielle
Ponction lombaire
Ponction sus-pubienne
Ponction pleurale
60 mn
120 mn
90 - 120 mn
90 - 120 mn
90 - 120 mn
Il existe d’autres utilisations que les ponctions citées ci–dessus :
• L’ablation de drains thoraciques : posée 3 h avant le geste, son efficacité est supérieure
à celle de la morphine IV (0,1 mg/kg) injectée 30 mn avant le geste ;
• La circoncision ou l’exérèse d’une lésion prépuciale superficielle.
Après application de 1 à 2 h, l’anesthésie cutanée dure environ 2 heures. L’efficacité de
la crème en tube ou en patch est identique.
L’utilisation de la crème Emla est reconnue. Son utilisation doit être systématique pour
certains gestes en respectant les temps d’application :
• Les ponctions veineuses et les poses de cathéters courts intraveineux,
• Les ponctions artérielles et les poses de cathéters artériels,
• Les poses de cathéters centraux (associée à une prémédication ou une sédation),
• Les ponctions lombaires,
• Les ponctions pleurales et autres ponctions ou biopsies en complément de l’infiltration,
alors facilitée par un anesthésique local.
3.2.2. ANESTHÉSIQUES LOCAUX
Hormis la crème Emla, la lidocaïne, bupivacaïne et ropivacaïne sont des substances
qui, administrées au voisinage d’un nerf, bloquent la conduction nerveuse de ce nerf
pour une période allant de une à six heures. L’utilisation de dose faible favorise le bloc
sensitif et épargne le bloc moteur. De nombreux territoires tronculaires (poignet, main,
cheville, pied, face, thorax, etc.) peuvent être bloqués avec ces substances et avec un très
grand coefficient de sécurité. Les gels et les sprays de lidocaïne donnent rapidement une
très bonne anesthésie au niveau des muqueuses.
Plusieurs formes de lidocaïne sont utilisables : gel, crème, solution, spray.
• La lidocaïne visqueuse à 2 % peut être employée pour l’anesthésie de la cavité buccale,
en massage sur les zones à anesthésier : muqueuse gingivale, aphtes, plaie de langue,
passage d’une sonde (application renouvelable toutes les 4 h).
• La lidocaïne, gel urétral à 2 %, permet l’anesthésie de l’urètre avant exploration ; elle
peut également être utilisée pour lubrifier une sonde œsophagienne ou trachéale.
• La lidocaïne spray à 5 % permet l’anesthésie de la sphère orolaryngée (attention au
risque de fausses-routes dans les 2 h qui suivent une pulvérisation).
• La lidocaïne à 1 % (utilisation d’un tampon imbibé de 1 à 2 ml de solution) peut être
utile par exemple avant l’infiltration des berges d’une plaie, avant suture ou avant la
pose d’une sonde gastrique pour anesthésier la muqueuse nasale.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%